Burgess 脱水反应
重要性
[开创性文献1,2;综述3,4;改进与优化5-17]
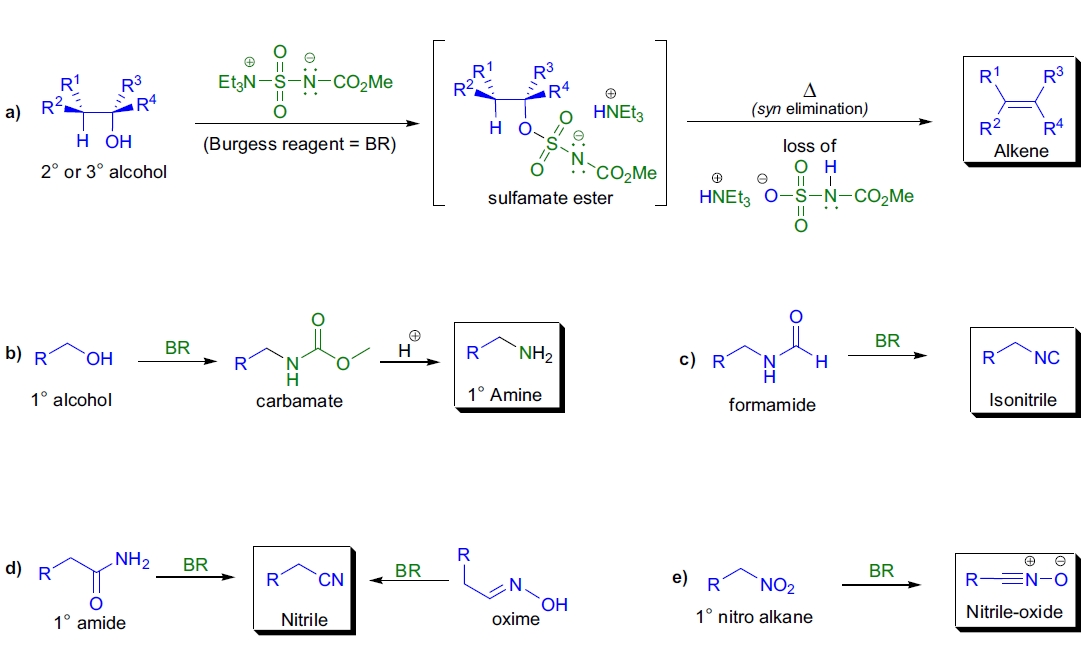
Burgess 脱水反应是 E.M. Burgess 在 20 世纪 70 年代早期发现的一种二级和三级醇脱水方法,使用 (甲氧羰基亚磺酰)三乙基铵氢氧化物的内盐(即 Burgess 试剂)生成相应的烯烃。该反应的显著优势是其温和条件(低温和中性介质),因此即使是对酸敏感的底物也能以优异的产率进行转化。脱水反应具有 syn 选择性,二级醇的 syn 选择性较高。三级醇的反应速率更快且条件更温和,但若生成稳定的碳正离子,则可能观察到 E1 消除产物。初级醇在反应中形成相应的氨基甲酸酯,经水解后生成伯胺。Burgess 试剂适用于多种官能团,包括环氧化物、烯烃、炔烃、醛、酮、卤代烃、缩醛、酰胺和酯等,使得高度官能化分子的高效脱水成为可能。
机理1,2
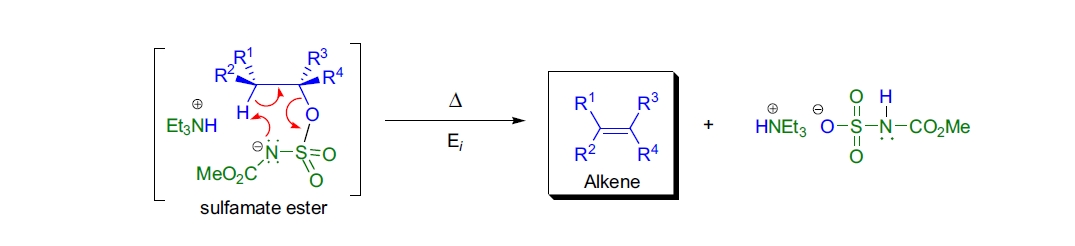
该反应的机理涉及通过亚磺酸酯中间体的离子对形成进行的立体专一性 syn 消除,与 Chugaev 消除(黄原酸酯的脱水)类似。动力学和光谱数据表明,反应的速率决定步骤是离子对的形成,随后快速发生 cis-β-质子转移。
合成应用
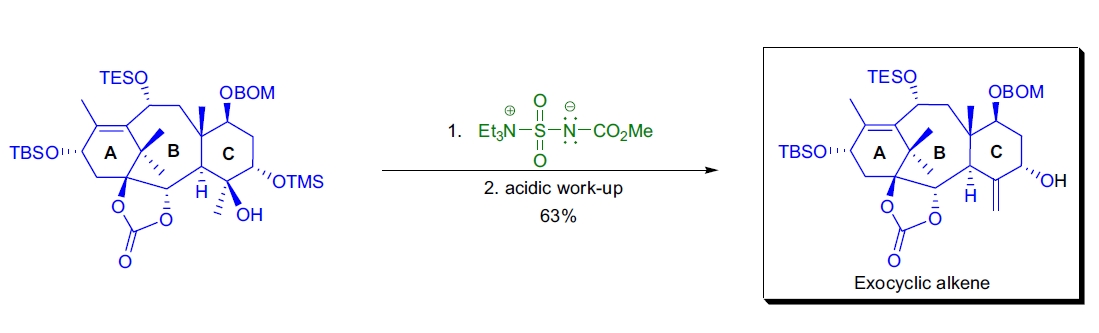
1. Taxol® 的全合成:R. Holton 等人在首次全合成 Taxol® 的过程中,通过 Burgess 脱水反应在 C 环上引入外亚甲基基团,为后续 D 环(氧杂环丁烷)的形成奠定了基础。该方法应用于复杂的三环三级醇中间体,最终生成目标烯烃,产率为 63%18。
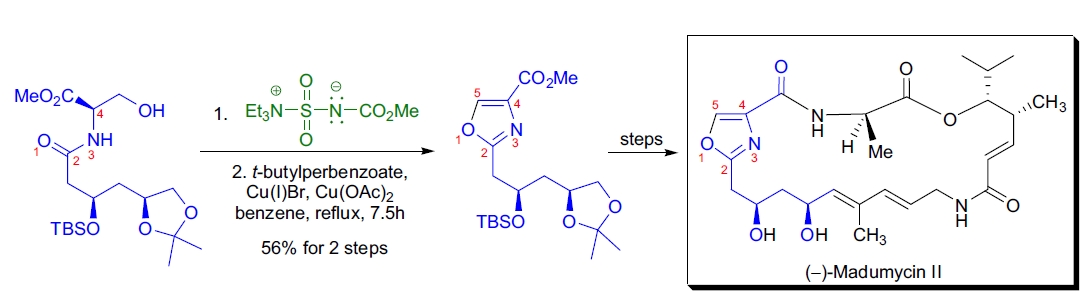
2. (–)-Madumycin II 的全合成:A.I. Meyers 等人首次实现了链阳肽抗生素 (–)-Madumycin II 的对映选择性全合成,其中氧唑部分被视为脱氢肽的掩蔽基团。该氧唑单元通过 Burgess 脱水环化反应生成的氧唑啉中间体,经氧化后转化为目标氧唑19。
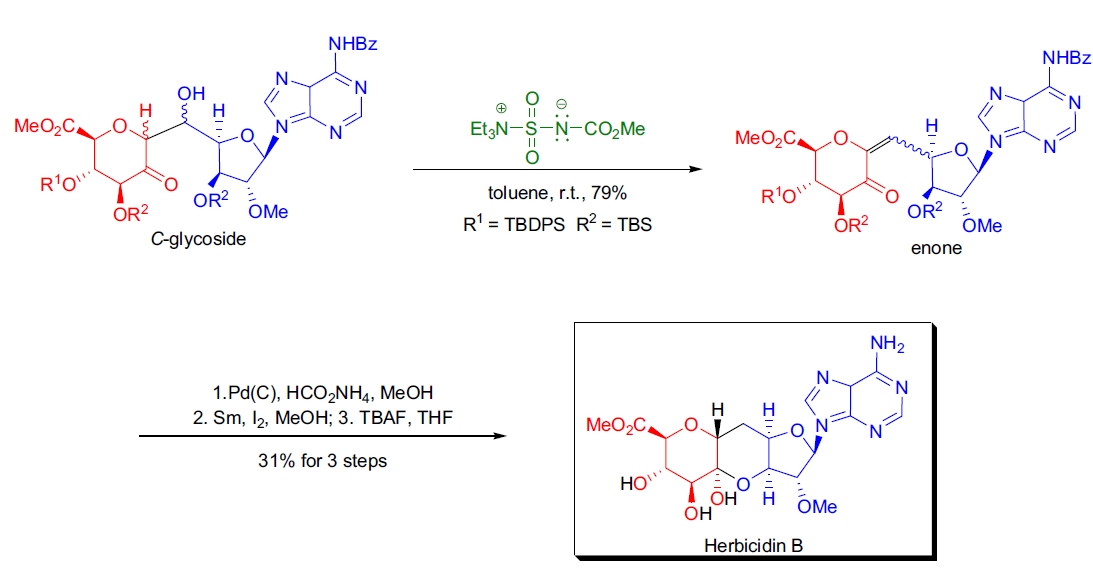
3. Herbicidin B 的全合成:A. Matsuda 等人通过 SmI2 促进的新型醛醇型 C-糖苷化反应,首次合成了核苷类抗生素 Herbicidin B。在关键步骤之后,生成的二级醇基团经 Burgess 试剂处理后去除,得到 α,β-不饱和酮,随后经氢化和保护基去除等步骤完成目标化合物的全合成20。