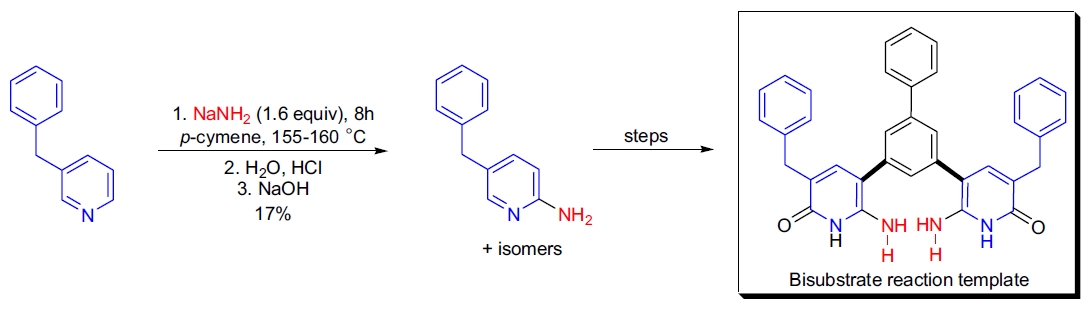
Chichibabin 反应
重要性
[开创性文献1,2;综述3-8;改进与优化9,10]
Chichibabin 反应是一种通过亲核芳香取代反应(SNAr)将氨基直接引入吡啶及其衍生物的反应。该反应是由 A.E. Chichibabin 在 1900 年代早期开发的,他通过将吡啶与钠胺(NaNH2)在二甲胺中加热至 110 °C,制备了 2-氨基吡啶,产率为 80%1。随后,他通过将吡啶加入粉末 KOH 中,在 320 °C 加热后分离出 2-羟基吡啶2。Chichibabin 反应广泛应用于杂环化合物的氨基化反应,包括喹啉、异喹啉、喹唑啉等。
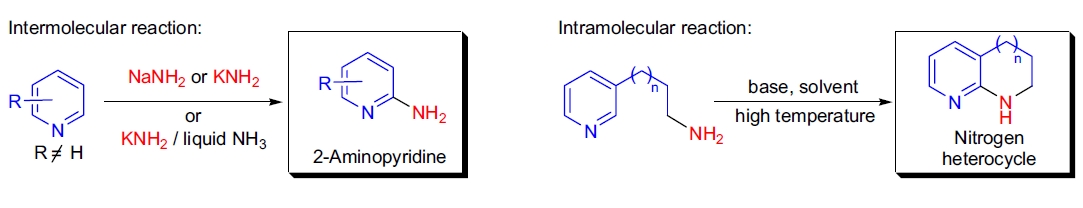
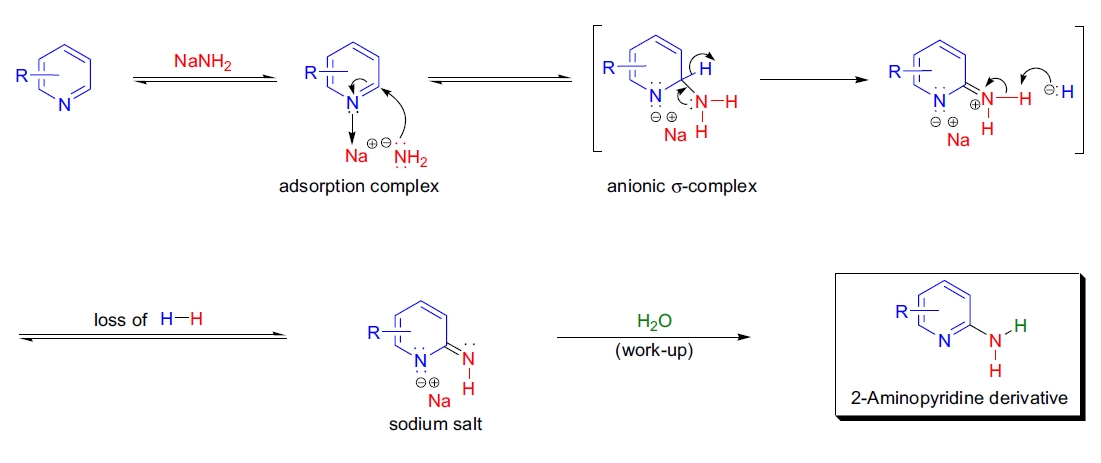
机理15-26,7
Chichibabin 反应的机理是通过氢负离子(H-)被氨基负离子(NH2-)亲核芳香取代实现的。第一步是钠离子与吡啶氮原子的配位,增加环 α-碳的正电性,促进 σ-复合物的形成。随后,σ-复合物脱去氢负离子并恢复芳香性,同时释放氢气(H2)。此过程可通过监测氢气体积来跟踪反应进程。
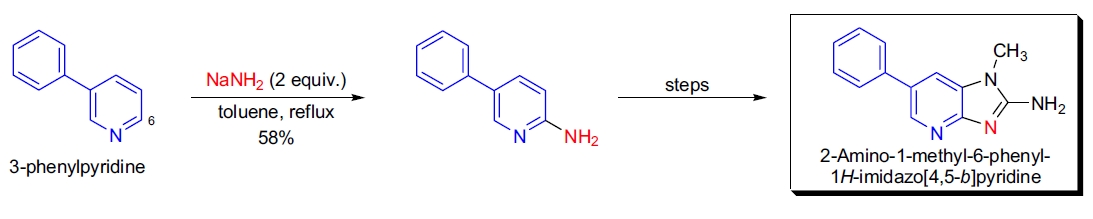
合成应用
1. PHIP 的合成:在 J.S. Felton 的实验室中,通过 Chichibabin 反应以 58% 的产率从 3-苯基吡啶合成了突变源 PHIP 的 6-氨基化合物27。
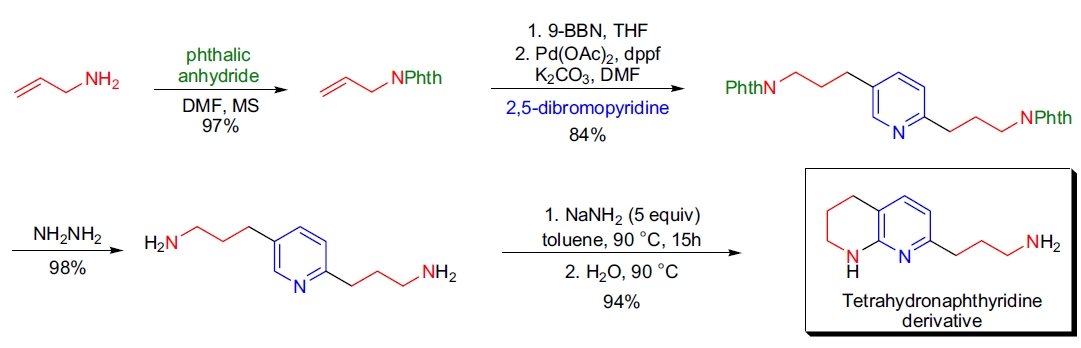
2. 大量制备氨基化合物:M. Palucki 等人通过一锅双 Suzuki 反应和高度区域选择性的 Chichibabin 环化反应合成了 2-[3-氨丙基]-5,6,7,8-四氢吖啶,该方法适用于大规模生产14。
3. 配体合成:A.N. Vedernikov 等人通过双 Chichibabin 缩合反应设计并合成了 [2.n.1]-2,6-吡啶环族配体,用于三齿面配位29。