Feist-Bénary 呋喃合成
重要性
[开创性文献1,2;综述3;改进与优化4-6]
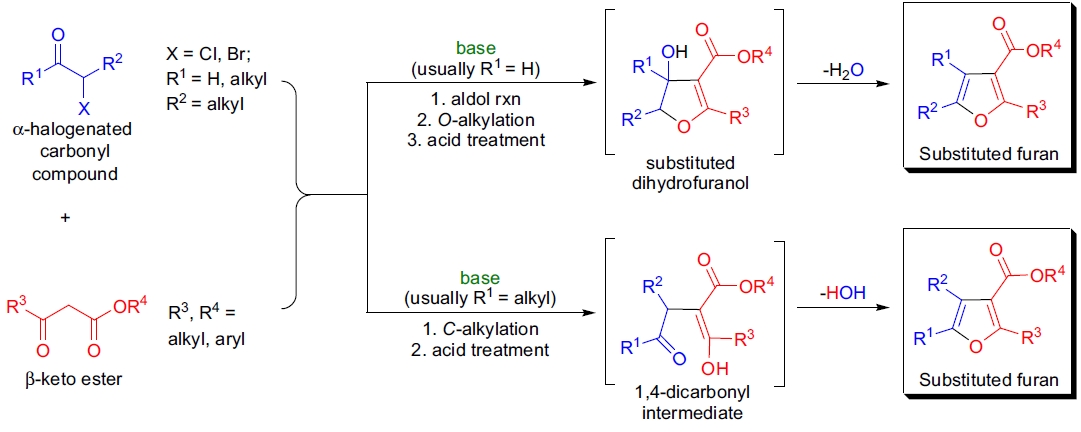
在碱性条件下,将 β-酮酯与 α-卤代羰基化合物(醛或酮)反应生成呋喃的过程被称为 Feist-Bénary 呋喃合成。此反应的特点包括:
- 1)产率对底物敏感,通常为中等;
- 2)反应的初始产物通常是二氢呋喃醇(“中断型 Feist-Bénary 反应”),在酸催化条件下脱水后分离出取代的呋喃;
- 3)区域化学结果取决于 α-卤代羰基化合物的反应性:α-卤代醛(R1=H)通常首先发生醛醇反应,然后发生 O-烷基化,而 α-卤代酮(R1=烷基)则首先 C-烷基化 β-酮酯,需要酸处理才能获得取代呋喃;
- 4)常用碱包括 NaH、NaOMe、NaOEt、NaOH 水溶液或 Et3N;
- 5)该反应对 β-二羰基化合物的性质具有普遍适用性:除 β-酮酯外,β-氧基丙酸酯、β-二酮和 β-二醛也可使用;
- 6)中断型 Feist-Bénary 反应的立体选择性取决于亲核试剂的碱性:使用中等酸性 β-二羰基化合物生成的亲核试剂主要形成顺式异构体,而高度酸性 β-二羰基化合物主要生成反式异构体。
Feist-Bénary 反应的几种改进方法包括:
- 1)β-酮酯与 1,2-二溴乙酸酯缩合,高产率得到 2,3-二取代呋喃;5
- 2)在 Cu(II)盐存在下,β-酮酯钠盐与 3-卤代炔烃(炔丙基卤化物)烷基化,得到烷叉呋喃,酸处理后异构化为四取代呋喃;9
- 3)加热 β-酮酯与 5-羟基-5H-呋喃-2-酮,在 Et3N 存在下生成 3-烷氧羰基呋喃。10
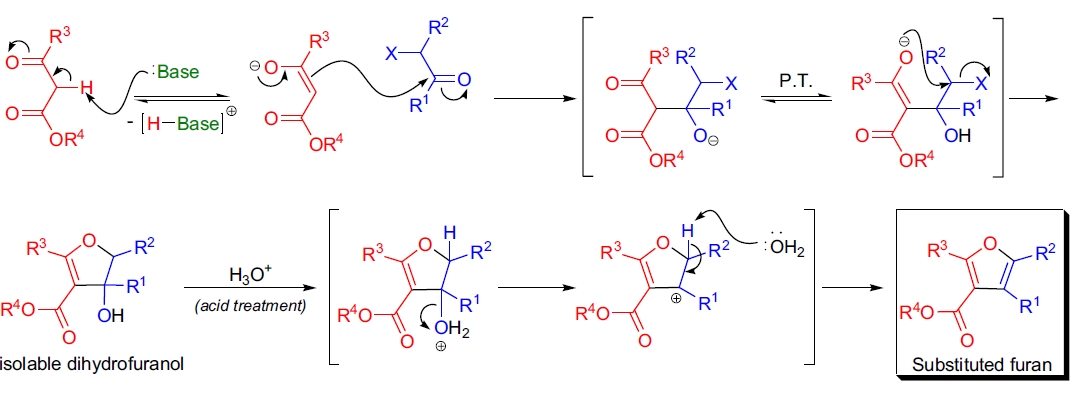
机理11,12
Feist-Bénary 呋喃合成的第一步是 β-酮酯在 α-碳上的去质子化。生成的稳定烯醇负离子与 α-卤代羰基化合物的羰基发生醛醇反应。随后,质子转移生成稳定的烯醇负离子,该负离子通过分子内 SN2 反应取代 α-卤原子。所得的二氢呋喃醇通常可分离,并在水性酸处理下生成取代的呋喃。
合成应用
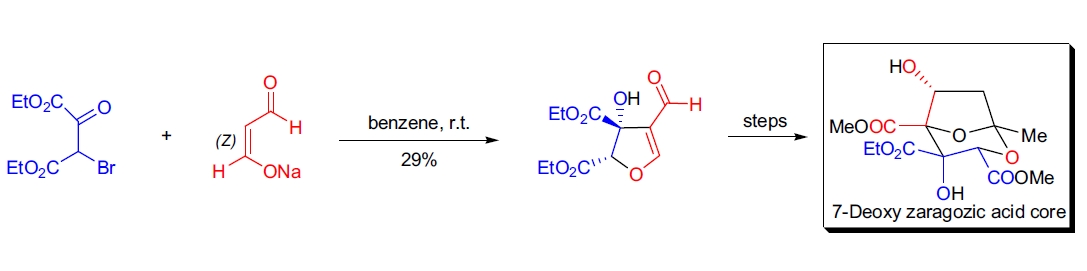
1. 7-去氧 zaragozic acid 核心结构的高效合成:M.A. Calter 等人基于“中断型” Feist-Bénary 反应开发了该结构的组装方法。使用丙二醛的钠烯醇与 2-溴-3-氧代-二乙基琥珀酸酯在室温苯中反应,获得 29% 的顺式二氢呋喃醇。该产物经过四步反应转化为 zaragozic acid 核心结构。13
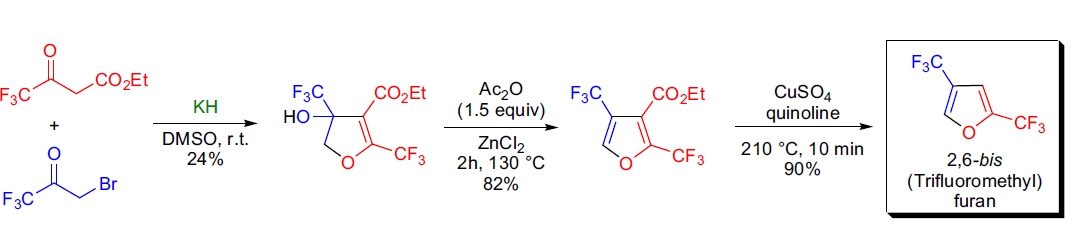
2. 2,4-双(三氟甲基)呋喃的合成:R. Filler 等人通过 Feist-Bénary 反应开发了一种合成 2,4-双(三氟甲基)呋喃的高效方法。14
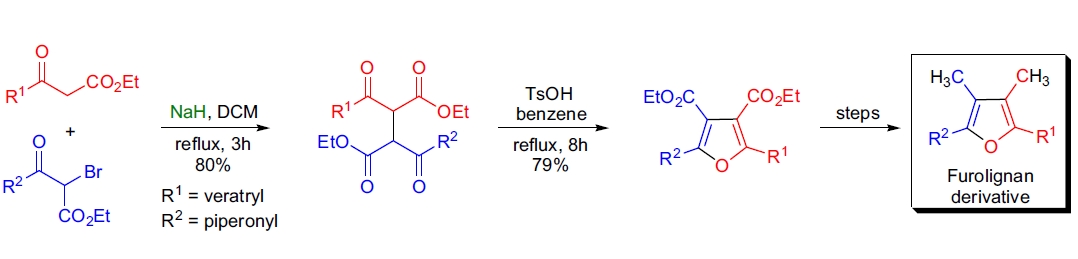
3. Furolignans 的合成:P. Xinfu 等人通过 Feist-Bénary 反应成功构建了含两个不同芳基的 furolignans。15
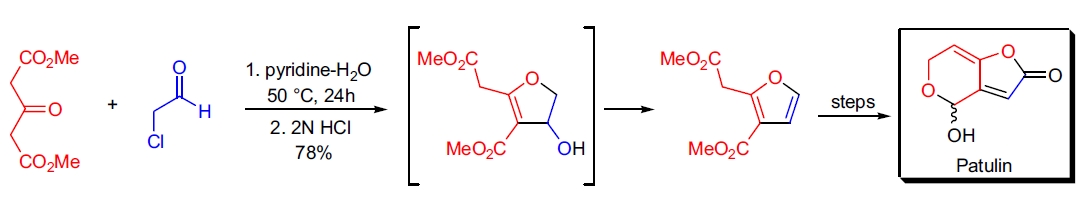
4. 真菌毒素 patulin 的合成:M. Tada 实验室通过 Feist-Bénary 反应合成了所需的 2,3-二取代呋喃,随后经过官能团修饰和氧化反应最终得到天然产物。16