烯反应
Ene reaction
重要性:
[开创性文献1-6;综述7-33;理论研究34-44]
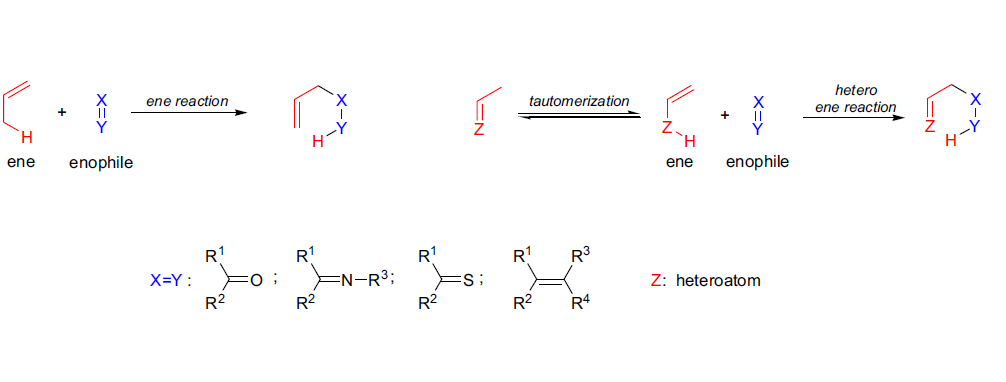
1943年,K. Alder系统地研究了涉及烯烃的烯基C-H键活化及其共轭双键转移的反应4-6,这些反应被称为烯反应(ene reaction)。它可以看作是烯烃与双键(C=C或C=O)的加成,是形成C-C键最简单的方法之一。含有烯丙基氢原子的烯烃参与的烯反应被称为“烃烯反应(carba-ene reaction)”。在没有催化剂的情况下,反应需要烯烃具有吸电子取代基(EWG)。这种吸电子化合物被称为烯受体(enophile)。
烯反应根据所使用的烯受体存在多种变体。7-9,11,12,45,14-16,46,18-20,24,47,27-30 烯烃作为烯受体的反应活性相对较低,而炔烃的烯受体活性更强。例如,在高压下,乙炔可与各种简单烯烃反应形成1,4-二烯。当烯受体为羰基化合物时,烯反应通常生成相应的醇而非醚(羰基-烯反应)。然而,硫羰基化合物反应时主要生成烯丙基硫化物而不是均烯丙基硫醇。
由醛生成的席夫碱可生成均烯丙基胺(烯亚胺,氮杂烯或杂烯反应)19。在钯、铂、镍等催化剂的作用下,金属-烯反应已成功应用于分子内体系。烯反应能兼容反应组分上存在的多种功能基团,例如附加的硅基、烷氧基或氨基,这些改性可增加对区域选择性的控制。烯反应可具有很高的立体选择性,添加路易斯酸(如RAlX2、Sc(OTf)3、LiClO4等)可使活性较低的烯受体发生反应。反应的区域选择性受氢原子的空间位阻影响,通常原子序数越低的氢被优先抽取。反应组分的功能化,如引入硅基、烷氧基或氨基,能够改变立体和电子特性,从而提高对反应区域选择性的控制。
机理48-52,31
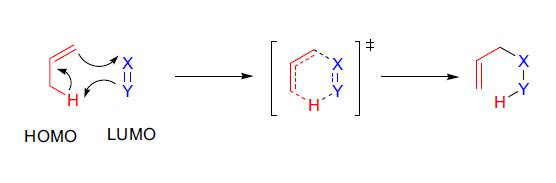
烯反应的机理与更为人熟知的Diels-Alder反应有关,据信它通过六元环芳香过渡态进行50,51。热的分子间烯反应具有较高的负激活熵,因此烯反应需要比Diels-Alder反应更高的温度。苛刻的反应条件导致了烯反应初期的稀少。然而,分子内的烯反应更容易进行。
烯受体与烯组分以“同面(syn-fashion)”方式反应,这表明反应是协同进行的。存在于烯组分的最高占据分子轨道(HOMO)与烯受体的最低未占分子轨道(LUMO)之间的前沿轨道相互作用促进了烯反应。烯反应受烯受体上的吸电子取代基、烯组分的应变及其有利的几何排列的推动。一些热的烯反应,如环戊烯与二乙基叠氮二甲酸酯(DEAD)之间的烯反应,由自由基引发剂催化,因此对于这些过程,建议为逐步双自由基途径。
应用
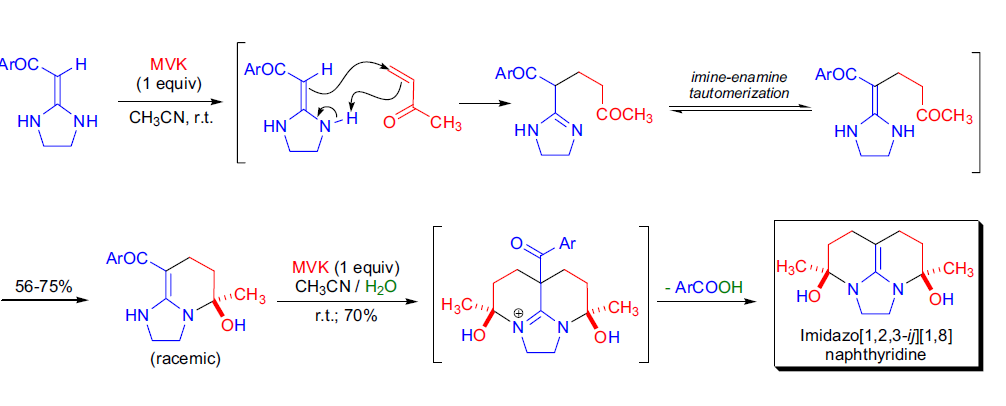
近年来,烯亚胺反应在合成咪唑并[1,2-a]吡啶和咪唑并[1,2,3-ij][1,8]萘啶衍生物中得到了应用。54
该反应是由杂环酮胺与烯酮(如甲基乙烯酮)发生的烯亚胺加成反应,然后通过分子内环化生成产物。
B. Ganem及其同事通过不对称金属促进的烯环化反应,成功实现了(-)-α-卡因酸的全合成52。在环化过程中,手性双噁唑啉-镁高氯酸体系强烈偏向顺式二面体异构体的生成。从易得的起始材料出发,用六步合成方法以超过20%的总收率制备了对映体纯的卡因酸。
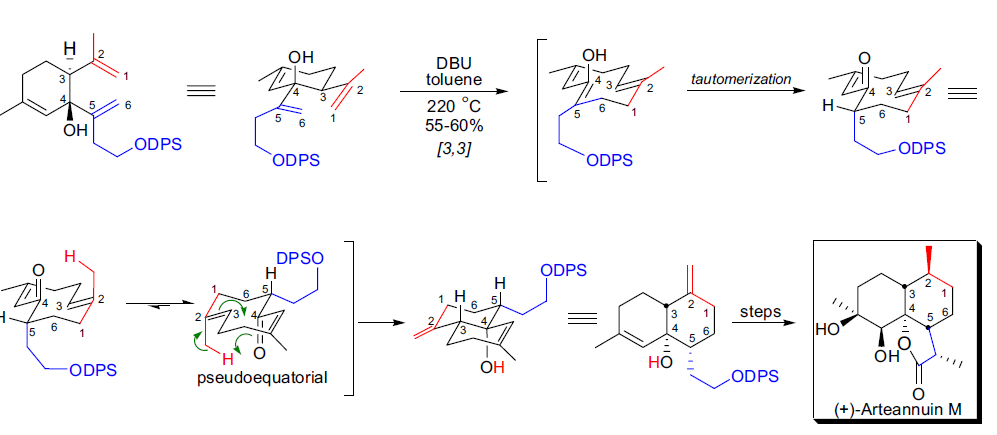
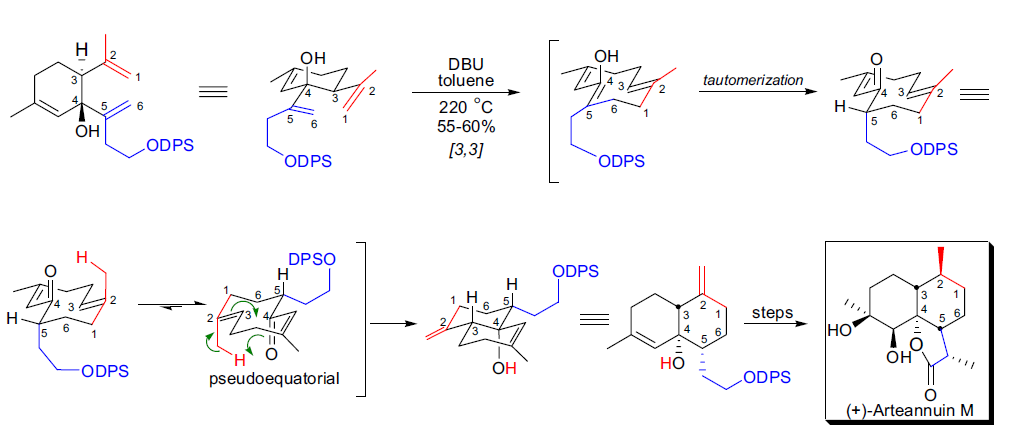
L. Barriault等人通过串联氧Cope/跨环烯反应作为关键步骤,完成了(+)-青蒿素M的首次全合成55。串联反应以很高的二面体选择性和对映体选择性进行。