乙酰乙酸酯合成法
acetoacetic ester synthesis
重要性:
[开创性文献1-4;综述5-9;改进与优化10-19]
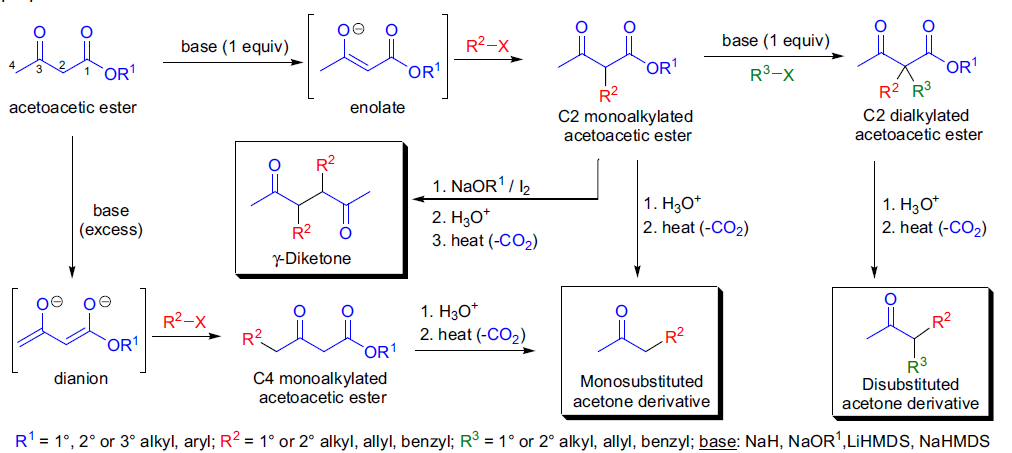
通过 3-氧代丁酸酯(acetoacetic ester, 乙酰乙酸酯)的C-烷基化制备酮类化合物的反应称为乙酰乙酸酯合成。 根据使用的碱量,乙酰乙酸酯可以在C2位置或同时在C2和C4位置去质子化。 C2位置的C-H键受到相邻两个羰基的电子吸引效应活化。这些质子具有相当强的酸性(C2位置的pKa约为11,C4位置的pKa约为24)。在加入一个当量的碱(如醇钠、LDA、NaHMDS或LiHMDS等)时,C2位置优先去质子化,生成的阴离子可以与各种烷基化试剂反应。 通过加入另一个当量的碱(乙醇钠, LDA, NaHMDS 或者 LiHMDS)和烷基化试剂,还可以实现C2的第二次烷基化。 当乙酰乙酸酯与过量的碱反应时,会生成对应的二价阴离子(扩展烯醇盐)。13-15,18,19
随后,加入亲电试剂(如烷基卤化物),首先在最具亲核性的C4位置发生烷基化。 所得的烷基化乙酰乙酸酯衍生物可以根据反应条件进行两种类型的水解裂解:
- 酸性水解水解酯基后,生成的β-酮酸发生脱羧反应,生成酮类化合物(单取代或双取代的丙酮衍生物)。
- 碱性水解 碱性条件下的逆Claisen反应:生成的产物在质子化后形成酸类化合物。
- 稀酸水解最常用,因为反应混合物中不会出现由酮裂解副产物引起的污染。最近,Krapcho脱羧反应的应用允许在中性条件下实现脱羧反应。11,12
机理3,20
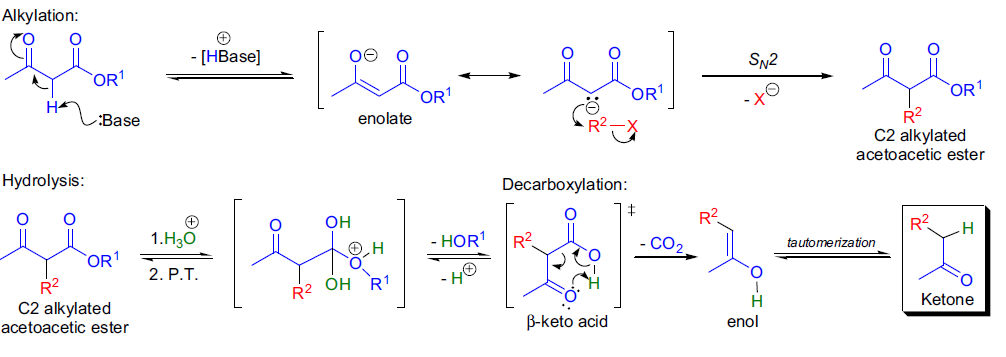
- C2位置去质子化
- 亲核取代(SN2)
- 水解和脱羧
在反应的第一步中,乙酰乙酸酯在一个当量碱的作用下在C2位置去质子化,生成烯醇盐(enolate)。 由于羰基的电子吸引效应,C2位置的质子较易被移除。
所得的烯醇盐具有亲核性,可以与亲电性的烷基卤化物发生SN2反应,生成C2取代的乙酰乙酸酯。此产物可以被分离纯化。
将C2取代的乙酰乙酸酯与水性酸处理,酯基发生水解生成相应的β-酮酸。由于β-酮酸的热稳定性较差, 它会通过六元环过渡态发生脱羧反应,生成目标酮类化合物。
备注: 此机理强调了碱催化去质子化和SN2反应的关键步骤,以及酸性条件下的水解和热诱导的脱羧反应的不可逆性。
应用
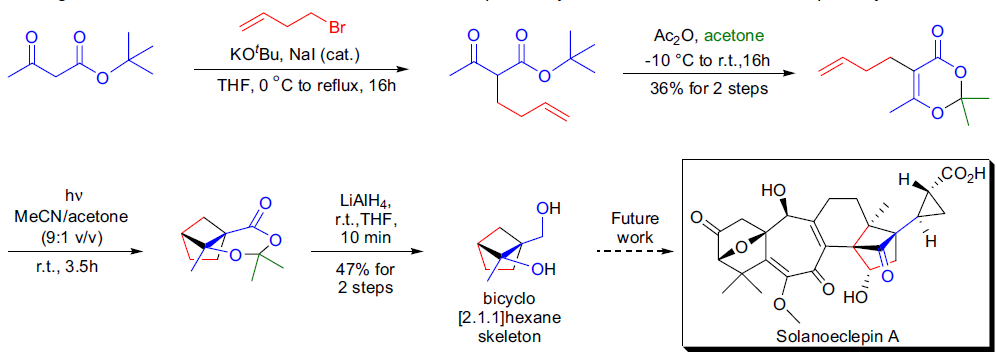
在H. Hiemstra实验室,研究人员利用分子内光化学二噁烯酮-烯烃[2+2]环加成反应合成了solanoeclepin A 的二环[2.1.1]己烷子结构。21
- 原料准备 二噁烯酮前体通过乙酰乙酸酯合成法从市售的叔丁基乙酰乙酸酯制备而得。
- 光化学环加成反应: 将该二噁烯酮前体在300 nm波长的光下照射约4小时后,观察到起始物质完全转化, 并以可接受的收率获得了预期的环加成产物。
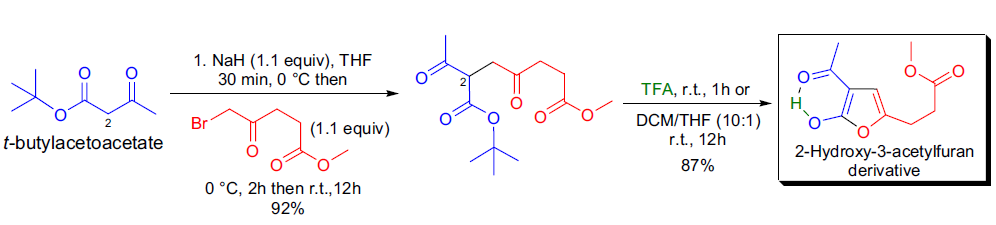
R. Neier等人通过叔丁基乙酰乙酸酯与α-卤代酮的烷基化反应,随后用三氟乙酸(TFA)处理中间体,成功合成了取代的2-羟基-3-乙酰基呋喃。22
- Feist-Bénary反应 当β-酮酯与α-卤代酮用于合成呋喃时,这一反应被称为Feist-Bénary反应。
- 二次烷基化与三取代呋喃的合成 对C2位烷基化的中间体进行第二次烷基化(使用各种溴代烷),生成2,2-二取代产物。这些产物在用TFA处理后,进一步生成三取代呋喃。