羟醛缩合反应
ALDOL REACTION
重要性:
[开创性文献1-4;综述5-9;改进与优化10-44]
羟醛缩合反应涉及含羰基化合物的烯醇或烯醇盐(亲核试剂)与醛或酮(亲电试剂)的加成反应。反应的初始产物为β-羟基羰基化合物,在一定条件下发生脱水生成相应的α,β-不饱和羰基化合物。 该转化反应因3-羟基丁醛而得名,3-羟基丁醛是乙醛经酸催化自缩合的产物,通常称为醇醛。 最初,羟醛缩合反应是在Brönsted酸或Brönsted碱催化下进行的,但这些过程会受到副反应如自缩合、多聚缩合、脱水以及Michael加成的影响。 烯醇盐预先形成和应用的方法的发展是羟醛缩合方法学中的一个突破。 在羟醛缩合反应中,最常用的烯醇盐是锂烯醇、硼烯醇、钛烯醇和硅烯醇醚,但还研究了多种其他烯醇盐衍生物,如镁、铝、锆、铑、铈、钨、钼、铼、钴、铁和锌的烯醇盐。 烯醇盐的形成可以以高度区域和立体选择性的方式进行。 立体化烯醇盐的羟醛缩合反应具有高度的非对映选择性。 (E)-烯醇盐通常生成抗型产物,而(Z)-烯醇盐则产生syn型产物作为主要的非对映体。 硅烯醇醚的Lewis酸介导羟醛缩合反应(Mukaiyama羟醛缩合反应)通常提供anti产物。
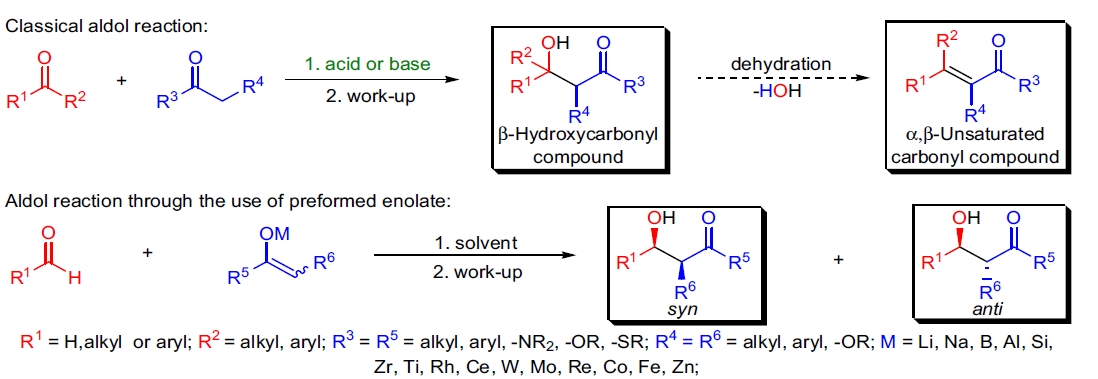
通过使用对映纯的起始物(试剂控制)或不对称催化可以控制反应的绝对立体化学结果。
试剂控制可以通过:
- 在烯醇组分中使用手性辅助试剂,如噁唑烷酮(也见Evans羟醛缩合)、生物碱基、吡咯烷酮、芳磺酰基苯醇、去甲肾上腺素和双(异丙基苯基)-3,5-二甲基酚衍生物;
- 在硼烯醇盐上施加手性配体,例如异品樟脑配体、薄荷酮衍生的配体、酒石酸衍生的硼酸盐和C2对称的硼烷;
- 使用手性醛。
不对称催化羟醛缩合反应可以通过:
- 生物催化,应用酶或催化性抗体;
- 手性金属络合物介导催化;
- 利用小有机分子的有机催化来实现。
机理7,12,13
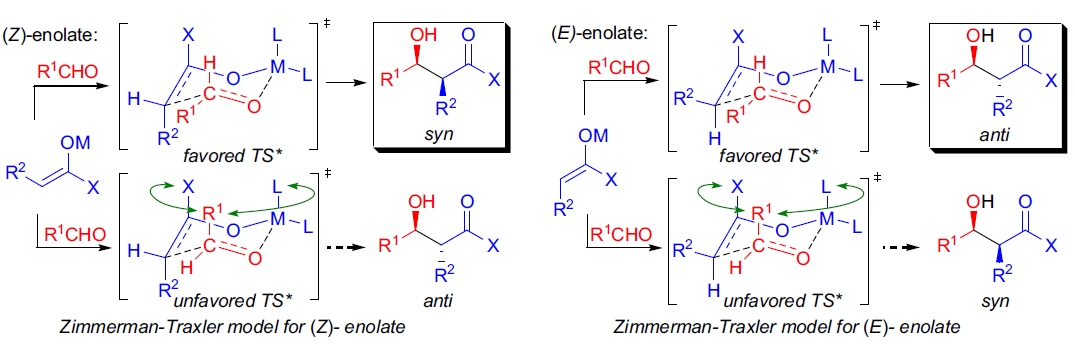
经典的酸催化羟醛缩合反应的机理涉及烯醇的形成平衡,烯醇作为亲核试剂。 亲电试剂的羰基通过质子化被活化以进行亲核攻击。 在碱催化的反应中,烯醇盐通过去质子化形成,随后烯醇盐加到羰基上。 在两种情况下,反应经历多个平衡步骤,产物的形成是可逆的。 预先形成的烯醇盐的羟醛缩合反应通常提供高非对映选择性的产物,(Z)-烯醇盐生成syn产物,(E)-烯醇盐形成anti产物作为主要的非对映体。 反应的立体化学结果可以通过Zimmerman-Traxler模型来解释,根据该模型,反应通过六元环椅式过渡态进行。 根据该模型,控制因素是避免在环状过渡态中发生不稳定的1,3-轴向相互作用。
合成应用
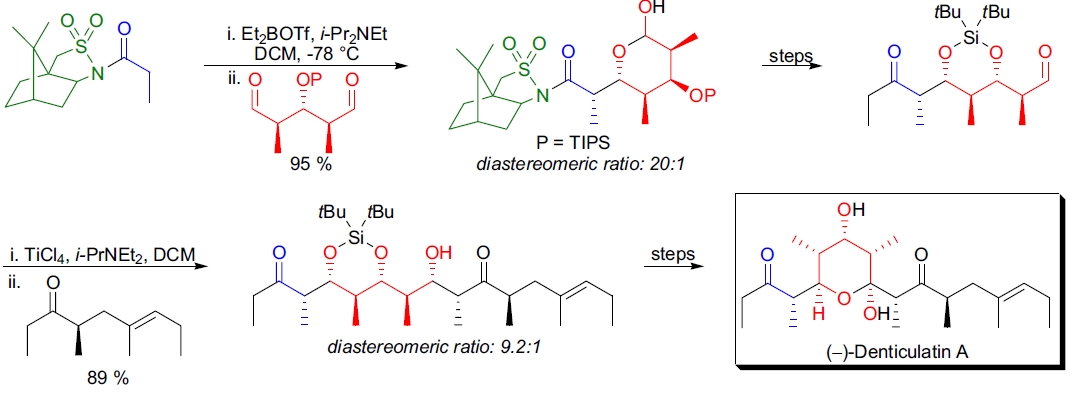
W. Oppolzer完成了(–)-denticulatin A的首次对映选择性全合成。关键步骤基于通过羟醛缩合反应对一个meso二醛中的对映异构基团的区分。 在羟醛缩合反应中,他们使用了生物碱基手性辅助试剂。 N-丙酰左旋樟脑磺内酰胺的烯醇化提供了(Z)-硼烯醇盐衍生物,该衍生物与内消旋化的二醛发生羟醛缩合反应,得到具有高产率和对映纯度的产物。 在合成的最后阶段,他们利用了第二次双非对映区分羟醛缩合反应。(Z)-钛烯醇盐的羟醛缩合反应给出了anti-Felkin syn产物。 反应的立体化学结果由醛组分中的α-手性中心决定。
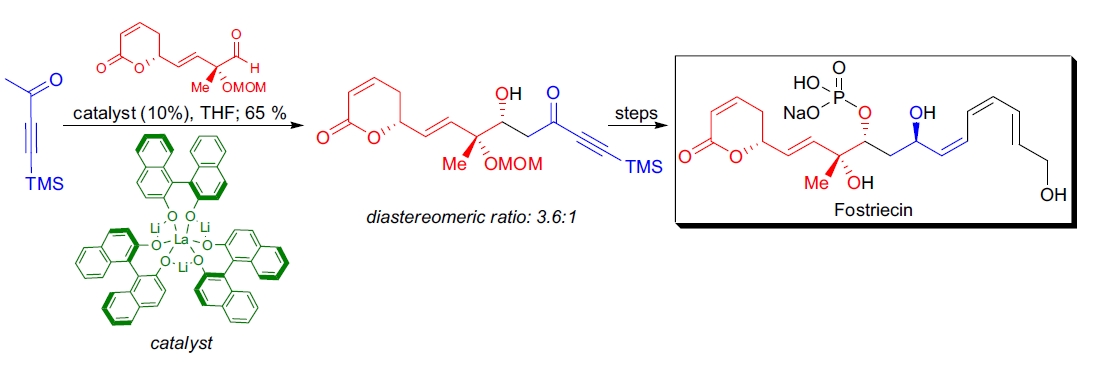
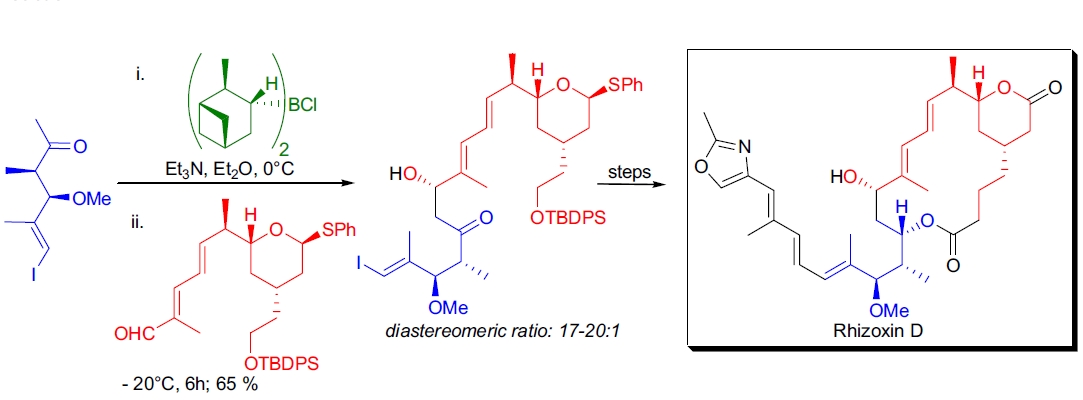
在J.D. White等人完成的rhizoxin D的全合成过程中,利用了不对称羟醛缩合反应来实现两个关键片段的耦合。 醛和从(+)-氯代异品樟脑硼烷衍生的手性烯醇盐的羟醛缩合反应在C13立体中心处以17-20:1的非对映体比例得到产物。 在他们的研究中,White和合作者还表明,手性硼取代基的立体诱导与烯醇盐中的立体中心相互增强,因而代表了“匹配”的羟醛缩合反应。 在羟醛缩合反应中引入对映选择性的一个可能方法是使用手性催化剂。
M. Shibasaki及其合作者开发了一种双功能催化剂(S)-LLB(L=镧;LB=双萘酚氧锂),该催化剂成功地应用于直接催化不对称羟醛缩合反应。 通过加入水和KOH从(S)-LLB衍生的改进版催化剂被用于fostriecin的正式全合成。