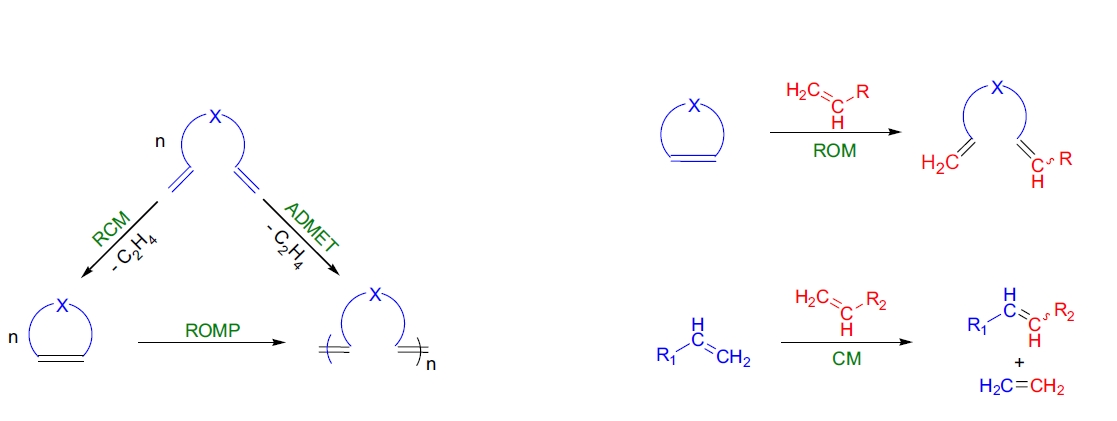
烯烃复分解
Alkene metathesis
重要性:
[开创性文献1,2;综述3-61;改进与优化62-70;理论研究71-76]
金属催化的碳碳双键重排称为烯烃(烯烃)复分解反应。首次关于双键重排的报道发表于1955年1,但“烯烃复分解”一词直到十三年后由N. Calderon2和同事引入。烯烃复分解反应包括多种类型:开环复分解聚合(ROMP)、闭环复分解(RCM)、无环二烯复分解聚合(ADMET)、开环复分解(ROM)和交叉复分解(CM或XMET)。这些不同的烯烃复分解反应可以得到通过其他方式难以获得的分子和聚合物。ROMP可以制备功能化聚合物,而RCM的应用使得中等和大型碳环以及杂环化合物的合成变得容易。 烯烃复分解用于复杂有机分子的合成直到1990年代初期才出现,因为当时可用的催化剂性能较低且对官能团的耐受性差。在过去10年中,烯烃复分解已成为一种可靠且广泛使用的合成方法。目前使用的L(L')X2Ru=CHR催化体系活性很高,且对大多数应用具有足够的官能团耐受性。然而,仍需要新的催化剂,因为现有的催化剂在某些苛刻的转化中表现不佳。目前仍存在的一些问题包括:1)与碱性官能团(如腈和胺)不相容;2)交叉复分解形成四取代烯烃;3)在CM和大环RCM反应中立体选择性低。
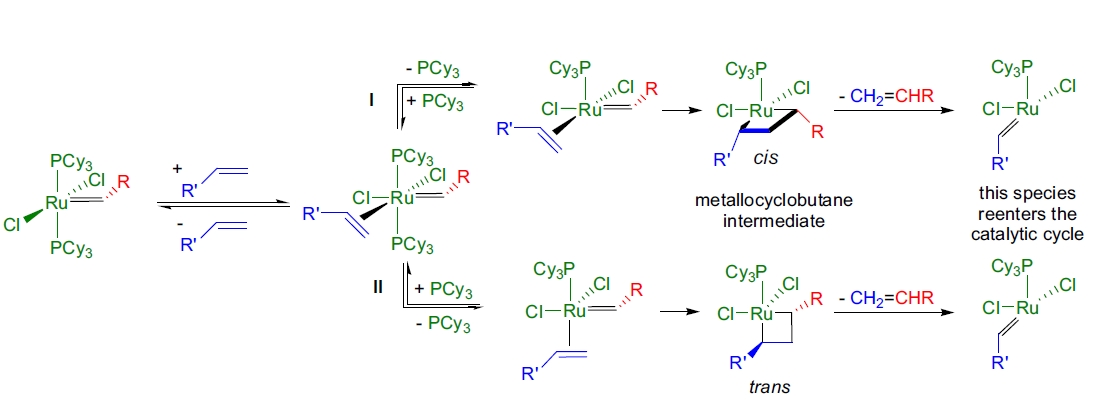
机理77-86
L2X2Ru=CHR卡宾配合物的晶体结构表明它们具有扭曲的四方锥几何结构,其中烷基烯位于轴向位置,而反式磷和卤素位于赤道平面87,88。R.H. Grubbs和合作者对L2X2Ru=CHR配合物进行了广泛的动力学研究,并提出了一种与观察到的活性趋势一致的机理89。有两种可能的机理路径(I和II)。
合成应用
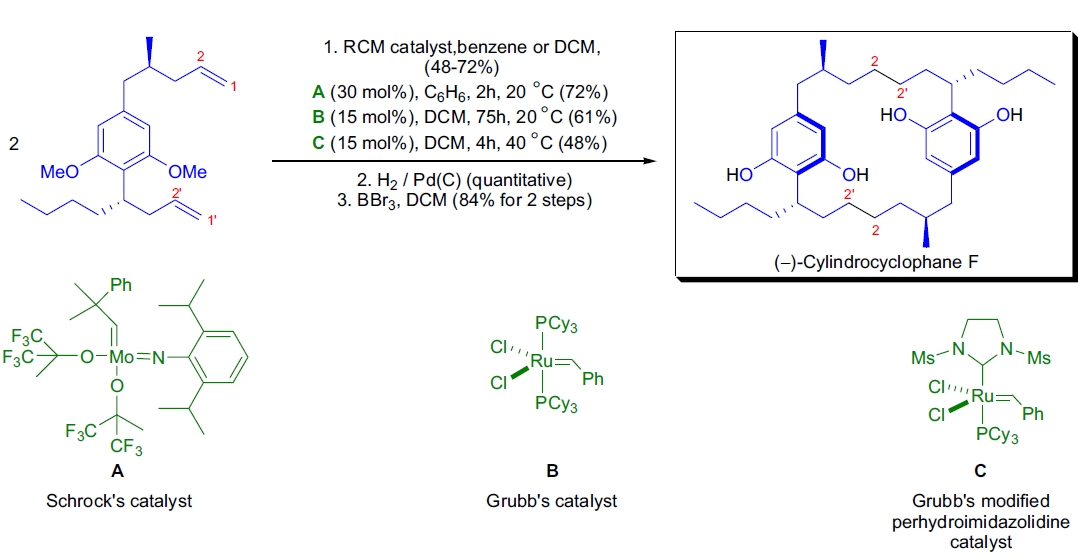
A.B. Smith和同事设计了一种有效的策略用于合成cylindrocyclophane类天然产物90,91。使用烯烃闭环复分解组装[7,7]-对环芳烃骨架。在他们的研究中,他们发现了一种非常有效的CM二聚过程,最终成功全合成了(–)-cylindrocyclophane
A和(–)-cylindrocyclophane F。他们确定交叉复分解二聚过程选择性地生成了一组结构相关异构体中热力学上最稳定的成员。在三种常用的RCM催化剂中,Schrock催化剂在此转化中表现最佳。
链霉菌属的多种土壤生物中分离出链阳性抗生素,这些抗生素对耐万古霉素的细菌具有活性。
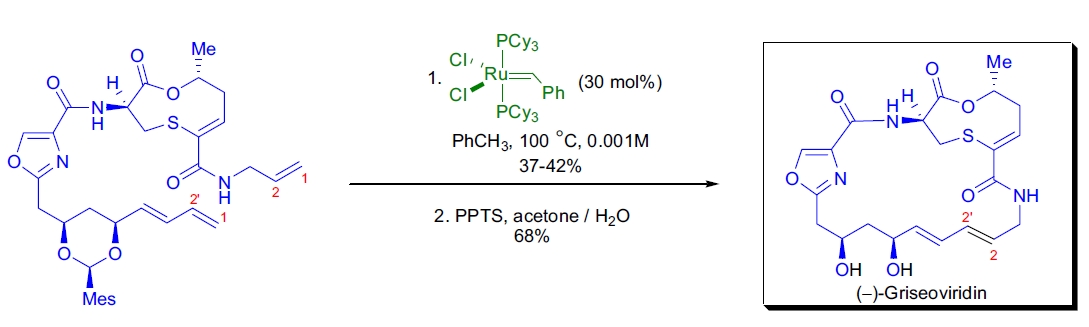
 在A.I.Meyers实验室,首次完成了链阳性抗生素(–)-griseoviridin及其C8对映体的全合成,其特征是一个23元不饱和环,使用了一种新颖的RCM,其中包括高非对映选择性的三烯到二烯大环环形成
92。该复分解在37-42%产率下进行,使用了30
mol%的Grubbs催化剂。天然产物作为单一非对映体获得;在闭环步骤中未形成其他烯烃异构体。
在A.I.Meyers实验室,首次完成了链阳性抗生素(–)-griseoviridin及其C8对映体的全合成,其特征是一个23元不饱和环,使用了一种新颖的RCM,其中包括高非对映选择性的三烯到二烯大环环形成
92。该复分解在37-42%产率下进行,使用了30
mol%的Grubbs催化剂。天然产物作为单一非对映体获得;在闭环步骤中未形成其他烯烃异构体。
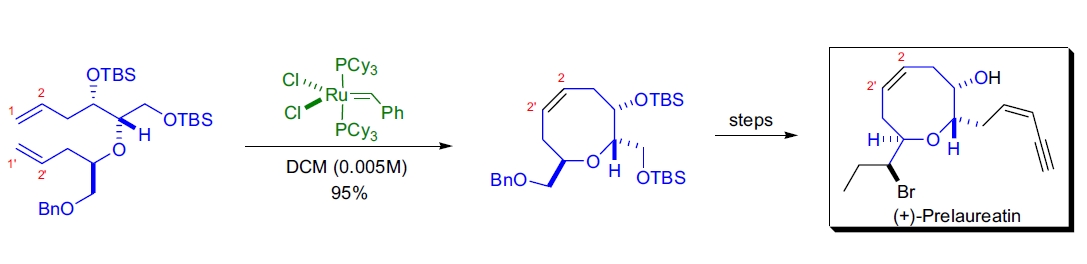
 (+)-prelaureatin的首次对映选择性全合成由M.T. Crimmins等人实现93。天然产物的氧杂环核心通过RCM反应在高产率下构建,使用了第一代Grubbs催化剂。
(+)-prelaureatin的首次对映选择性全合成由M.T. Crimmins等人实现93。天然产物的氧杂环核心通过RCM反应在高产率下构建,使用了第一代Grubbs催化剂。