炔烃复分解
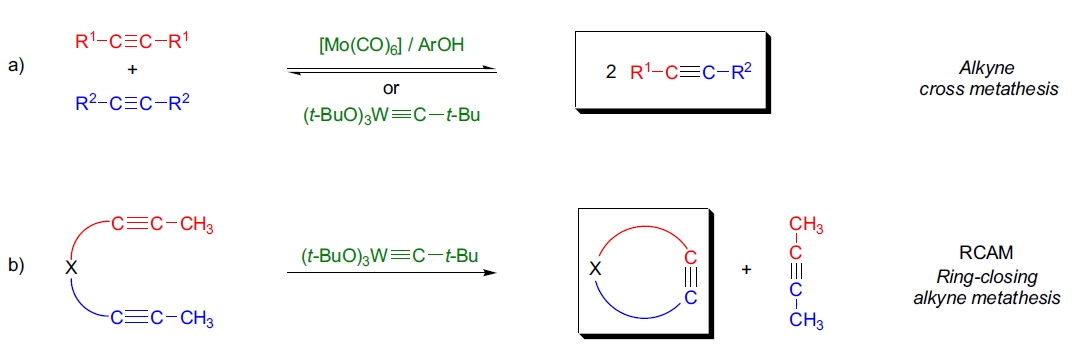
Alkyne metathesis
重要性:
[开创性文献1-3;综述4-11]
金属催化的碳碳三键重排称为炔烃复分解反应。在1970年代初期,A.
Mortreux及其同事首次实现了均相催化的碳碳三键复分解反应,他们在110°C条件下使用原位形成的[Mo(CO)6]/间苯二酚催化剂将对甲苯基苯乙炔不成比例地转化为二苯乙炔(tolan)1。然而,使用这种催化剂时,所有转化端炔的尝试均失败,而是分离出了环三聚体和复杂聚合物。十年后,在1980年代,Schrock钨炔配合物[(t-BuO)3W≡C-t-Bu]被证明可催化端炔的复分解,伴随乙炔气体的释放12。该反应同样受到底物聚合成聚乙炔的影响。在1990年代,寻找合适催化剂的研究逐渐加强。M.
Mori及其同事在Mortreux类型催化剂存在下成功进行了内炔的交叉复分解13,14,而在A.
Fürstner的实验室中,环炔复分解(RCAM)的条件得到了开发15。通过RCAM得到的环炔可以通过催化氢化16-18、硼氢化及随后的质子化以及其他方法立体选择性地转化为相应的(Z)-或(E)-烯烃19。在未来几年,炔烃复分解可能会成为有机合成和聚合物合成的有用工具。
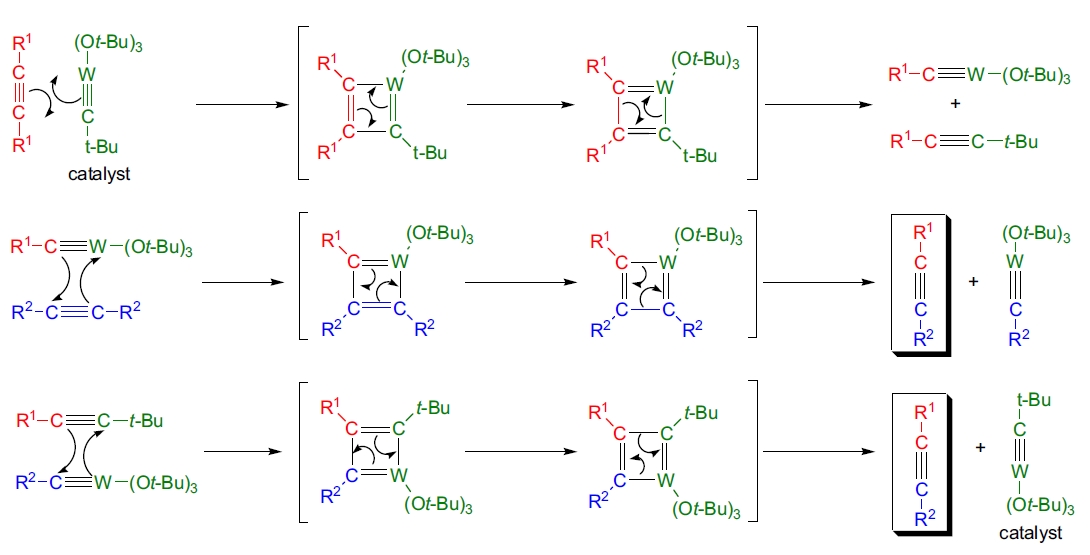
机理20-27
炔烃交叉复分解和复分解聚合可以通过热或光化学方法进行。热激活和光激活体系中催化活性物种的性质尚不清楚。下图所示的机理解释了炔烃交叉复分解产物的形成,但目前提出的机理均缺乏可靠的实验证据支持。
合成应用
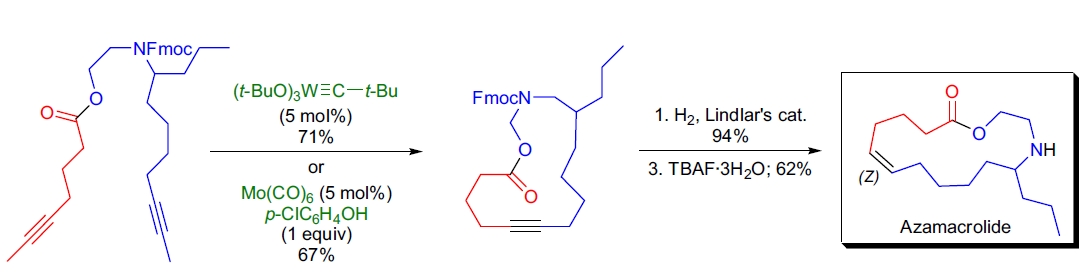
A. Fürstner在其实验室中进行了新近发现的氮杂大环内酯的全合成16。这些化合物是墨西哥甲虫Epilachna
varivestis的蛹的防御分泌物,它们是含有碱性氮原子的天然大环内酯的首例,这些氮原子位于系链中而不会环缩为相应的酰胺。通过RCAM和Lindlar还原提供了一种方便、高产率且立体选择性地引入(Z)-双键的方法。(使用Grubbs卡宾进行的通常的RCM方法仅得到了烯烃混合物(Z):(E)=1:2)。
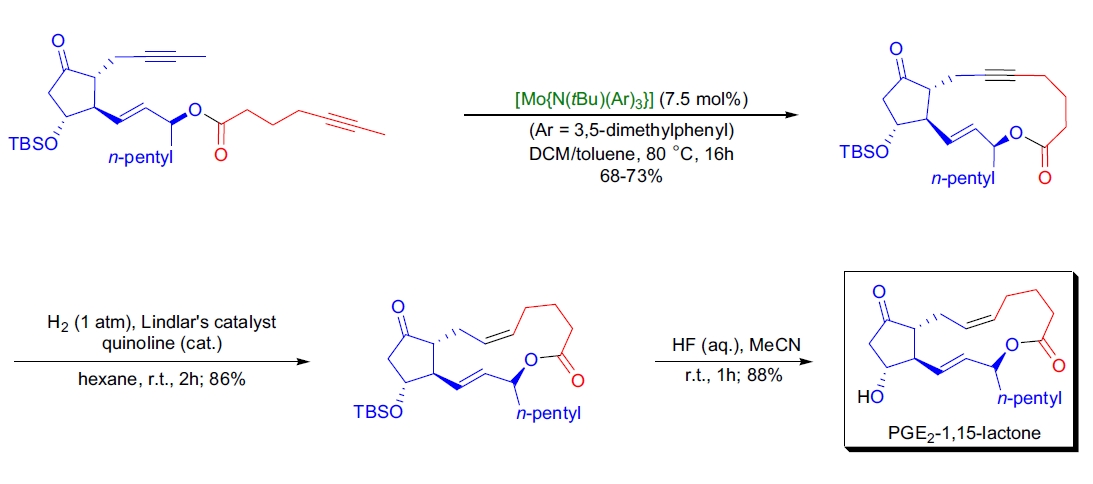
A. Fürstner及其同事还表明,RCAM确实是一种非常温和的方法,因为在他们对前列腺素E2-1,15-内酯的立体选择性全合成过程中,Mo[N-(t-Bu)(Ar)3]衍生催化剂耐受预先存在的双键和酮官能团17。对反应混合物的色谱检查表明,在环闭合之前或之后没有发生外消旋化,底物和产物的对映体过量几乎相同。
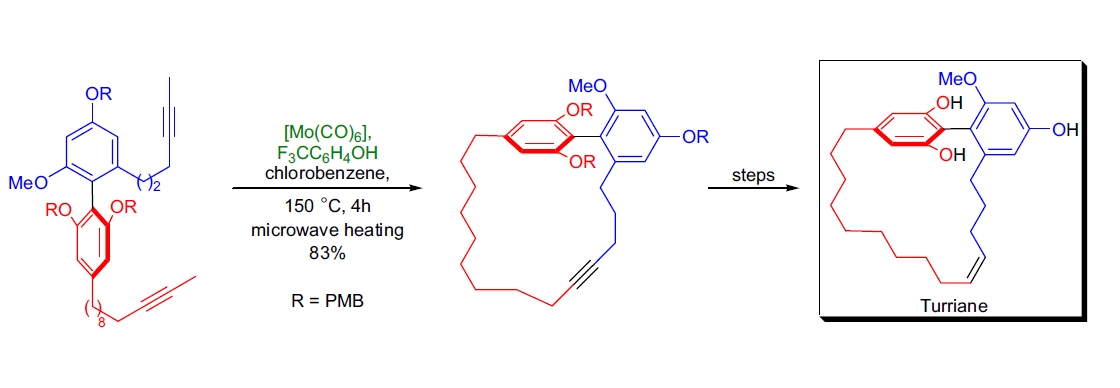
A. Fürstner等人还描述了三种天然存在的环芳烃衍生物(属于turriane类天然产物)的首次全合成28。这些天然产物具有空间阻碍的双芳基部分以及饱和和不饱和的大环系链。使用RCAM后续Lindlar还原这些环炔的立体选择性途径可以进入这一类化合物。