Arndt-Eistert 合成法
Arndt-Eistert 同系化
Arndt-Eistert synthesis
重要性
[开创性文献1;综述2-4;改进与优化5-10]
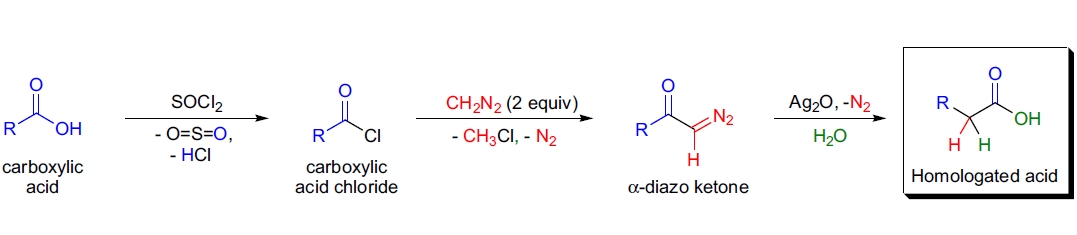
通过三个步骤将羧酸转化为其同系物(比原分子链长一个CH2单元)的过程被称为Arndt-Eistert合成。 这种同系化是延长羧酸碳链的最佳制备方法。
第一步是将酸转化为相应的酰氯。
第二步涉及生成α-重氮甲基酮,第三步通过Wolff重排完成。
第三步通常在固体氧化银/水或苯甲酸银/三乙胺溶液中进行。产率通常较高(50-80%)。如果在反应中存在醇(ROH)或胺(RNHR'),则生成相应的同系酯或酰胺。
其他金属(如Pt、Cu)也可催化重氮酮的分解。另一种方法是在含有亲核溶剂(如H2O、ROH或RNH2)的情况下加热或光解重氮酮,此时无需催化剂。 该反应能够容忍多种非酸性官能团(如烷基、芳基、双键)。但酸性官能团会与重氮甲烷或重氮酮发生反应。
机理2,11,4
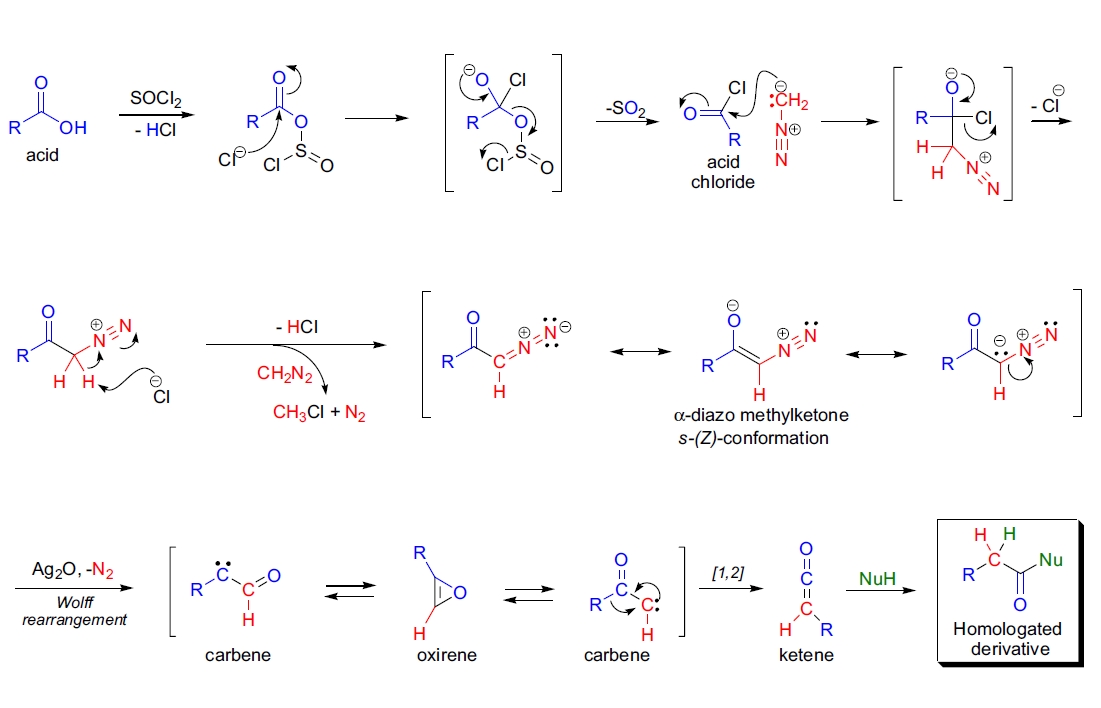
由于酰氯与重氮甲烷的反应会产生氯化氢(HCl)作为副产物,为避免副产物(如氯代酮)的生成,需要两当量的重氮甲烷。HCl会与第二当量的重氮甲烷反应,生成氯甲烷和氮气。
催化剂的作用尚不完全明确。重氮酮可以存在于两种构象中,即s-(E)和s-(Z)构象,由C-C单键的旋转产生。据研究,Wolff重排优先从s-(Z)构象开始。
随着一分子氮气的丢失,重氮酮的分解包括形成卡宾,然后卡宾经过卡宾重排生成氧杂环丙烷中间体。卡宾快速发生[1,2]-迁移生成酮烯,酮烯与亲核溶剂反应生成同系酸衍生物。
合成应用
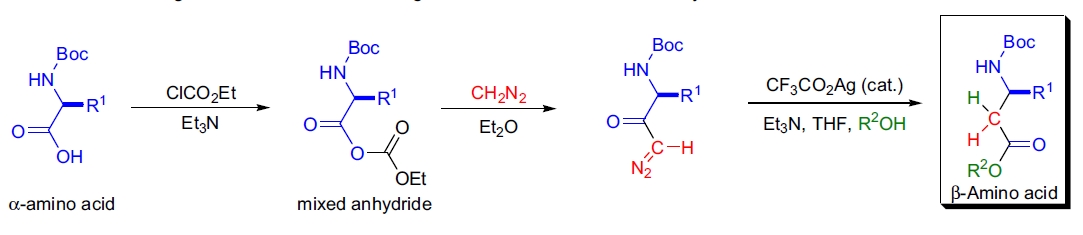
与α-肽相比,β-氨基酸的低聚物表现出在溶液和固态中折叠成良好定义的二级结构的显著能力。 在D. Seebach实验室,β-氨基酸的构建模块通过Arndt-Eistert同系化反应从α-氨基酸合成而来12。
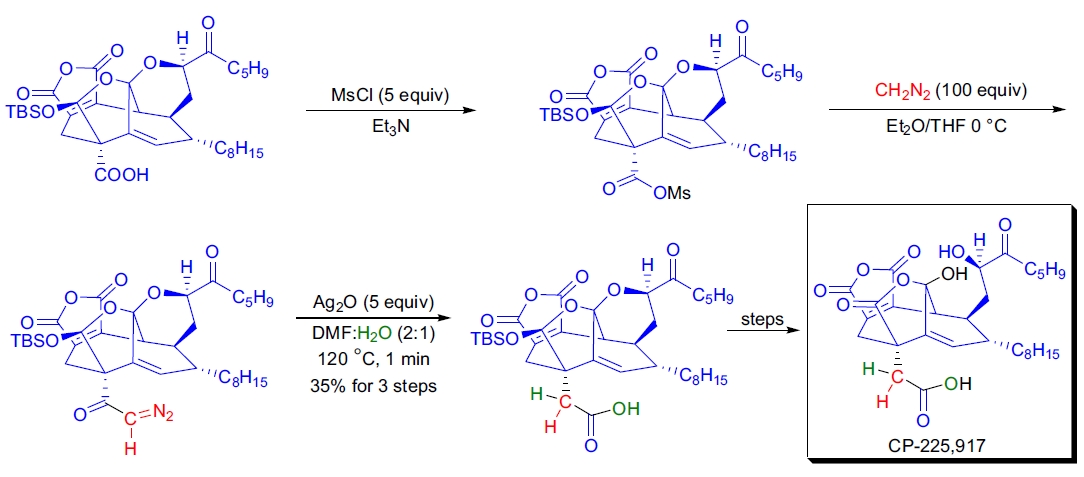
在CP分子全合成过程中,K.C. Nicolaou等人将一个具有位阻的羧酸同系化,这是一个高级中间体的一部分13。 由于该中间体的敏感性,重氮酮是通过酰基甲磺酸酯而非酰氯制备的。然后将重氮酮立即溶解在DMF:H2O(2:1)中,并在过量Ag2O存在下加热至120°C,仅需1分钟即可生成35%收率的同系酸。
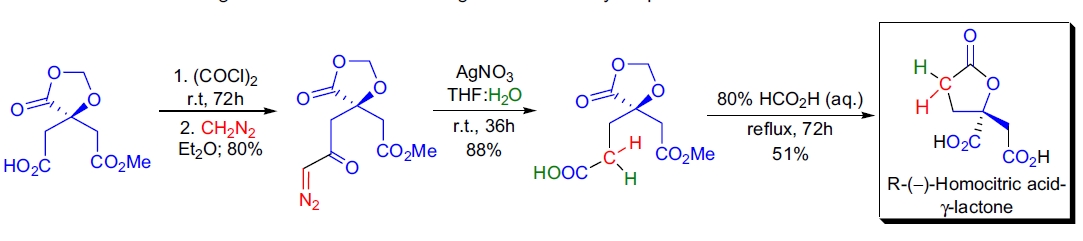
A.T. Russell及其同事从柠檬酸衍生物出发,使用Arndt-Eistert同系化为关键步骤,成功合成了(R)-(-)-同柠檬酸-γ-内酯,达到了克级规模14。
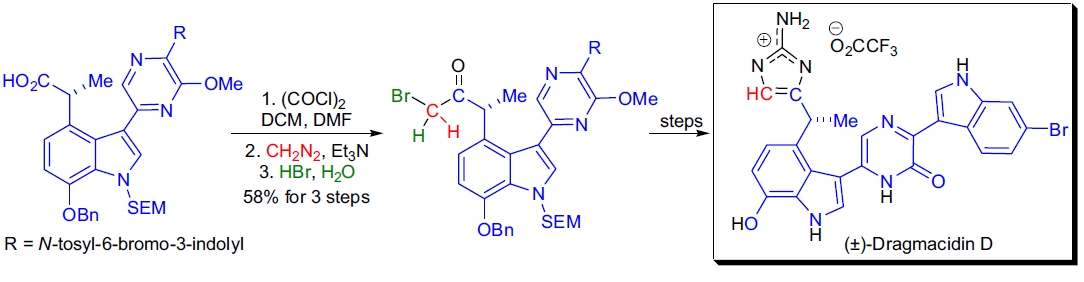
在B.M. Stolz实验室,首次实现了双吲哚生物碱(±)-dragmacidin D的全合成15。 在最终阶段,通过用氢溴酸处理重氮酮中间体,将羧酸同系化为相应的α-溴代酮。