aza-[2,3]-Wittig rearrangement
重要性
[开创性文献1,2;综述3;改进与优化4-14;理论研究9,15]
![aza-[2,3]-Wittig rearrangement overview](../../figure/name-reaction/aza_23_wittig_001.png)
α-金属化醚高立体选择性重排为金属烷氧化物的反应称为Wittig重排,由G. Wittig和L. Löhmann于1942年首次报道16。
该反应的产物在水解后为仲醇或叔醇。 该反应的氮类似物是电子等排的aza-Wittig重排,涉及α-金属化叔胺重排为骨架重排的金属酰胺,经过后处理得到相应的同烯丙基仲胺。 研究表明,aza-[2,3]-Wittig重排与氧系列反应一样,通过锂负载碳的构型反转发生17。 aza-Wittig重排不应与Stevens或Sommelet-Hauser重排混淆,后两者都需要季铵盐作为起始材料。 Stevens和Sommelet-Hauser重排可能导致副产物,如季铵盐在强碱处理下,通过邻位烷基迁移生成重排叔胺。 在苄基三烷基铵盐的情况下,Sommelet-Hauser重排在低温下竞争,生成邻位取代的苄基二烷基胺,经过[2,3]-σ迁移重排生成产物3。总体而言,由于缺乏热力学驱动力,α-金属化胺的aza-[2,3]-Wittig重排比α-金属化醚慢得多且选择性较低。 当由于环应变的缓解加快反应速率时,例外也有报道。
机理18-22,9
aza-[2,3]-Wittig重排通过协同过程发生,经过一个含六电子、五元环的信封状过渡态。 根据Woodward-Hoffmann规则,[2,3]-σ迁移重排是热允许的协同重排,以对两个片段超面的方式进行。 因此,aza-[2,3]-Wittig重排是一步SNi反应,通过超面烯丙反转实现区域专一性碳-碳键形成,其中杂原子功能从烯丙位转位到同烯丙位. 这些重排的驱动力是形式负电荷从较低电负性的α-碳转移到较高电负性的杂原子。
![aza-[2,3]-Wittig rearrangement mechanism](../../figure/name-reaction/aza_23_wittig_002.png)
合成应用
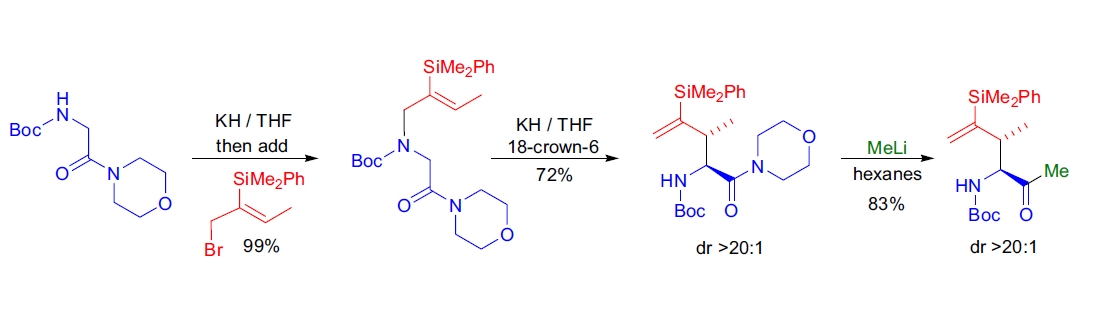
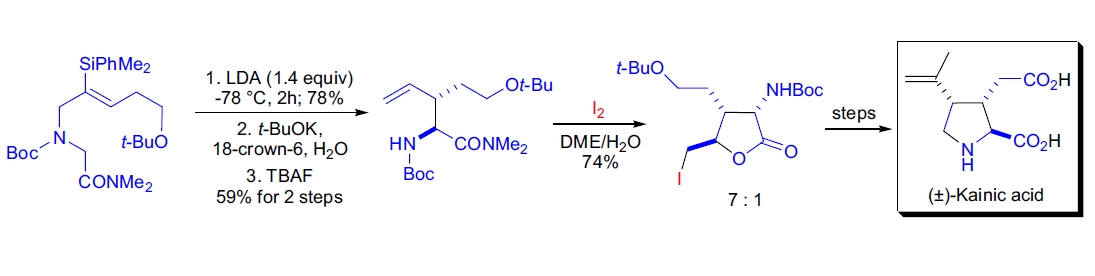
J.C. Anderson实验室利用aza-[2,3]-Wittig重排作为关键步骤完成了(±)-海人酸的全合成,建立了C2和C3之间的正确相对立体化学23。
C4立体中心通过碘内酯化反应建立。
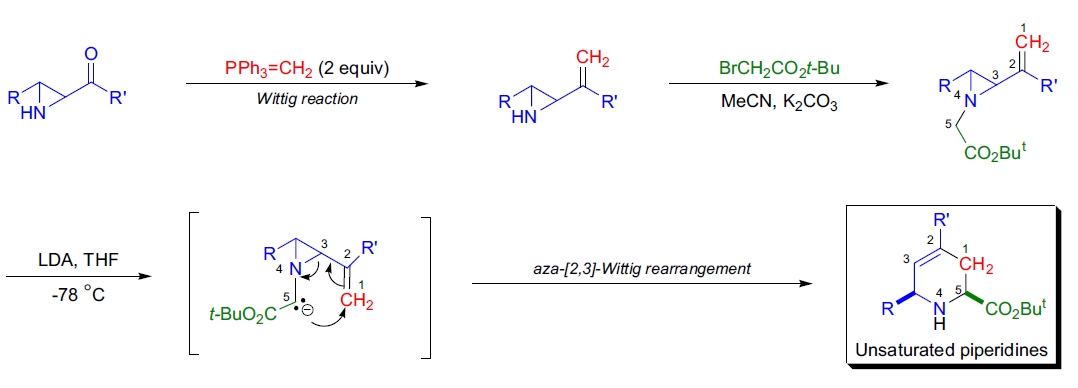
适当取代的乙烯基氮杂环丙烷的aza-Wittig重排导致了四氢吡啶的立体选择性生成,这是哌啶合成中的关键中间体。
I. Coldham等人报道了2-酮氮杂环丙烷利用aza-[2,3]-Wittig重排的一锅两步法合成不饱和哌啶24。 2-酮氮杂环丙烷与两当量膦叶立德反应生成乙烯基氮杂环丙烷,该化合物通过[2,3]-σ迁移重排伴随氮杂环丙烷开环生成不饱和哌啶。