aza-Cope rearrangement
重要性
[开创性文献1-3;综述4-6;改进与优化7-28;理论研究18,21,29]
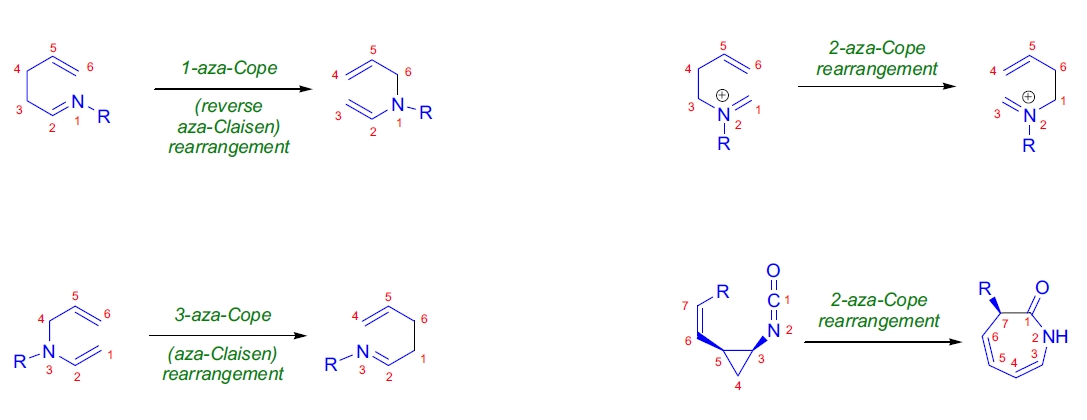
当1,5-二烯加热时,它们通过[3,3]-σ迁移重排异构化为Cope重排。N-取代的1,5-二烯的重排称为aza-Cope重排。
该反应有多种变体,即1-aza-、2-aza-、3-aza-以及1,3-、2,3-、2,5-、3,4-二氮Cope重排7,8。
3-aza-Cope重排也称为aza-Claisen重排。顺式-2-乙烯基环丙基异氰酸酯重排为1-氮杂环庚-4,6-二烯-2-酮(2-aza-二乙烯基环丙烷重排)与高度立体专一的顺式二乙烯基环丙烷重排类似。
氧原子在π键附近的存在已被证明会加速Cope重排。如果在C3或C4上有基团能与新形成的双键共轭,反应温度低于未取代的情况。
与所有[3,3]-σ迁移重排一样,当起始二烯带电时,活化能显著降低。
机理
aza-Cope重排是一个协同过程,通常通过类似椅式过渡态进行,其中取代基排列在准赤道位置。
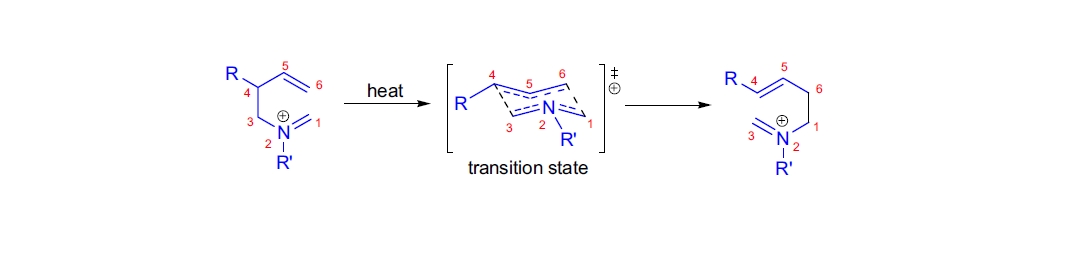
请参见Cope重排以了解更多细节。
合成应用
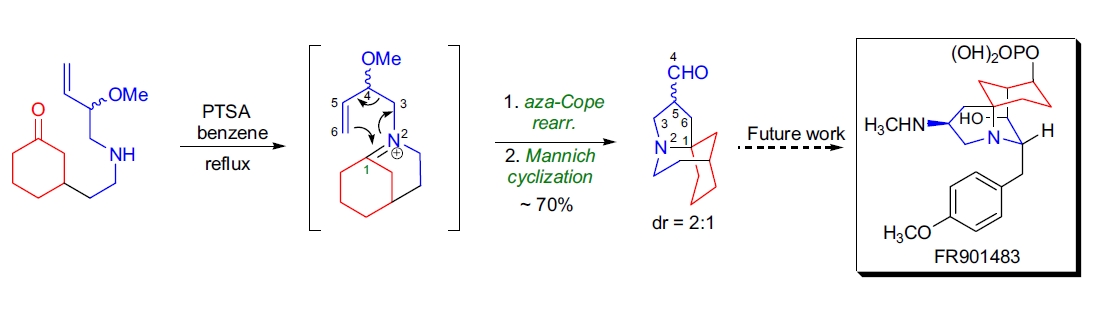
K. Brummond实验室利用串联阳离子aza-Cope重排和Mannich环化合成了强效免疫抑制剂FR901483的新型三环核心结构39。
该方法是首次通过桥头亚胺阳离子实现该串联反应的合成实例。
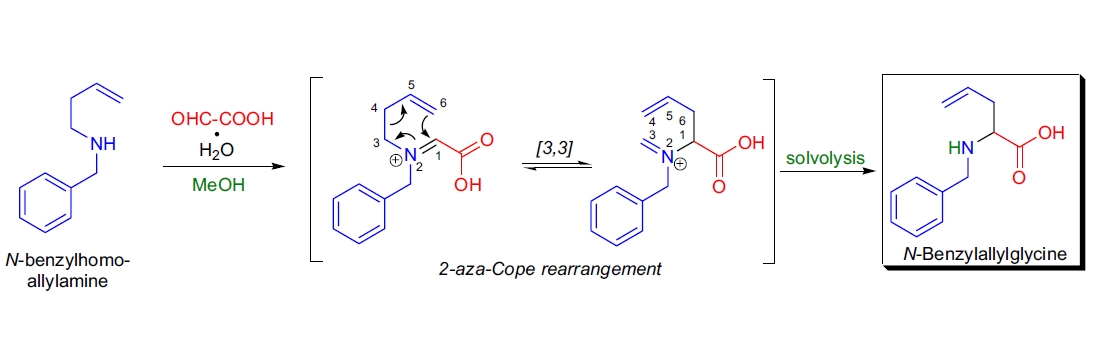
D.J. Bennett等人基于串联2-aza-Cope/亚胺离子溶解反应开发了一种简便的N-苄基烯丙基甘氨酸合成方法40。
N-苄基烯丙基甘氨酸可通过N-苄基高烯丙胺与水合乙醛酸在甲醇中的一锅反应以良好产率制备。
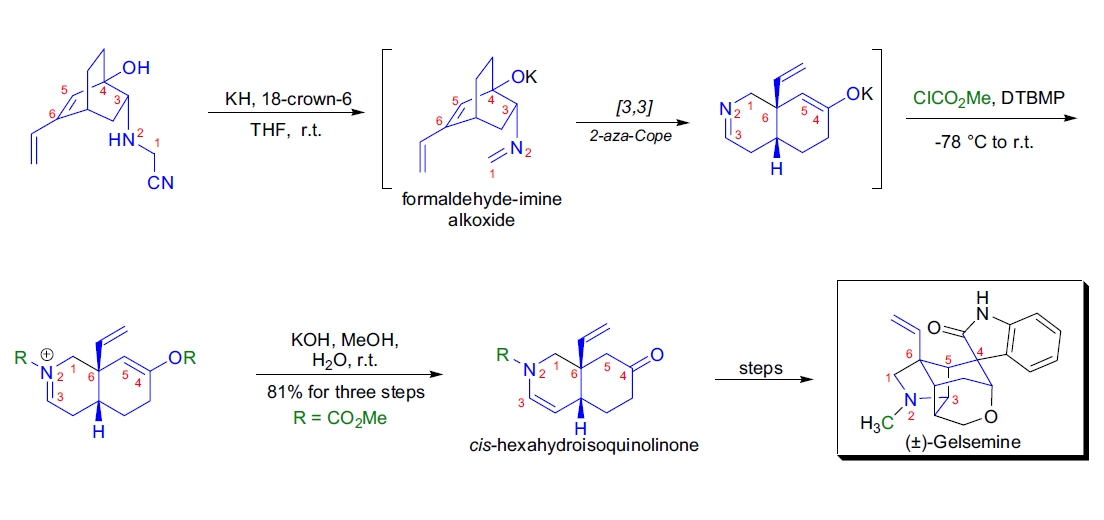
L.E. Overman及其团队通过一系列关键步骤完成了(±)-gelsemine的全合成,这些关键步骤包括串联阴离子2-aza-Cope重排和Mannich环化、分子内Heck反应以及复杂的碱促进分子重组以生成六环体系41。
将双环底物暴露于18-冠-6存在的氢化钾中,引发双环甲醛-亚胺醇盐的阴离子aza-Cope重排。重排产物与过量氯甲酸甲酯淬灭后,再用碱处理,得到所需的顺式六氢异喹啉酮。
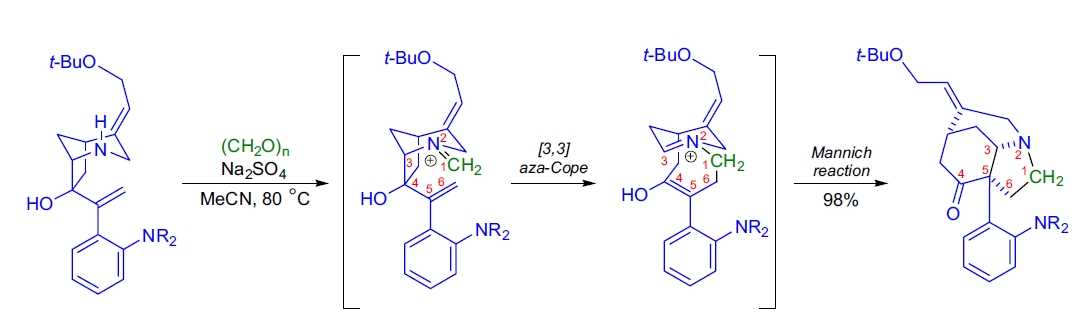
在对(–)-和(+)-士的宁及Wieland-Gumlich醛的对映选择性全合成中,L.E. Overman及其团队将串联aza-Cope重排/Mannich反应用作关键步骤42。
该中心aza-Cope/Mannich重组步骤的产率为98%。