Baylis-Hillman 反应
重要性
[开创性文献1,2;综述3-13;改进与优化14-31]
1968 年,K. Morita 报道了乙醛与丙烯酸乙酯在叔膦催化下生成 α-羟基乙基化产物的反应。1 四年后,A.B. Baylis 和 M.E.D. Hillman 使用更廉价且毒性更低的 DABCO 作为催化剂,完成了相同的转化。2 Baylis-Hillman 反应通过在三级胺类催化剂存在下,使共轭羰基化合物(如酯和酰胺)的 α-位与羰基亲电体(如醛和活化酮)形成 C-C 单键。常用催化剂包括 DABCO、奎尼啶、金鸡纳生物碱衍生物和三烷基膦。羟基化手性胺催化的 Baylis-Hillman 反应对脂肪族和芳香族醛均有效,并具有高对映选择性。该反应的主要局限在于反应速率缓慢(需数日或数周)以及底物范围有限,但可以通过使用 Lewis 酸部分克服这些问题。15,16
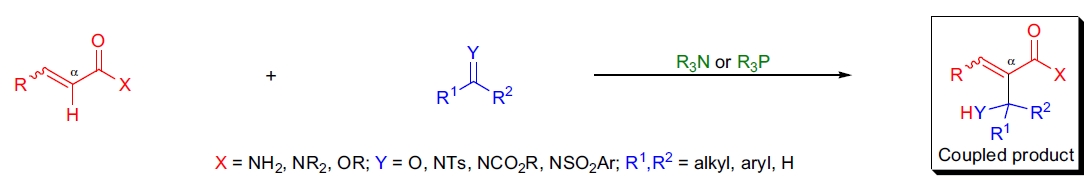
机理32-34,17,35-38
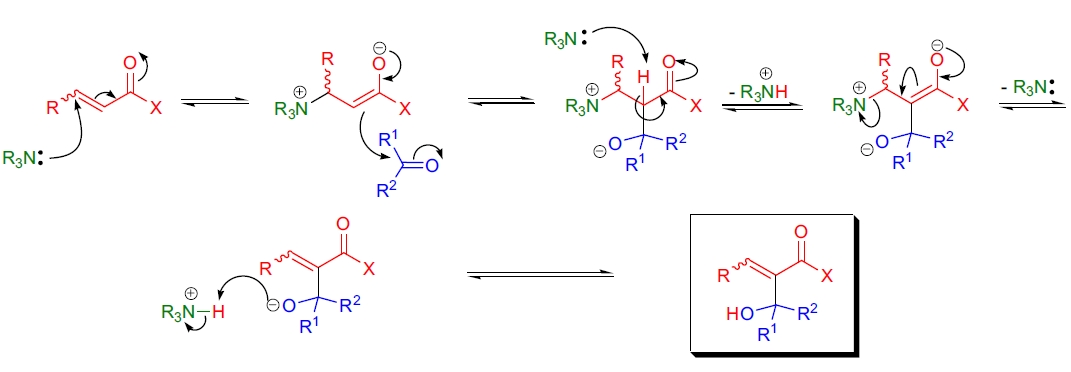
目前公认的 Baylis-Hillman 反应机理包括:催化剂(如三级胺)在活化烯烃的 β 位发生 Michael 加成,形成一个双离子烯醇负离子。此烯醇负离子与醛反应生成另一个双离子中间体,并在脱质子化后释放催化剂,最后通过质子转移生成目标产物。
合成应用
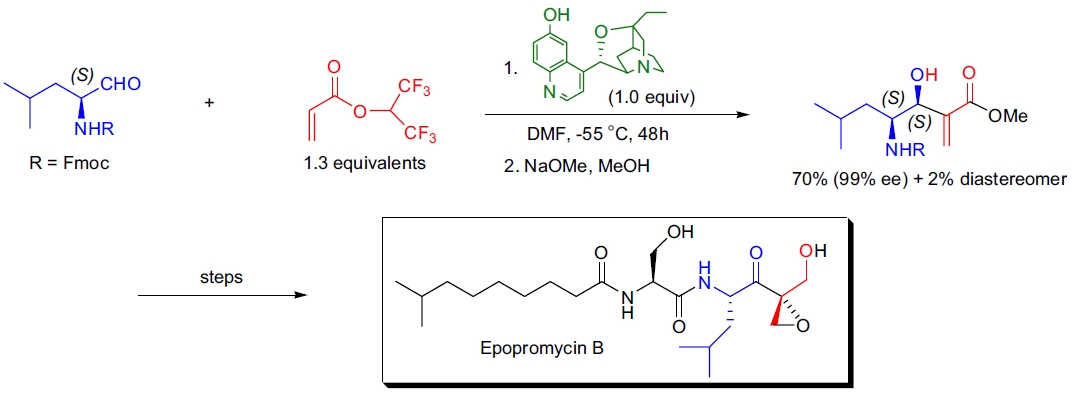
1. Epopromycin B 前体的合成: S. Hatekayama 等人通过金鸡纳生物碱催化的 Baylis-Hillman 反应,对 N-Fmoc 亮氨醛进行了高对映和立体选择性合成,成功制备了植物细胞抑制剂 Epopromycin B 的关键前体39。
2. 2H-色烯衍生物的制备: P.T. Kaye 等人研究了 2-羟基苯甲醛和 2-羟基-1-萘甲醛与活化烯烃的反应,在 Baylis-Hillman 条件下区域选择性地生成 3-取代 2H-色烯衍生物,并取得高产率40。
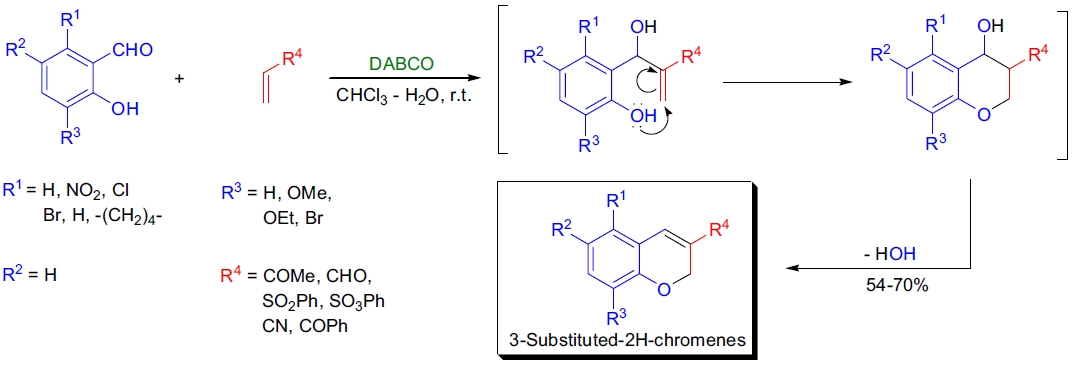
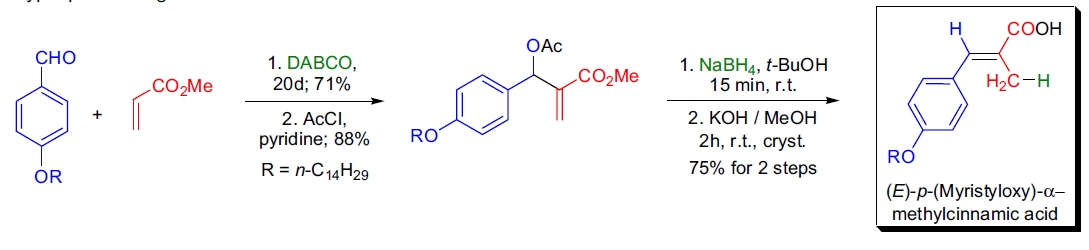
3. α-甲基肉桂酸的合成: D. Basavaiah 等开发了通过 Baylis-Hillman 加成产物的乙酸酯与硼氢化钠反应制备 α-甲基肉桂酸的简单方法,并进一步应用于活性降脂剂 p-(十四烷氧基)-α-甲基肉桂酸的合成41。
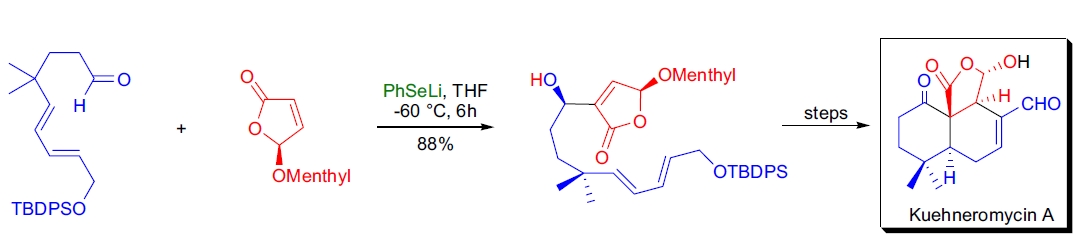
4. Kuehneromycin A 的全合成: J. Jauch 研究发现,对于高碱敏感底物,可以使用弱碱性但强亲核性的苯硒化锂来完成 Baylis-Hillman 反应,并成功实现了 Kuehneromycin A 的全合成42。
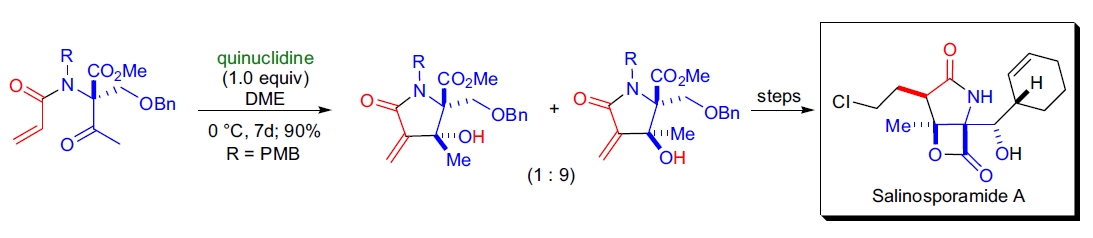
5. Salinosporamide A 的全合成: E.J. Corey 等人在 Salinosporamide A 的简单立体选择性全合成中,使用了 Baylis-Hillman 反应。该反应在奎尼啶催化下对酮酰胺底物进行环内反应,生成了 9:1 的 γ-内酰胺二异构体混合物,其中目标异构体占优43。