Beckmann 重排反应
重要性
[开创性文献1;综述2-5;改进与优化6-17;理论研究18-27]
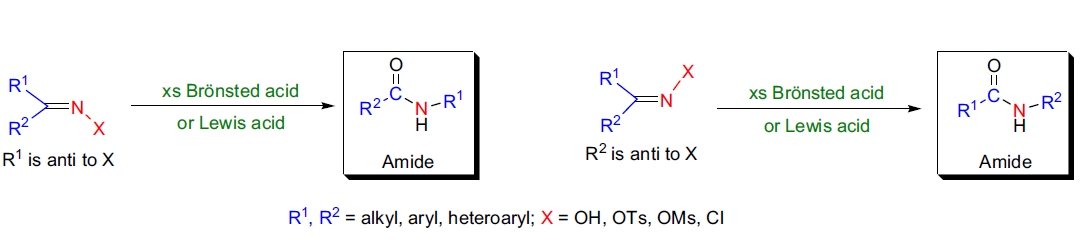
Beckmann 重排反应是在酸性介质中将醛肟和酮肟转化为相应酰胺的反应。该反应在工业中尤为重要,特别是在生产 ε-己内酰胺(合成纤维用的聚酰胺单体)中应用广泛。通常,该反应需要较高温度(>130 °C)和大量强酸(如 H2SO4 或 HCl/Ac2O/AcOH),因此不适用于敏感底物。该反应的立体化学结果是可预测的:与氮上离去基团反式的 R 基团会迁移,但氢原子不会迁移,因此此法不能用于合成 N-未取代酰胺。
机理28,19,22-24,29-31
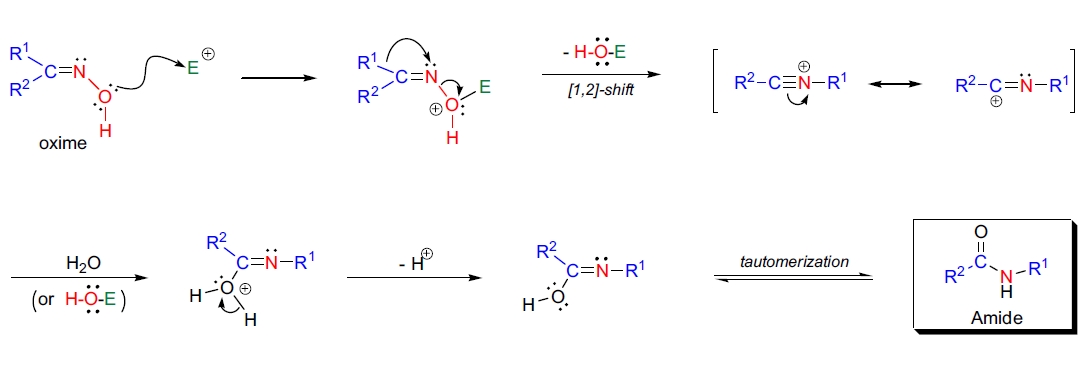
反应机理的第一步是 X 基团通过与亲电试剂反应被转化为离去基团。随后,离去基团的离去伴随着 R 基团的 [1,2]-迁移(迁移的 R 基团与离去基团反式)。生成的碳正离子与亲核试剂(如水分子或离去基团)反应,经互变异构生成最终的酰胺产物。
合成应用
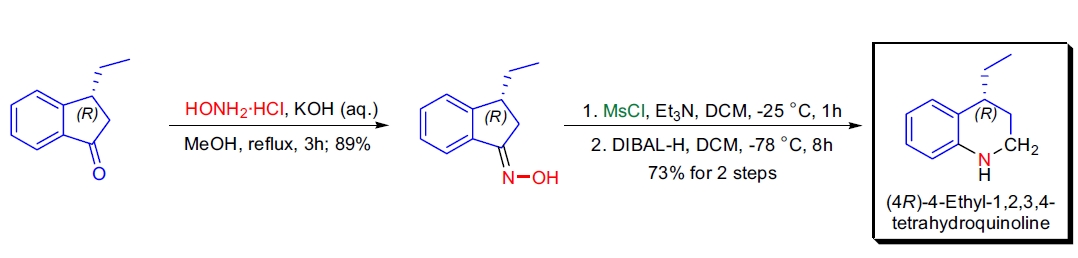
1. 手性 4-烷基-1,2,3,4-四氢喹啉的合成: N.S. Mani 等人在高效合成手性 4-烷基-1,2,3,4-四氢喹啉的路线中,使用了铝有机物促进的改良 Beckmann 重排反应。以 (3R)-3-乙基-1-茚酮的酮肟磺酸酯为起始物,生成了六元内酰胺产物,随后用二异丁基铝氢还原为相应的环状二级胺32。
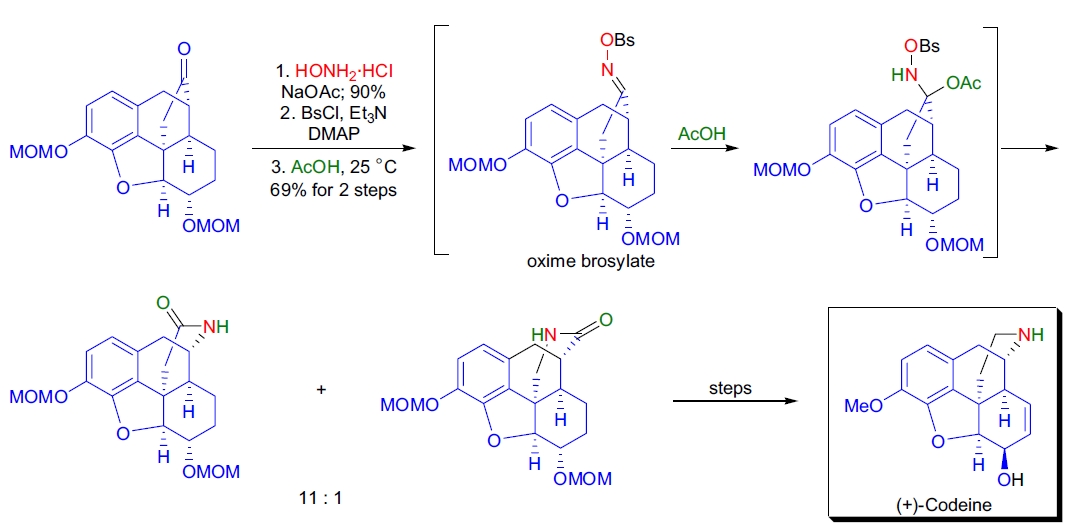
2. (+)-可待因的非天然全合成: 在 J.D. White 的实验室中,通过 Beckmann 重排反应成功将中间体环戊酮肟转化为六元哌啶结构的内酰胺,用于 (+)-可待因的非天然全合成。该反应通过乙酰酸中的溴磺酰基肟(Bs)顺利实现,得到 69% 收率的内酰胺混合物,目标异构体比例为 11:133。
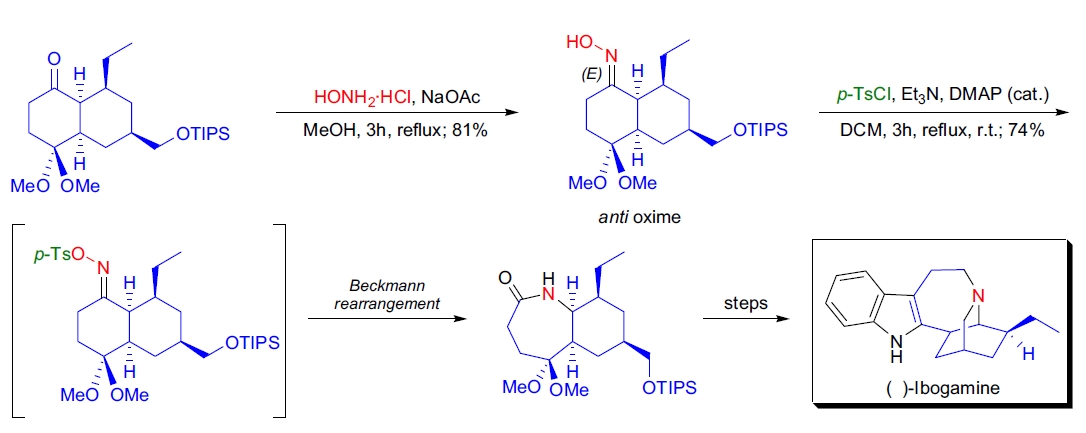
3. (-)-Ibogamine 的全合成: J.D. White 等利用催化不对称 Diels-Alder 反应合成 (-)-Ibogamine。分子中含氮三环骨架通过将双环酮转化为抗式肟,并在对甲苯磺酰氯存在下进行 Beckmann 重排生成七元内酰胺,再通过几步反应得到 Ibogamine 的天然产物34。
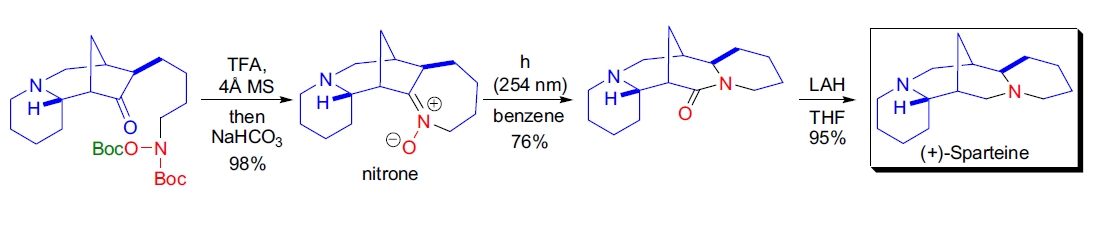
4. 光催化 Beckmann 重排: 在 (+)-Sparteine 的全合成终端步骤中,J. Aubé 等使用了一种新型光催化 Beckmann 重排变体。通过原位生成羟胺并与酮内酯化形成亚胺氧化物,光解后获得目标内酰胺,产率良好35。