Benzoin 缩合反应
重要性
[开创性文献1-3;综述4-8;改进与优化9-16;理论研究17,18]
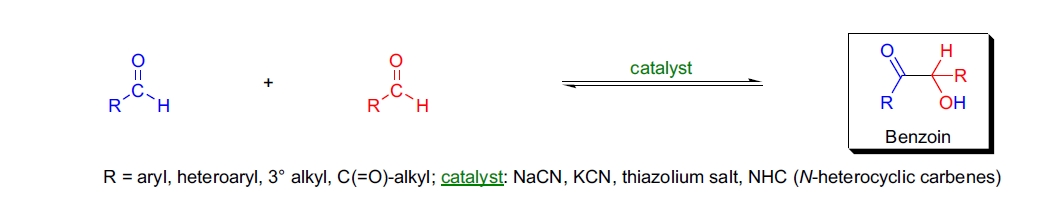
Benzoin 缩合反应是将某些芳香醛或乙醛酸(α-酮醛)与氰离子(CN⁻)反应生成 benzoin(α-羟基酮或酰醇)的一种反应。其逆过程称为逆 Benzoin 缩合反应,常用于制备酮类化合物。缩合反应中,一分子醛加到另一分子醛的 C=O 基团上,一个醛作为供体,另一个作为受体。某些醛只能作为供体(如对二甲氨基苯甲醛)或受体,不能自缩合,而其他醛(如苯甲醛)能同时充当供体和受体,可发生自缩合。噻唑盐在温和碱存在下也可催化该反应,这种方法比原始氰化物方法更具合成价值,因为它适用于含或不含烯醇化氢的醛,且可以使用手性催化剂。此外,混合脂肪族和芳香族醛可以生成混合 benzoin,手性噻唑盐还可用于立体选择性合成 benzoin。
机理20,21,17,22-24,18,25-30,19,31
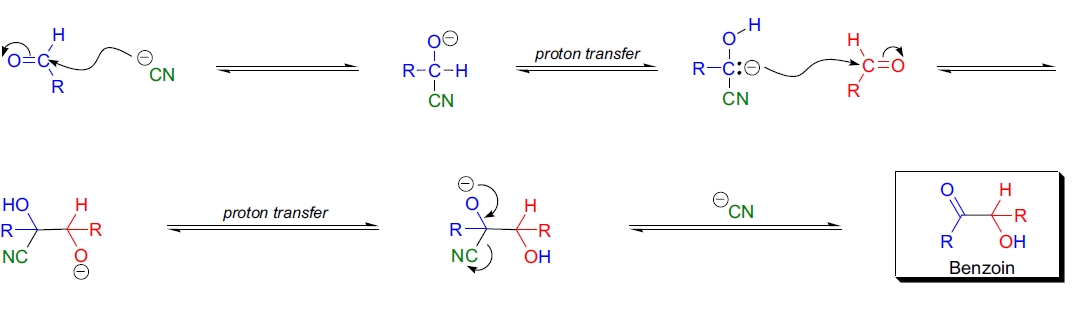
Benzoin 缩合反应中由氰离子催化的所有步骤都是可逆的。普遍接受的机理是关键步骤中醛质子丢失,这一去质子化过程是由于 CN 基团的吸电子效应增强了醛基 C-H 键的酸性。 氰离子是该反应的特定催化剂,既是优良的亲核试剂和离去基团,其吸电子效应还能增强醛质子的酸性。。
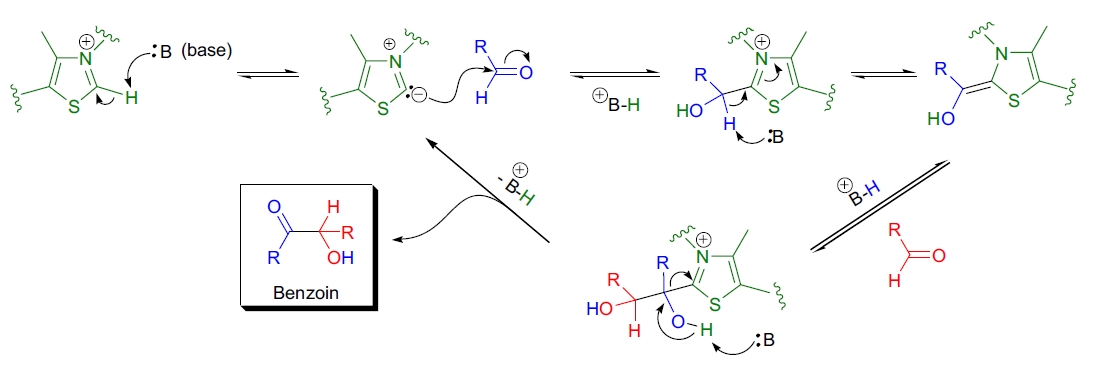
此外,噻唑盐催化的缩合反应机理最早由 R. Breslow 提出
合成应用
1. Ketone 的合成: A. Miyashita 等人基于 Benzoin 缩合反应的可逆性(逆 Benzoin 缩合反应)开发了一种新方法,生成最稳定的产物。通过将 α-苄基 benzoin 与 KCN 在 DMF 中反应,C-C 键裂解生成了脱氧 benzoin 和苯甲醛。该方法已成功应用于多种 α-取代 benzoin 的制备32。
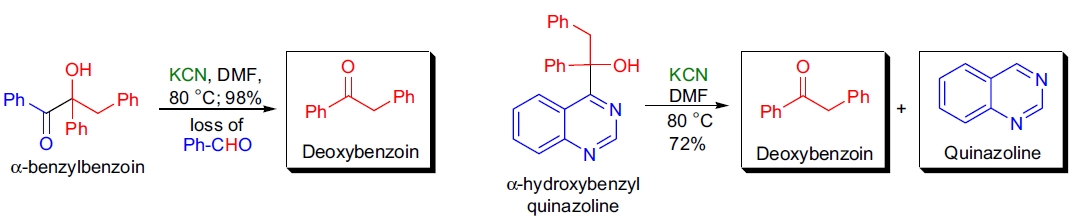
2. 2-取代喹唑啉的合成: 逆 Benzoin 缩合法被用于从 2,4-二氯喹唑啉合成 2-取代喹唑啉,最终产率较高。通过该方法,可以在含氮杂环的 α-位置引入芳酰基作为保护基,然后通过逆 Benzoin 缩合轻松去除33。
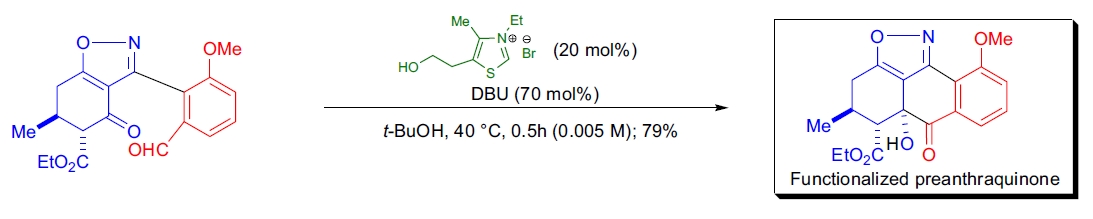
3. 前蒽醌的合成: 在 K. Suzuki 的实验室中,开发了交叉醛酮 Benzoin 缩合反应催化方法,并成功应用于立体化功能化前蒽醌的合成15。

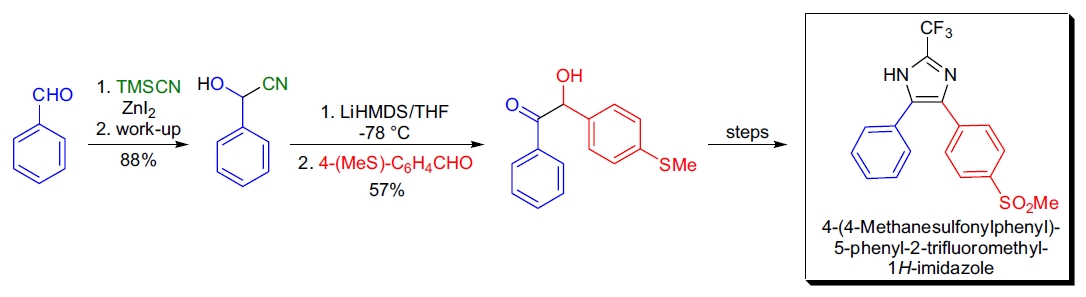
4. 抗炎化合物 4,5-二芳基咪唑的合成: 在 T.E. Barta 的研究中,Benzoin 缩合是关键的碳-碳键形成步骤。苯甲醛首先通过 TMSCN 转化为氰醇,随后去质子化后与 4-(甲硫基)-苯甲醛反应生成 benzoin34。