Bischler-Napieralski 合成
重要性
[开创性文献1;综述2-4;改进与优化5-15]
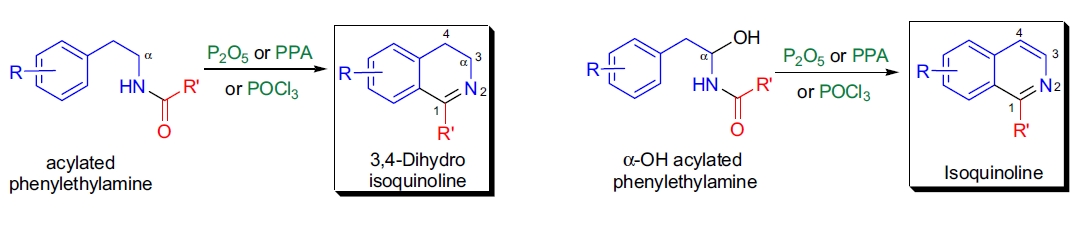
Bischler-Napieralski 合成是通过 Friedel-Crafts 酰基化路线合成异喹啉的一种方法。当苯乙胺的酰基衍生物与脱水剂(如 POCl3、P2O5、PPA、TFAA 或 Tf2O)反应时,会发生环脱水反应,生成 3,4-二氢异喹啉衍生物。如果起始化合物在 α-位含有羟基,还会发生额外脱水生成异喹啉。
机理16,5
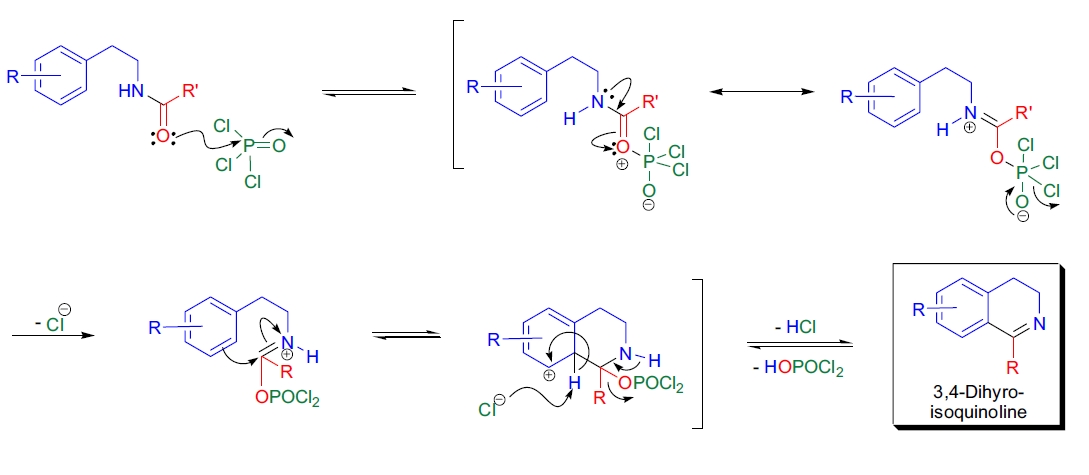
该反应的第一步是通过脱水剂活化酰基衍生物,促进内环化过程形成中间体。随后,分子内氮原子进攻形成环状化合物,最终经脱水步骤生成 3,4-二氢异喹啉或异喹啉衍生物。
合成应用
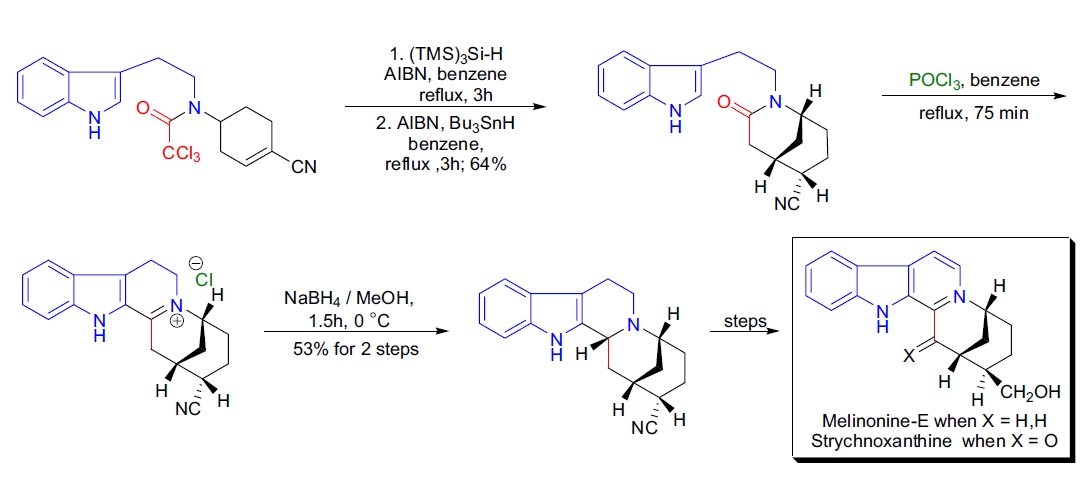
1. Strychnoxanthine 和 Melinonine-E 的全合成:在 J. Bonjoch 的实验室中,利用 α-羰酰二氯甲基自由基进行自由基碳环化反应,随后通过 Bischler-Napieralski 反应完成了五环生物碱(±)-strychnoxanthine 和(±)-melinonine-E 的首次全合成17。
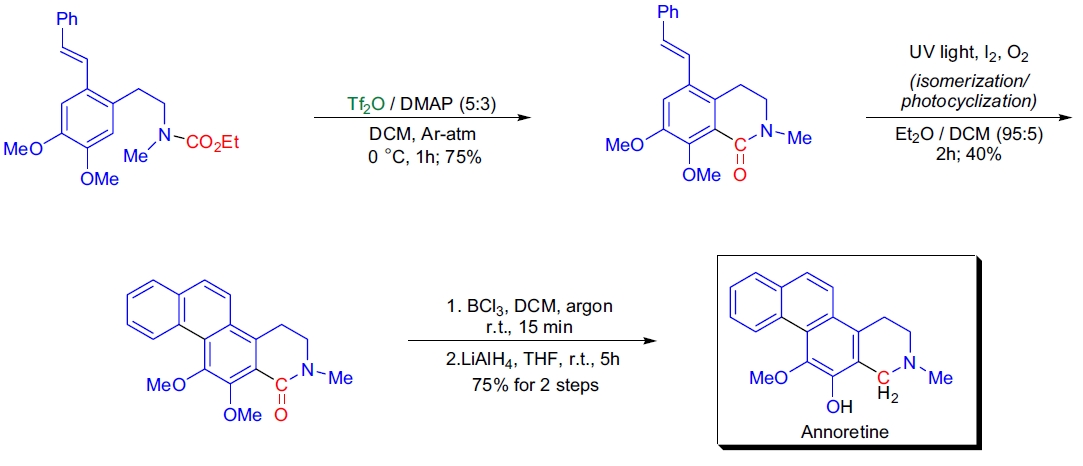
2. Annoretine 的全合成:J.C. Estevez 等人首次全合成了含 1,2,3,4-四氢萘并[2,1-f]异喹啉结构的生物碱 annoretine,其关键步骤包括 Bischler-Napieralski 反应形成 5-苯乙烯基异喹啉单元以及后续的光环化反应18。
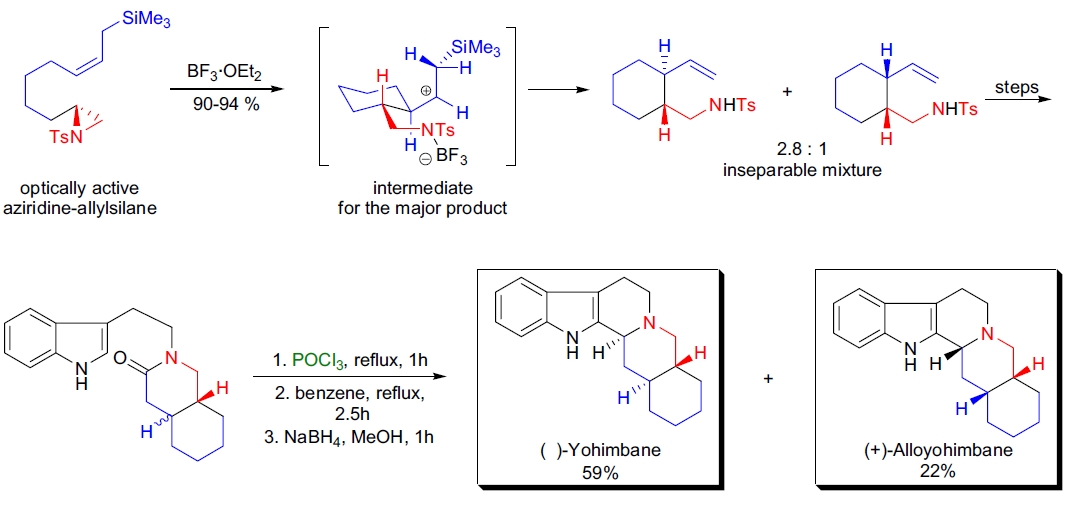
3. Rauwolfia 生物碱的合成:S.C. Bergmeier 等人通过一种新型的氮杂环丙烷-烯丙基硅烷环化方法和 Bischler-Napieralski 合成异喹啉的方法,成功完成了(–)-yohimbane 和(–)-alloyohimbane 的不对称全合成,这些生物碱具有降压和抗精神病等生物活性19。
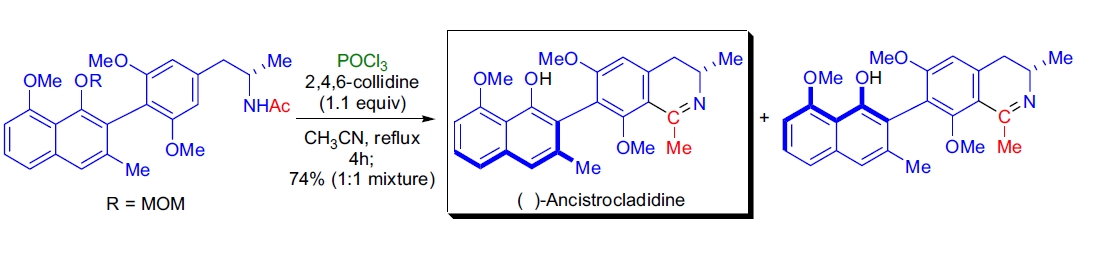
4. Ancistrocladidine 的全合成:J.C. Morris 等人首次实现了 7,3'-连接萘基异喹啉生物碱(–)-ancistrocladidine 的全合成。其关键步骤包括 Pinhey-Barton 邻位芳基化和 Bischler-Napieralski 环化反应。天然产物通过甲苯/石油醚重结晶从 1:1 的异构体混合物中分离20。