Brown硼氢化反应
Brown hydroboration reaction
重要性
[开创性文献1;综述2-21;改进与优化22-28;理论研究29-34]
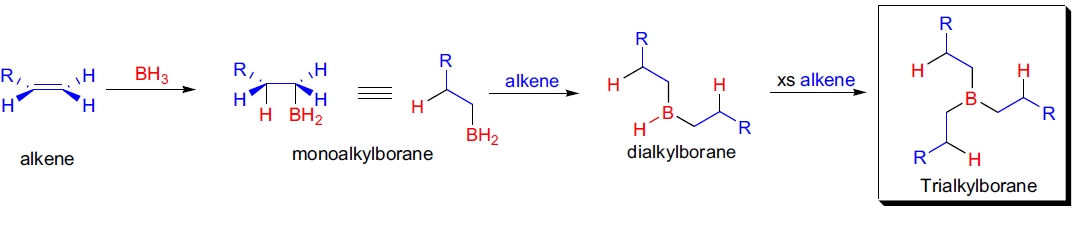
Brown 加成反应是指将 B-H 键加成到碳碳双键或三键上的过程,具有高度的区域选择性和立体专一性(syn 加成)。硼原子主要连接到烯烃的低取代碳原子上(反马氏规则产物)。生成的有机硼化物是非常有用的有机合成中间体,硼可被羟基、卤素或氨基取代(如加成/氧化、加成/氨化等)。当使用 BH3 作为加成试剂时,可与三分子烯烃反应生成三烷基硼(R3B)。过渡金属配合物可催化硼烷对烯烃和炔烃的加成反应,显著提高反应速率,并改变化学选择性、区域选择性及对映选择性27。
机理35-43
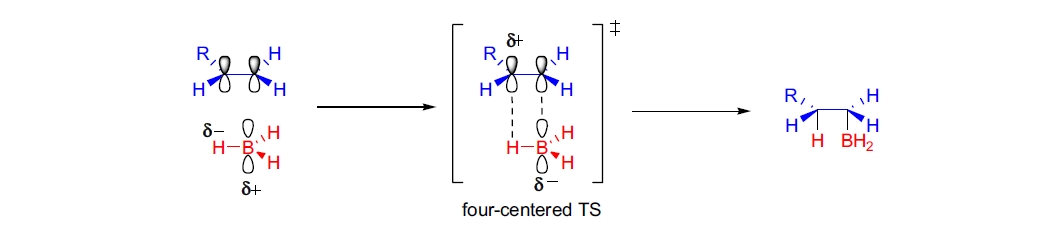
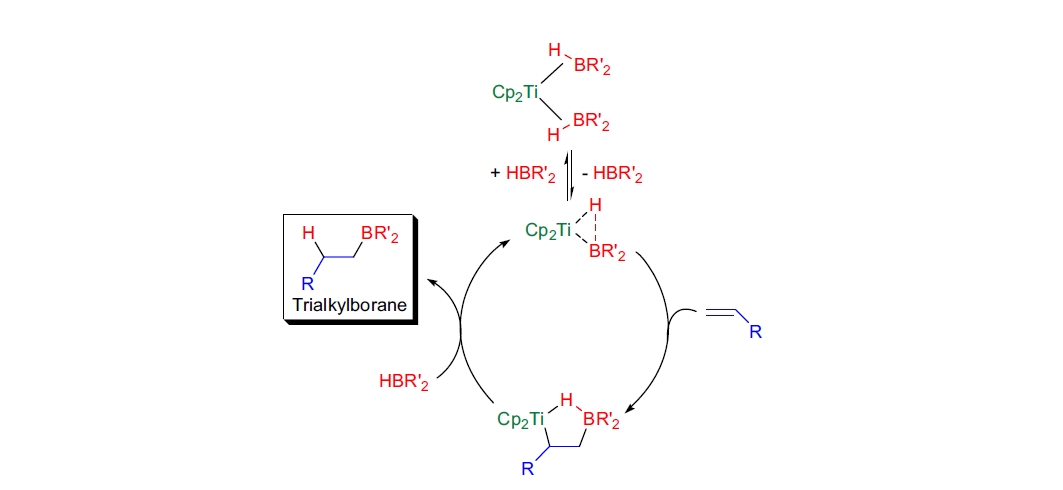
硼原子只有三个价电子,其化合物为电子缺乏型,且硼原子上具有一个空的 p 轨道。硼烷(BH3)以 B2H6/BH3 平衡形式存在,二聚化部分缓解了硼的电子缺陷。该平衡迅速,大多数反应通过 BH3 进行。硼烷对双键的加成为协同过程,经历一个四中心过渡态。C-B 键的形成先于 C-H 键的形成,使得硼和碳在过渡态中部分带电。
合成应用
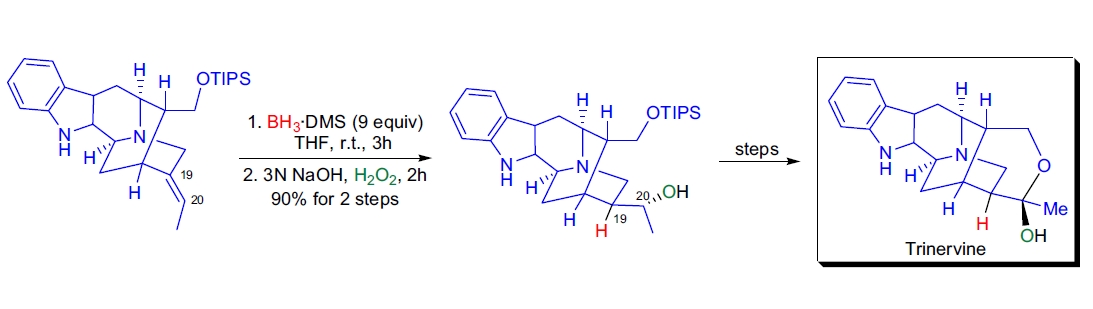
1. Trinervine 的全合成:在 J.M. Cook 实验室中,使用加成/氧化序列以优异的区域选择性功能化了 C19-C20 外双键,从而完成了生物碱 trinervine 的全合成44。
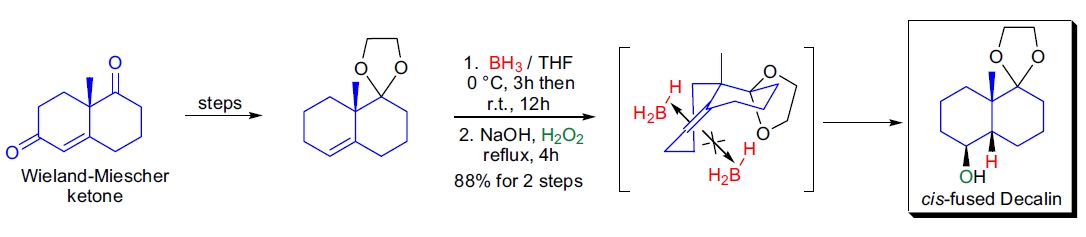
2. 维生素 D 类似物的片段合成:M. Vandewalle 等人发现,对八氢萘衍生物进行加成/氧化处理,得到 cis-癸烷结构,取代了文献报道的 trans 融合结构45。
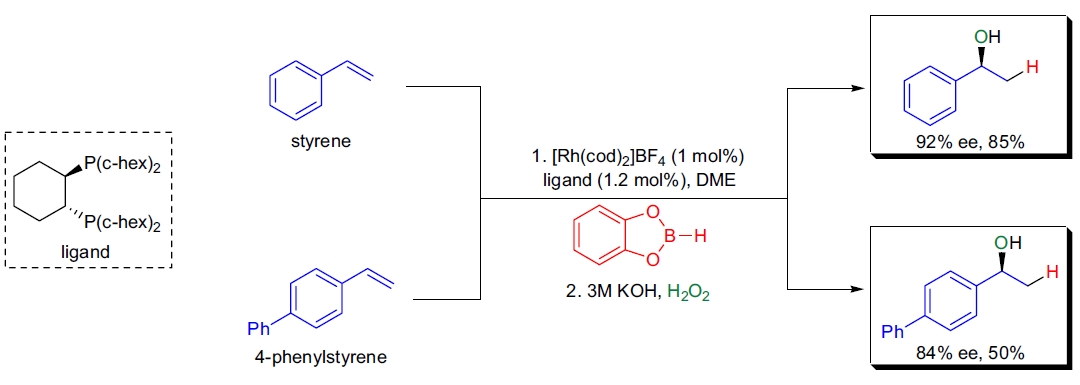
3. Rh 催化的不对称加成:P. Knochel 等人使用二膦配体在铑催化下实现了苯乙烯衍生物的不对称加成。最佳结果为 92% ee 的(S)-1-苯乙醇和超过 99:1 的区域选择性46。
4. (–)-Cassine 的全合成:H. Makabe 实验室中,利用 9-BBN 对氨基烯醇进行加成/氧化后生成所需的一级醇,最终完成了(–)-cassine 的全合成47。