Buchner反应(Buchner ring expansion)
Buchner扩环反应
重要性
[开创性文献1-3;综述4-9;改进与优化10-20]
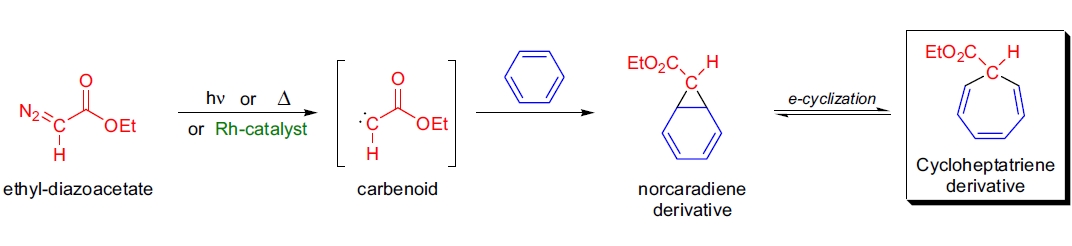
Buchner 反应是指乙基重氮乙酸酯与苯及其同系物发生的热或光化学反应,生成环庚三烯羧酸的相应酯。该反应的核心机制是通过芳烃的环丙烷化形成中间体,然后经电环化开环得到环庚三烯酯。这一反应由 E. Buchner 和 T. Curtius 在 1885 年首次报道,为合成七元碳环提供了重要途径。现代过渡金属催化剂(如 Rh2(OAc)4)的应用极大地提高了反应的选择性。例如,使用 Rhodium(II)-trifluoroacetate 催化可以在 98% 的收率下得到单一异构体的环庚三烯酯11。
机理21-23
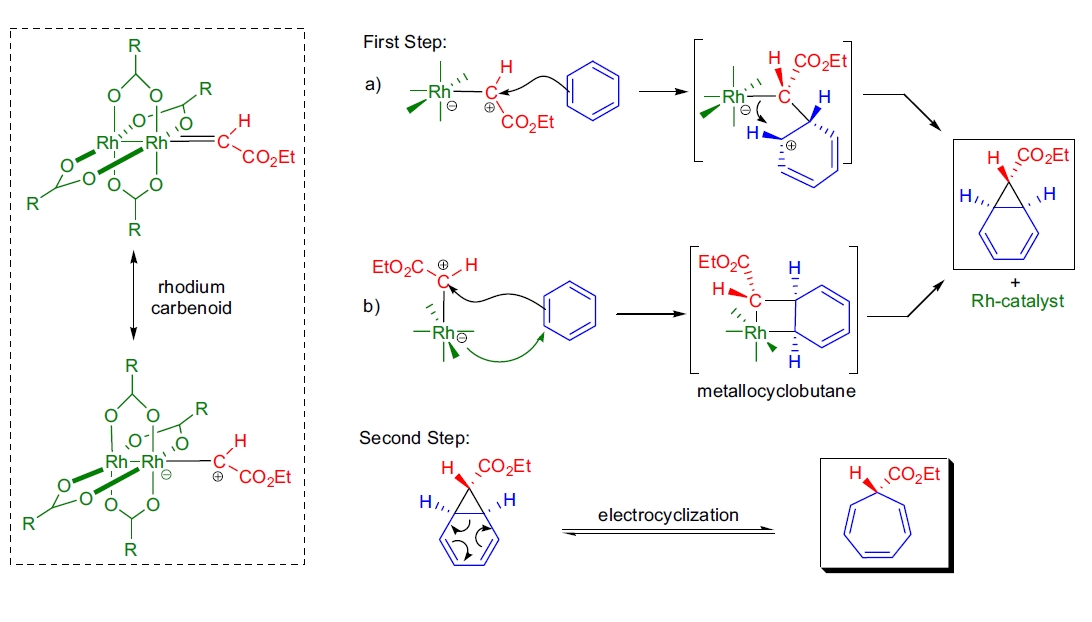
反应的第一步是芳香环的一个 π 键与金属-羰基中间体发生环丙烷化反应。金属羰基中间体是通过过渡金属催化剂(如 Rh2(OCOR)4)与重氮化合物反应生成的暂时性亲电中间体。随后,得到的环丙烷化产物经电环化反应生成环庚三烯衍生物。催化剂的活性取决于金属中心的配位不饱和度,从而使其能够与重氮化合物发生亲电反应。
合成应用
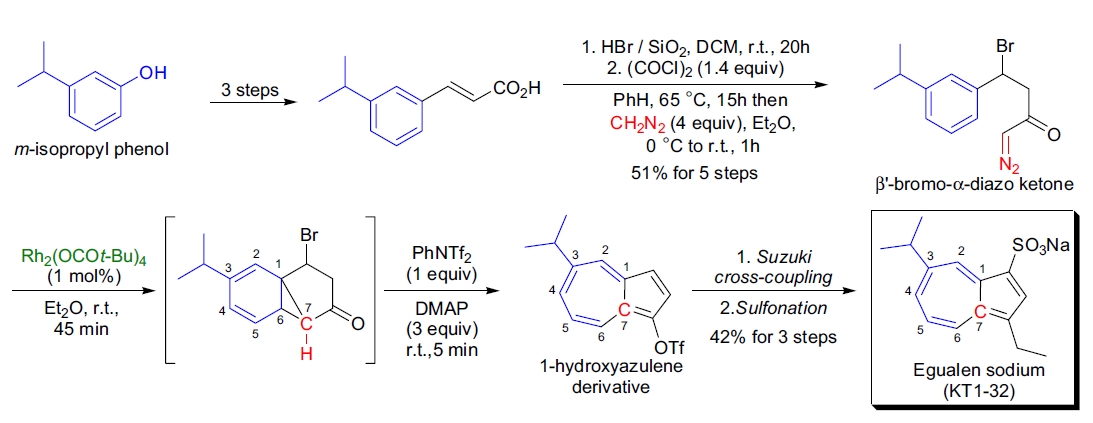
1. Azulene 衍生物的合成:R.L. Danheiser 等人利用 β-溴-α-重氮酮与 Rh2(OAc)4 催化剂,开发了合成取代的 Azulenes 的新策略。这一方法应用于抗溃疡药物 Egualen Sodium(KT1-32)的全合成24。
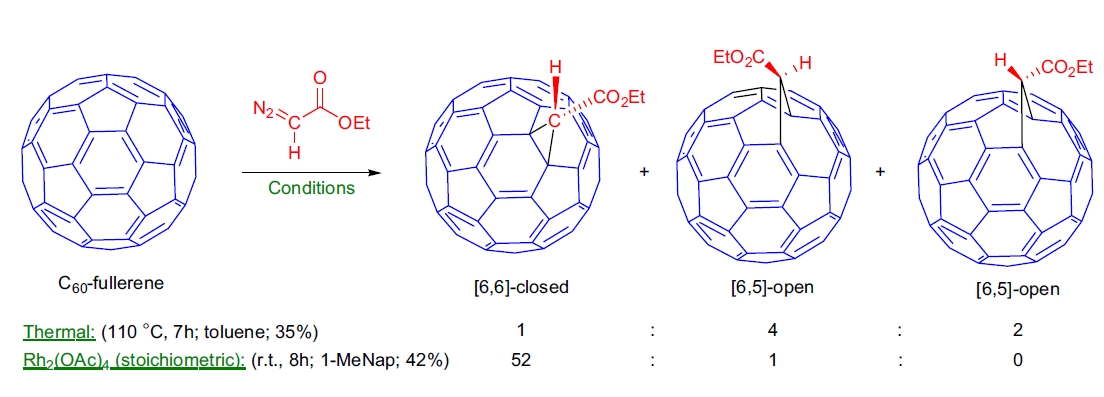
2. 富勒烯衍生物的功能化:R. Pellicciari 等人通过 Rh2(OAc)4-催化分解 α-重氮酯与 C60 反应,实现了富勒烯的功能化,生成高选择性的 [6,6]-甲基富勒烯羧酸酯,条件温和且特异性高25。
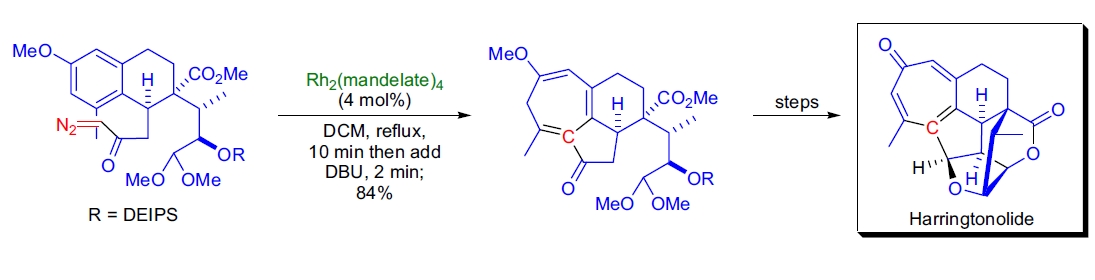
3. Harringtonolide 的全合成:L.N. Mander 实验室中,利用 Buchner 反应完成了二萜醌 Harringtonolide 的七元环构建。这一反应通过 Rhodium Mandelate 催化生成环庚三烯中间体,再经 DBU 处理得到稳定化产物26。