Cannizzaro 反应
重要性
[开创性文献1,2;综述3;改进与优化4-14;理论研究15,16]
Cannizzaro 反应是指无 α-氢的脂肪族或芳香族醛在浓 NaOH (50 wt%) 或其他强碱(如醇盐)条件下发生的一种分子间氢化物转移反应。在该歧化反应中,一个醛分子氧化另一分子生成相应的羧酸,同时被还原为相应的伯醇(理论最高产率为 50%)。当醛含有 α-氢时,醛醇缩合反应的速率通常快于 Cannizzaro 反应。在存在过量甲醛的条件下,几乎所有醛均可通过交叉 Cannizzaro 反应高产率生成伯醇。α-酮醛则可发生分子内 Cannizzaro 反应。此外,反应在无溶剂条件下的速率显著提高。尽管如此,由于 1946 年氢化物还原剂的出现,该方法已逐渐被取代。
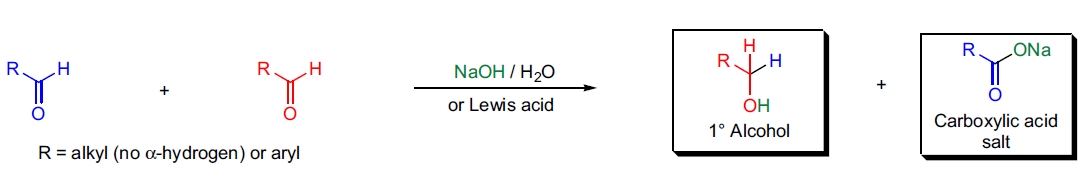
机理17-23
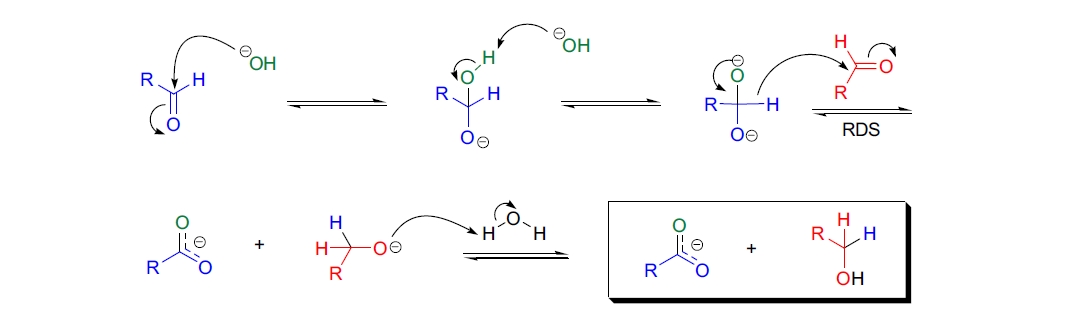
Cannizzaro 反应的公认机理涉及氢化物转移。首先,OH- 进攻羰基形成四面体中间体,该中间体在碱性条件下脱质子生成二负离子。随后,二负离子使醛基中的氢以氢化物离子形式离去,后者进攻另一个醛分子生成醇盐,醇盐最终被质子化为伯醇。在重水 (D2O) 中进行反应时,生成的伯醇中未观察到氘,表明氢化物来自另一醛分子而非反应介质。此外,ESR 谱研究表明取代苯甲醛与 NaOH 或 KOt-Bu 反应时生成自由基阴离子,表明反应可能通过单电子转移 (SET) 机制进行。
合成应用
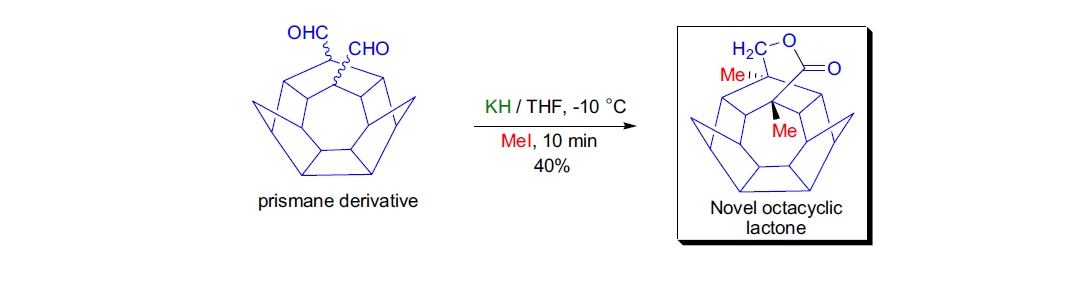
1. 新型跨环 Cannizzaro 反应:G. Mehta 等人在研究 1,4-双高碳环-6-seco[7]prismane 二醛衍生物时,发现其在碱性条件下经历了新颖的跨环 Cannizzaro 反应生成八环内酯24。
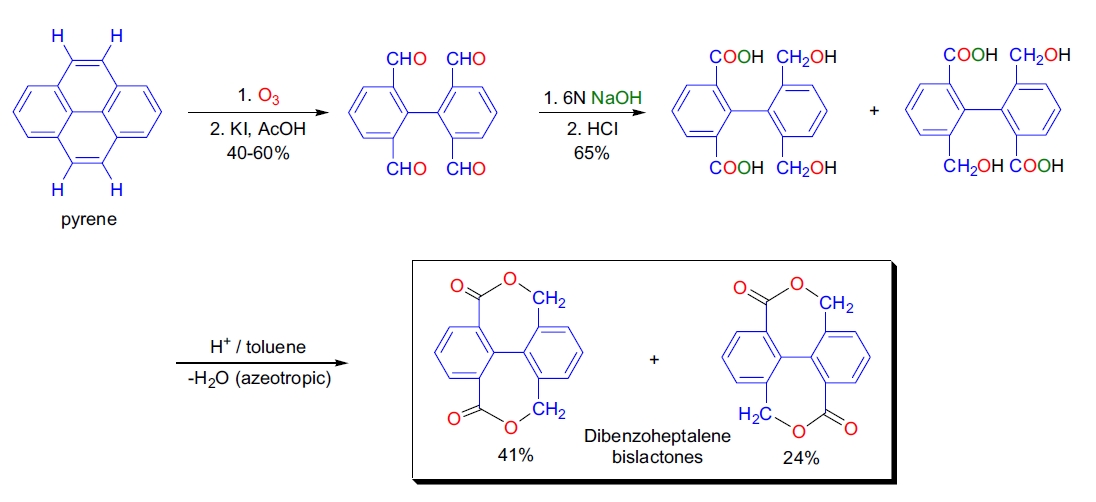
2. 双分子内 Cannizzaro 反应:J. Rebek 等人通过双分子内 Cannizzaro 反应合成了新型二苯并庚稠缩双内酯,用于缩合聚合和远程催化研究25。
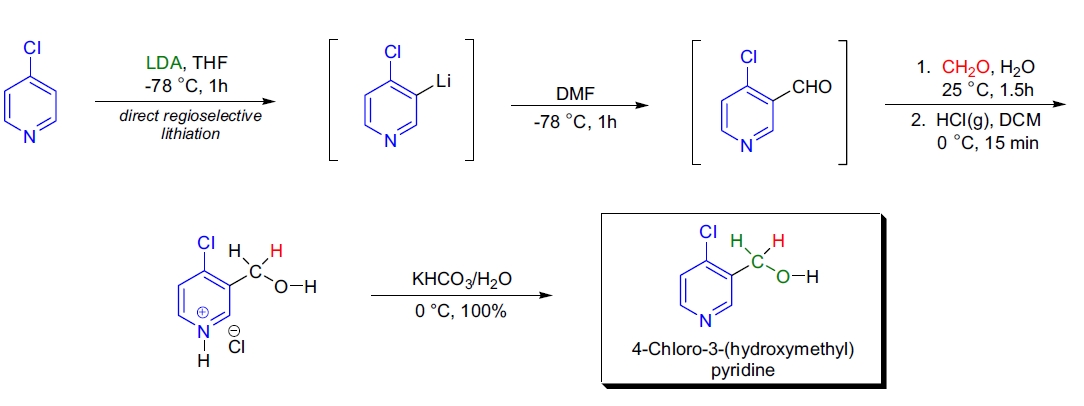
3. 交叉 Cannizzaro 反应:在 M. Penso 等人的研究中,4-氯吡啶的直接区域选择性锂化/甲酰化和交叉 Cannizzaro 还原被用于合成多官能分子4-氯-3-(羟甲基)吡啶,该分子可与头孢菌素偶联26。
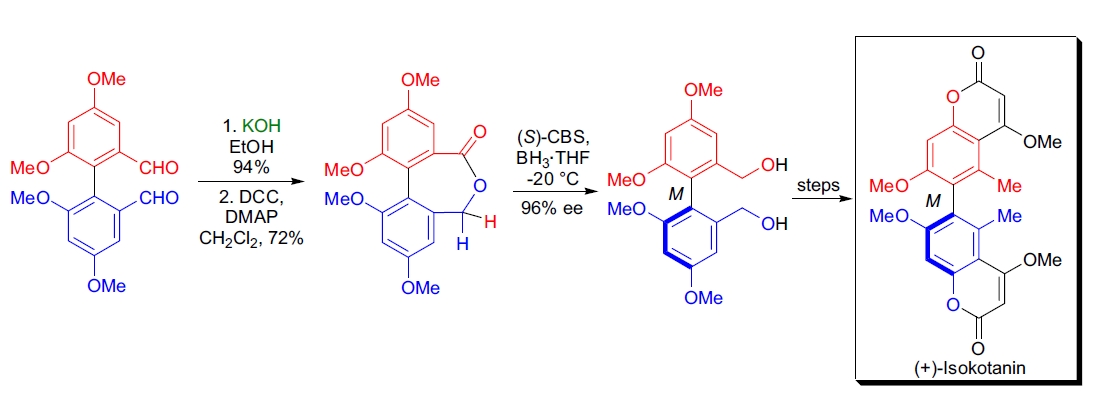
4. (+)-Isokotanin 的全合成:J. Bringmann 等人通过关键的 Cannizzaro 反应生成轴向手性双香豆素 (+)-Isokotanin 的构型稳定的七元双芳基内酯,并通过对映选择性环裂解进行动力学拆分27。