Carroll 重排反应
Kimel-Cope 重排反应
脱羰Claisen重排反应
重要性
[开创性文献1,2;综述3,4;改进与优化5-12]
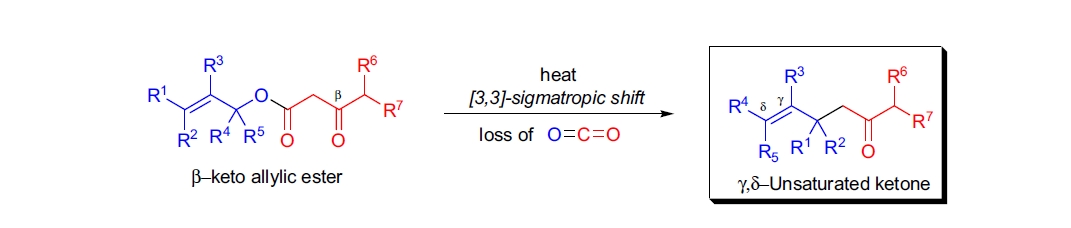
Carroll 重排反应(亦称为 Kimel-Cope 重排反应或脱羧 Claisen 重排反应)是指烯丙基 β-酮酯通过 [3,3]-σ迁移生成 γ,δ-不饱和酮的反应。尽管该反应早在 1940 年被发现,但直到 1990 年代初才应用于药物合成6。由于需在 130-220 °C 的苛刻条件下进行,该反应在合成有机化学中应用较少。然而,通过改变 β-酮酯前体结构,这些热屏障得以降低6-12。反应的主要变体包括伴随 β-酮酸脱羧的反应;通过酯化或分子内内酯化,可以在低温下避免脱羧,生成的产物表现出优异的 syn/anti 选择性。
机理13,14
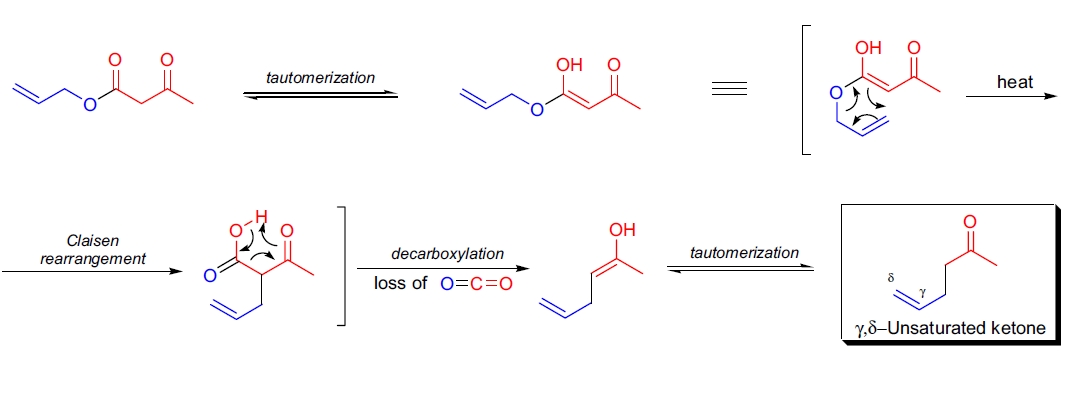
Carroll 重排反应通过 [3,3]-σ迁移机理进行。首先,β-酮酯通过烯醇或酯负离子形成中间体,随后在适宜温度下重排为 γ,δ-不饱和酮。若 β-酮酸脱羧,生成脱羧产物;若 β-酮酸酯化或内酯化,则避免脱羧,生成环状或酯化的重排产物。
合成应用
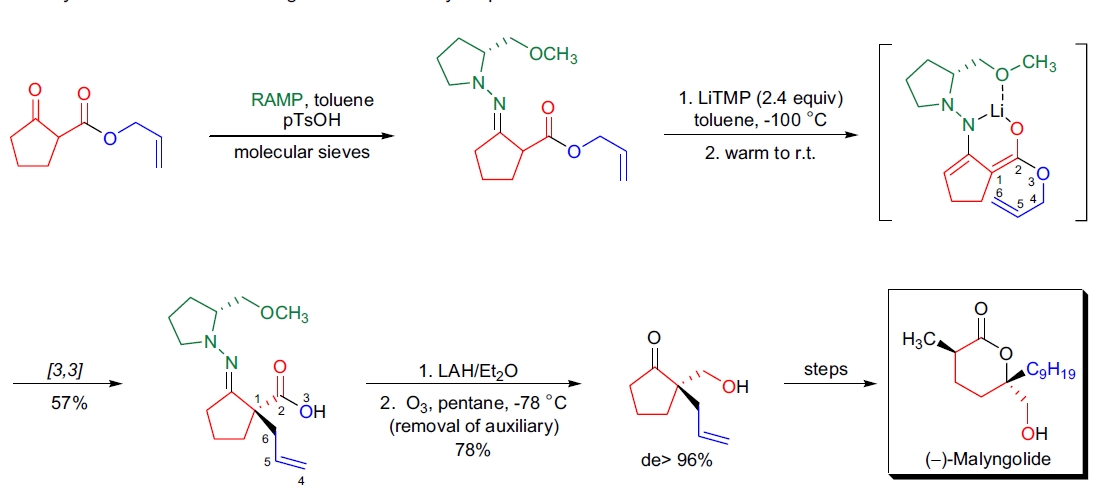
1. (–)-Malyngolide 的全合成:D. Enders 等人通过不对称 Carroll 重排反应成功实现了抗生素 (–)-malyngolide 的全合成,证明了该反应的立体控制能力11。
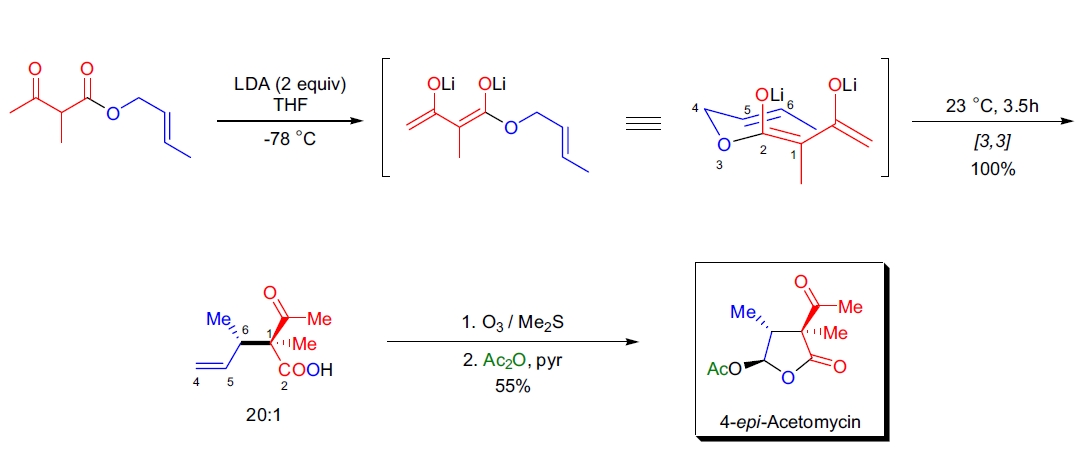
2. (±)-4-Epi-Acetomycin 的全合成:A.M. Echavarren 实验室利用 (E)-丁烯基-2-甲基乙酰乙酸酯的不对称酯负离子 Carroll 重排反应,并结合臭氧化和乙酰化步骤,完成了抗生素 (±)-4-epi-acetomycin 的全合成6。
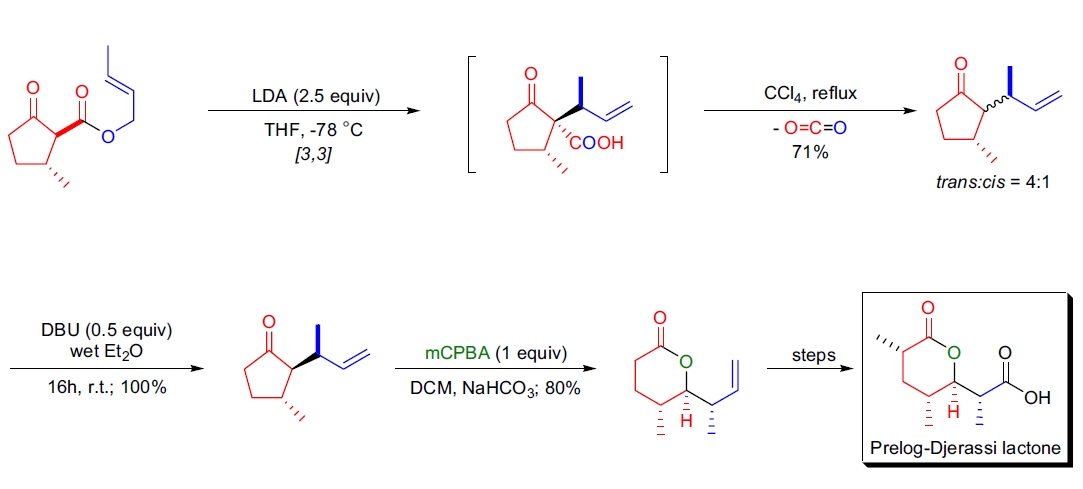
3. Prelog-Djerassi 内酯的合成:J. Rodriguez 等人研究了 (E)- 和 (Z)-烯丙基 β-酮酯的不对称酯负离子 Carroll 重排反应,为合成 Prelog-Djerassi 内酯及相关化合物提供了一种新颖方法7。
4. 取代芳基丙酮的合成:K.L. Sorgi 等人利用取代 p-醌制备乙酰乙酸酯,并在室温下通过 Carroll 重排反应成功合成了取代芳基丙酮及相关衍生物,产率从中等至优异10。