Claisen 缩合反应
重要性
[开创性文献1;综述2-8;改进与优化9-11;理论研究12-14]
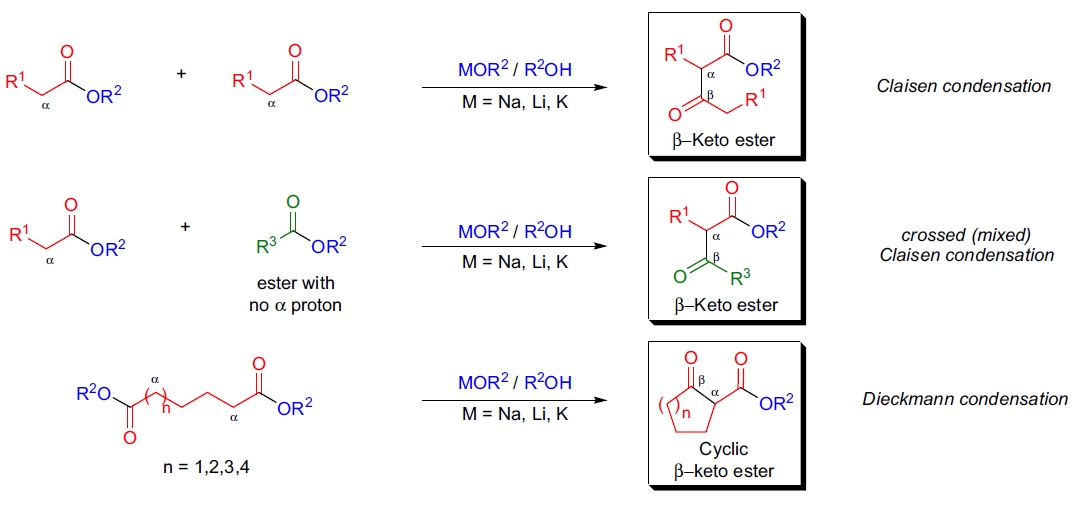
Claisen 缩合反应是指含有 α-氢的酯分子与另一个相同酯分子缩合生成 β-酮酯的过程。如果反应中的两个酯基通过链相连,则称为 Dieckmann 缩合。当两个不同的酯在相同条件下反应时,称为交叉(混合)Claisen 缩合。为了避免多种产物的形成,通常选择不含 α-氢的酯作为接受体(例如芳香酸、甲酸或草酸的酯)。该反应需要等当量的碱(如烷氧化物、LDA 或 NaH),且当使用烷氧化物时,必须与酯的醇部分相匹配,以避免酯交换引起的产物混杂。其他两种变体包括酯烯醇盐与酮或醛反应生成 β-羟基酯,以及酮或醛烯醇盐与酯反应生成 1,3-二酮。
机理15-23
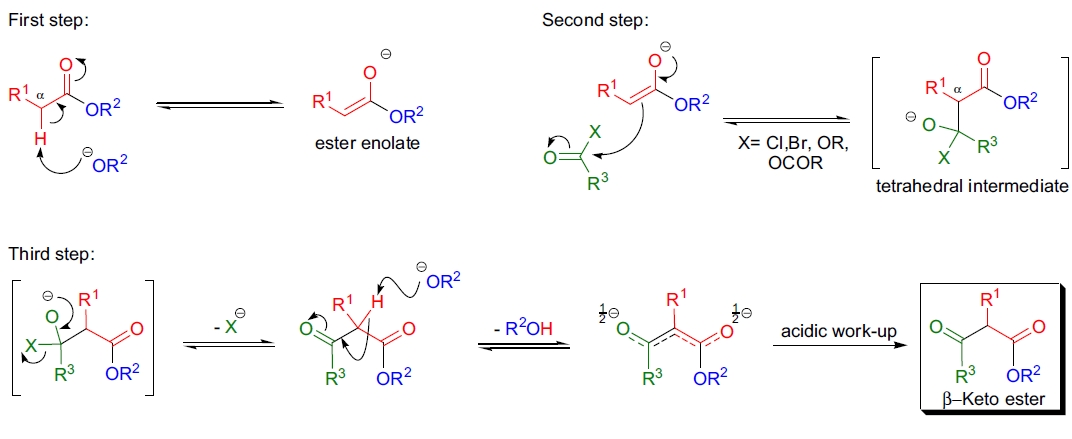
反应的第一步是碱去质子化酯的 α-氢,生成酯烯醇盐作为亲核试剂。随后,烯醇盐进攻另一酯分子的羰基,形成四面体中间体;接着,中间体通过离去基团(烷氧基或卤化物)分解生成 β-酮酯。在反应的碱性条件下,产物 β-酮酯的 α-氢被去质子化,形成共振稳定的阴离子,从而防止进一步反应。
合成应用
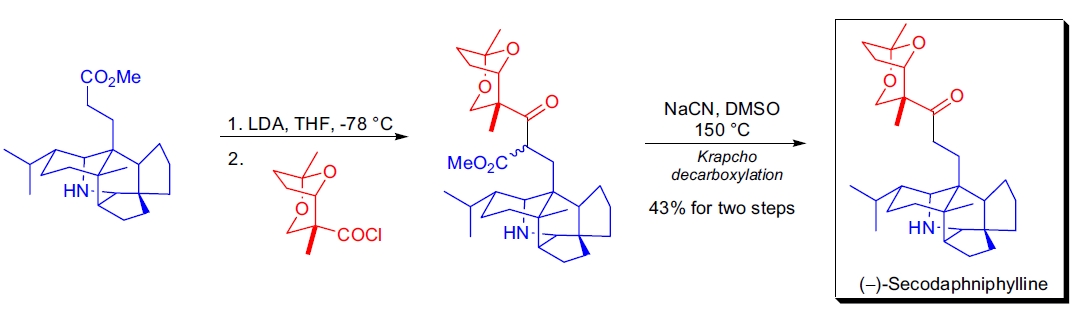
1. Secodaphniphylline 的全合成:C.H. Heathcock 等人通过混合 Claisen 缩合实现了(–)-secodaphniphylline 的高效不对称全合成。在合成的最后阶段,利用(–)-甲基 homosecodaphniphyllate 的锂烯醇盐与 2,8-二氧杂双环[3.2.1]辛烷酰氯反应生成 β-酮酯混合物,并通过 Krapcho 脱羧反应两步获得天然产物,产率为 43%24。
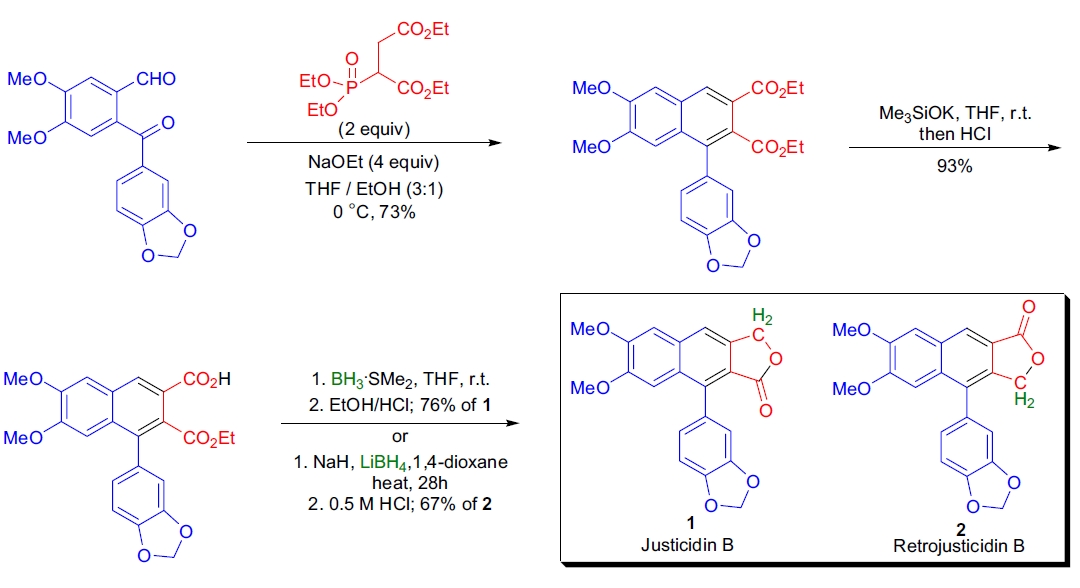
2. Justicidin B 和 Retrojusticidin B 的全合成:D.C. Harrowven 等人使用醛和亚磷酸四酯之间的新型串联 Horner-Emmons 烯化/Claisen 缩合反应,成功合成了天然产物的高取代萘核。二酯产物进一步转化为 Justicidin B 和 Retrojusticidin B,产率为 73%25。
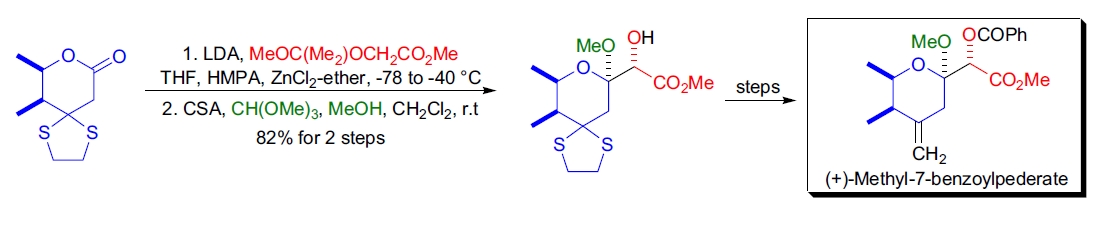
3. Mycalamides 前体的合成:T. Nakata 等人开发了一种简单高效的方法来合成 (+)-methyl-7-benzoylpederate,其关键步骤包括 Evans 不对称醛醇反应、选择性 Claisen 缩合和 Takai-Nozaki 烯化反应26。