Claisen 重排反应
重要性
[开创性文献1,2;综述3-32;改进与变体33-48;理论研究49-55]
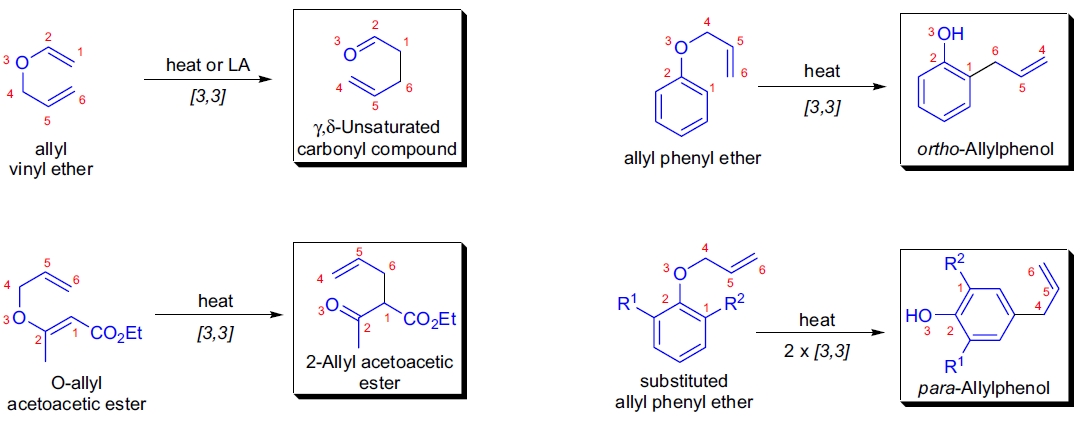
Claisen 重排反应由 L. Claisen 于 1912 年首次报道,描述了烯丙基苯醚热解生成 C-烯丙基酚的反应过程1。该反应属于 [3,3]-σ迁移反应,可将烯丙基乙烯醚转化为 γ,δ-不饱和羰基化合物。烯丙基乙烯醚可以通过多种方式制备,包括汞离子催化交换、酸催化交换、Wittig 烯化和 Tebbe 烯化等。通常,不需要分离中间体烯丙基乙烯醚,因其可在生成条件下直接重排。
机理66,67,6,68-70,18,20,31
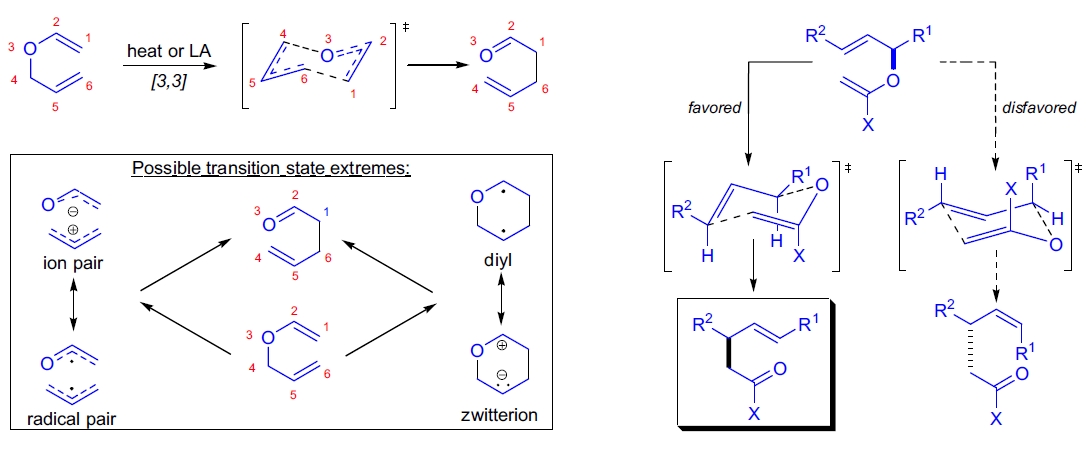
Claisen 重排反应是一个单分子 [3,3]-σ迁移反应,经过超面、协同、非同步的六元环状过渡态完成。立体化学研究表明,双键的立体信息可传递至新生成的 σ 键。过渡态通常为六元椅式,但当大位阻效应或其他几何限制排除椅式结构时,反应可能通过舟式过渡态进行。此外,手性烯丙醇生成的烯丙基乙烯醚可将手性传递至产物,其选择性由不同过渡态的能量差决定。
合成应用
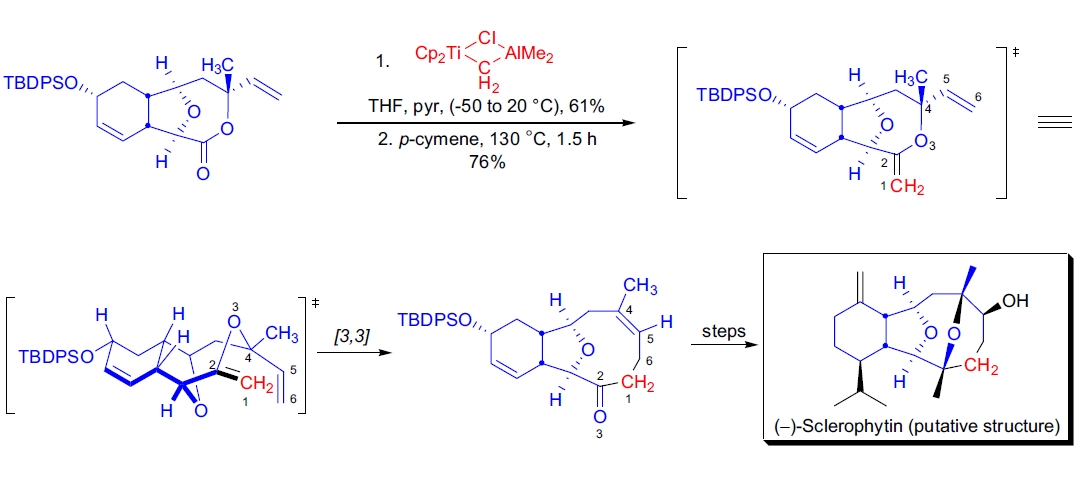
1. Sclerophytin A 的全合成:在 L.A. Paquette 的实验室中,通过 Tebbe-Claisen 重排反应完成了(–)-Sclerophytin A 的全合成。三环内酯前体经 Tebbe 甲亚烯化后,生成的烯丙基乙烯醚在 130-140 °C 的对异丙苯中加热发生 Claisen 重排,产率较高73。
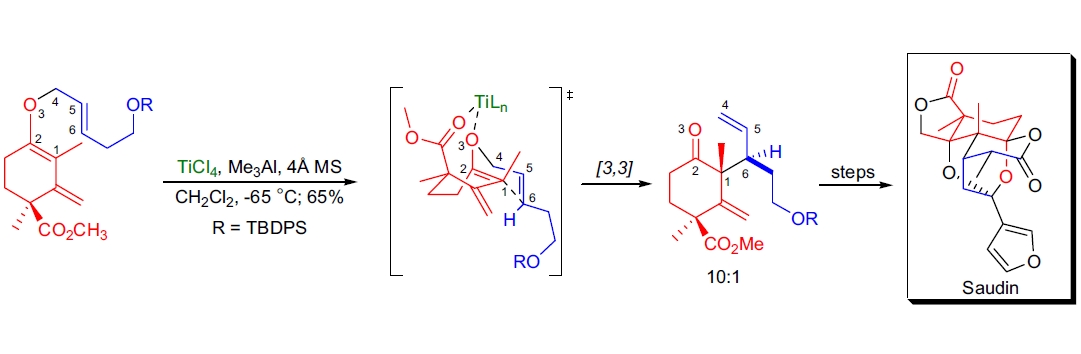
2. Saudin 的全合成:R.K. Boeckman Jr. 等人通过 Lewis 酸 TiCl4 催化的立体选择性 Claisen 重排反应,完成了 (+)- 和 (–)-Saudin 的全合成。该反应通过协调效应强制过渡态采用舟式构象74。
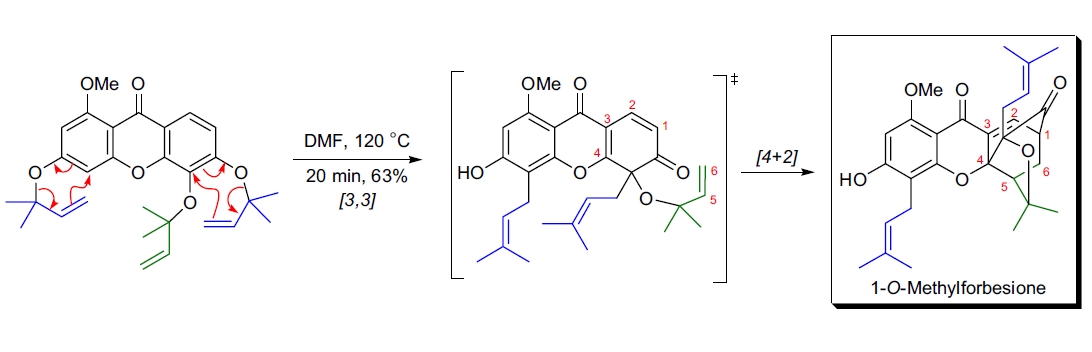
3. 1-O-Methylforbesione 的生物仿生合成:K.C. Nicolaou 通过双 Claisen 重排反应与分子内 Diels-Alder 反应串联完成了 1-O-Methylforbesione 的合成。这一一步法生物仿生反应以 63% 的产率生成目标产物75。