Dieckmann 缩合
重要性
[开创性文献¹,²;综述³-⁸;改进与优化⁹-¹⁷]
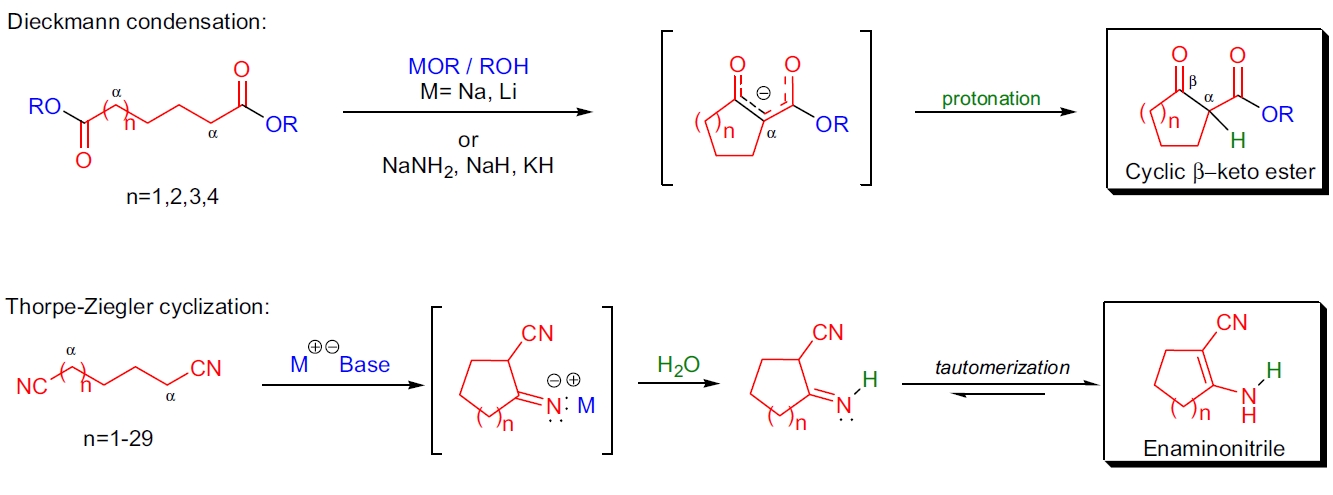
含有 α-氢原子的酯与另一分子相同酯在碱介导下缩合生成 β-酮酯的反应称为 Claisen 缩合。当两个反应的酯官能团通过分子内连接时,该反应称为 Dieckmann 缩合,并生成环状 β-酮酯。在相关的 Thorpe-Ziegler 缩合中,二腈在碱催化下发生分子内环化生成烯胺腈。¹⁸,¹⁹ 常用的方法是在干燥溶剂中,在惰性气氛下回流,并使用至少 1 当量的强碱(烷氧化物、钠酰胺或碱金属氢化物)处理二酯较长时间。²⁰ Dieckmann 缩合能高产率形成 5、6、7 和 8 元环,但对于更大的环,产率很低。²¹,⁴ 然而,通过高稀释条件可以使分子内反应占主导地位,在某些情况下可以制备大环(>12 元环)。²²,²³ 如果产物 β-酮酯没有酸性 α-氢,则反应较慢,且逆 Dieckmann 环化占主导地位;若使用 1 当量无醇碱,平衡会向右移动。对于 Thorpe-Ziegler 环化,可以组装 5 至 33 元环,并且这种方法在 7 和 8 元环的形成上优于 Dieckmann 缩合。原始 Dieckmann 方法的改进使得可以使用温和的反应条件:
- 用钠氢化物处理二硫醇(或二硫酯),在室温下仅需 2 小时即可完成环化;⁹
- 环境友好的无溶剂条件下允许空气存在,反应在室温下 1 小时内以高产率进行;¹⁶
- 在甲苯中使用 TiCl₄/Bu₃N 和催化量 TMSOTf,可在室温下 2-3 小时内获得高产率。¹⁴,²⁴,¹⁷
机理25-31
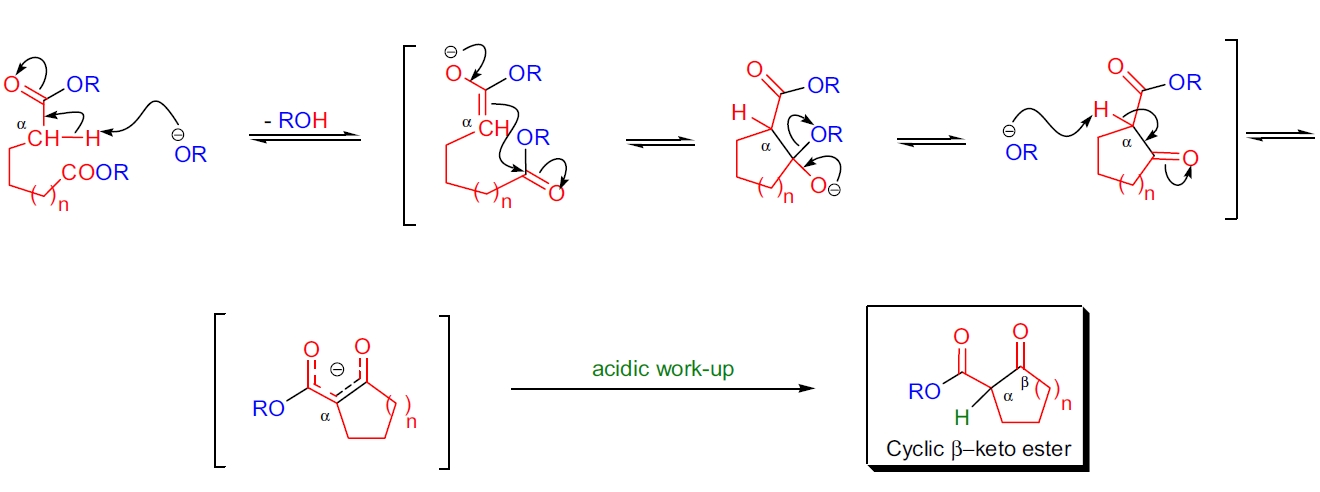
Dieckmann 缩合的每一步都是完全可逆的。反应的驱动力是生成产物 β-酮酯的共振稳定的烯醇负离子。如上所述,如果无法生成这种稳定的中间体,缩合通常会失败。Dieckmann 缩合的机制几乎与 Claisen 缩合的机制相同。然而,决定速率的步骤是环的形成,在此过程中酯烯醇负离子攻击第二个酯官能团的羰基。²⁵,²⁶ 所得的四面体中间体迅速分解为 β-酮酯的烯醇负离子。烯醇负离子经质子化后得到最终产物。
合成应用
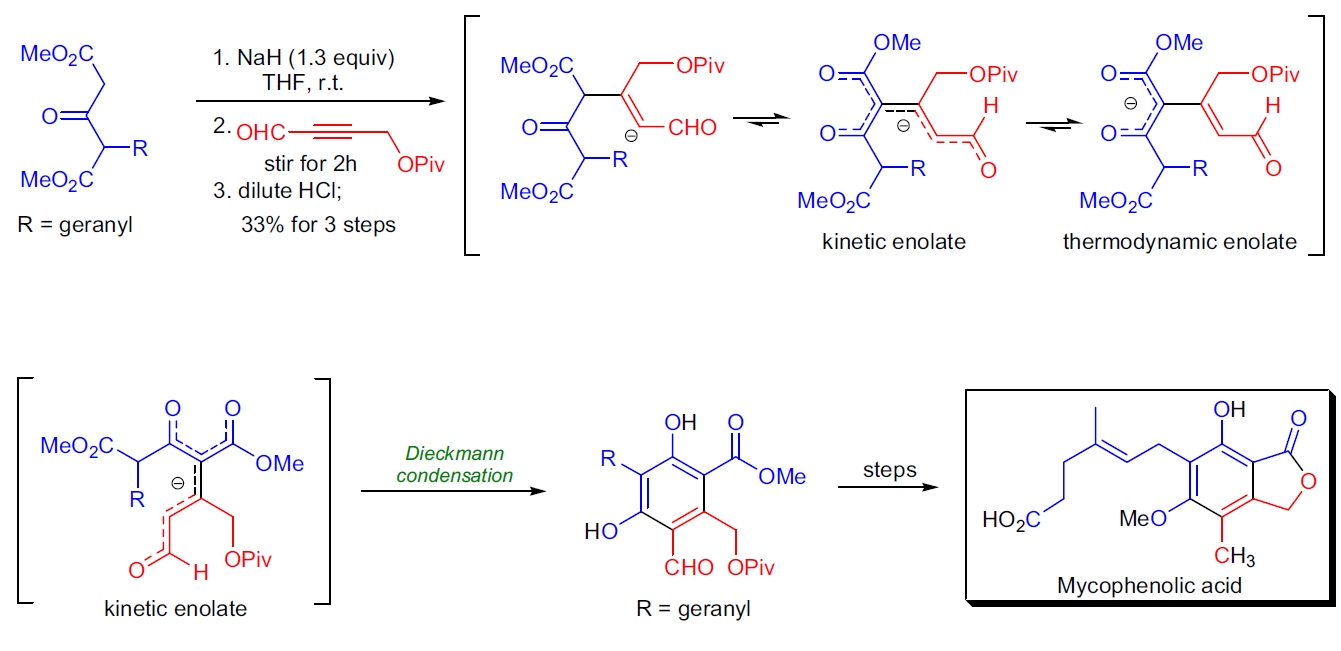
1. 霉酚酸的合成:霉酚酸是一种高度取代的邻苯二甲酸内酯类天然产物,具有许多体内和体外的生物活性。A. Covarrubias-Zúñiga 的全合成策略基于以 Michael 加成和 Dieckmann 缩合为关键步骤的环并反应序列。³² 用钠氢化物去质子化 2-异戊二烯基-1,3-丙二酸酯后,加入保护的炔醛生成原位烯醇负离子,该负离子环化为天然产物的六取代芳环,产率为 33%。
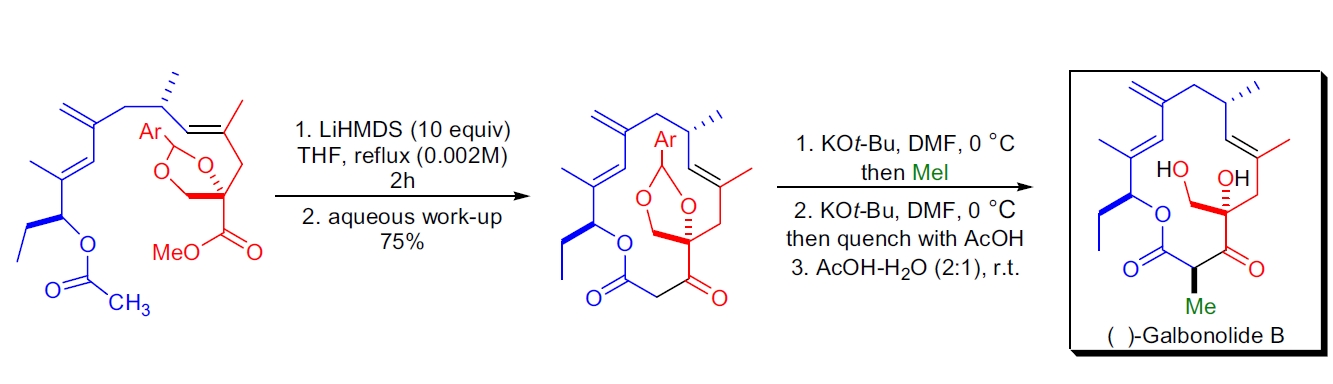
2. (-)-Galbonolide B 的合成:其 14 元大环是通过一种新型宏观 Dieckmann 缩合形成。用 LiHMDS 在高稀释条件下于回流 THF 中处理二级乙酸酯,得到目标内酯,产率为 75%。³³
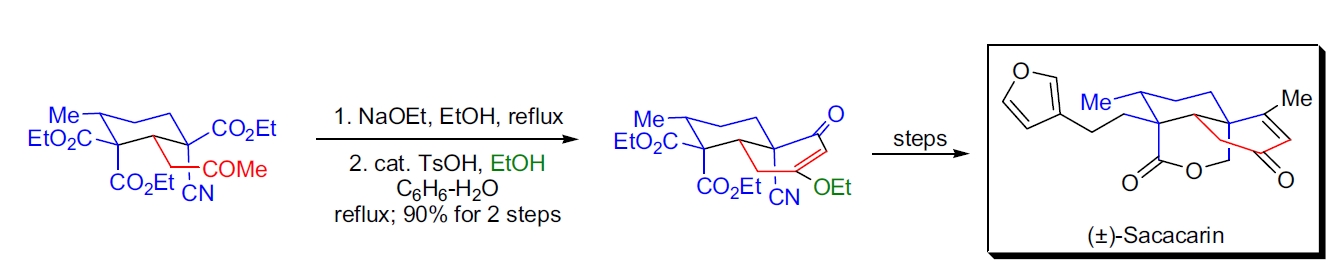
3. (±)-Sacacarin 的合成:天然存在的 clerodane 二萜类化合物 (±)-sacacarin 的第二个环通过分子内 Dieckmann 缩合以优异的产率制备而成。³⁴ Sacacarin 的第二个环通过酯与甲基酮的分子内 Dieckmann 缩合制备,生成的烯醇随后立即使用乙醇和酸催化剂转化为相应的乙基烯醇醚。