Diels-Alder 环加成反应
重要性
[开创性文献1-4;综述5-47;理论研究48-66]
[4π + 2π] 环化反应将二烯和烯烃环加成生成环己烯衍生物,称为 Diels-Alder 环加成反应 (D-A 环加成)。20 世纪初期,H. Wieland⁶⁷、W. Albrecht⁶⁸、Thiele、H. Staudinger 和 H.V. Euler⁶⁹ 报道了此类环化反应,但错误地确定了产物结构。直到 1928 年,O. Diels 和 K. Alder 才确定了 p-苯醌与环戊二烯环加成产物的正确结构。² 从发现以来,D-A 环加成已成为使用最广泛的合成工具之一。
Diels-Alder反应有以下特点:
- 1)能在一步中设置四个立体中心;
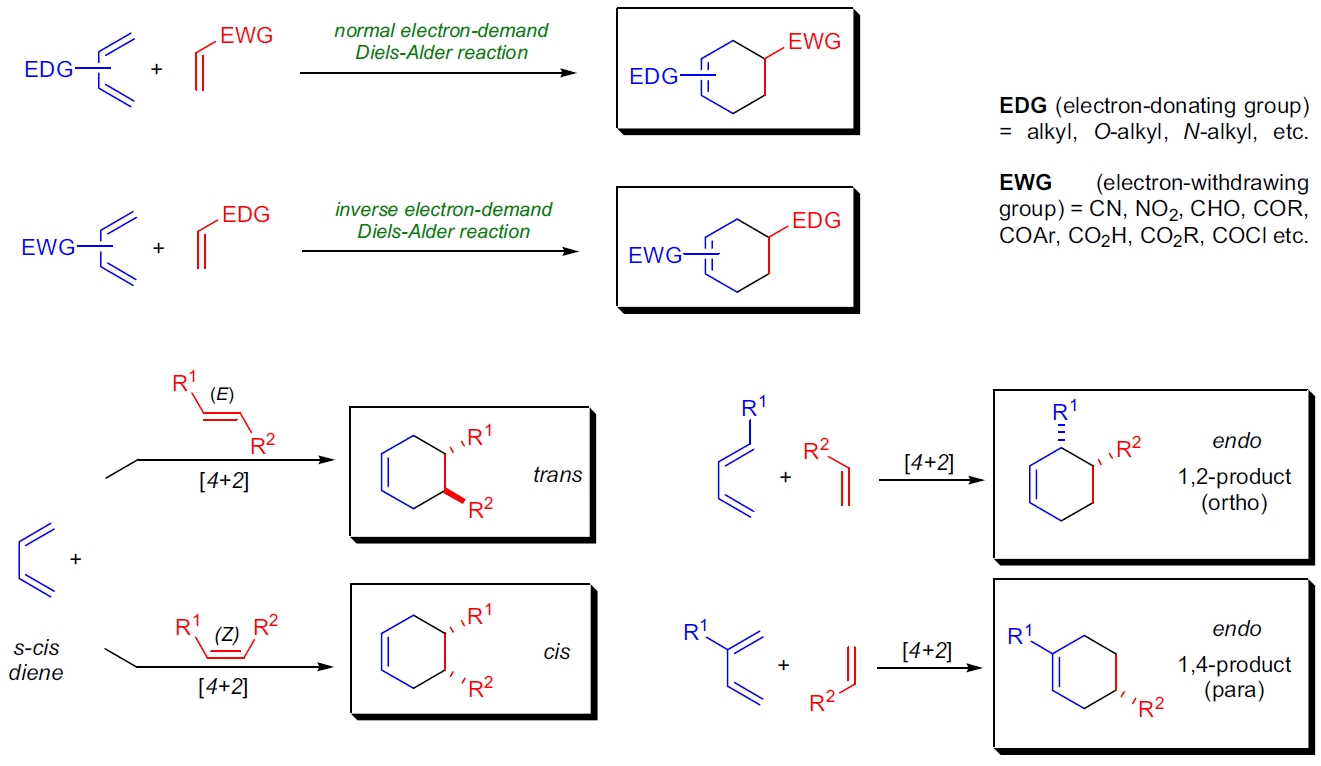
- 2)如果不对称二烯和二烯亲和体反应,则具有高度区域选择性和立体特异性;
- 3)区域异构体以“邻”位和“对”位产物为主,而非“间”位产物;
- 4)如果使用顺式 (Z) 烯烃作为二烯亲和体,则产物中的两个取代基为顺式;而如果使用反式 (E) 烯烃,则产物中取代基为反式;
- 5)二烯中的立体化学信息 (E 或 Z) 也会转移到产物中;
- 6)主要产物为内环加成产物;
- 7)使用适当的手性催化剂,可使环加成反应具有对映选择性;⁷¹⁻⁷³,⁴¹
- 8)能在一步中形成多个具有明确立体化学的环。
机理23,74-86
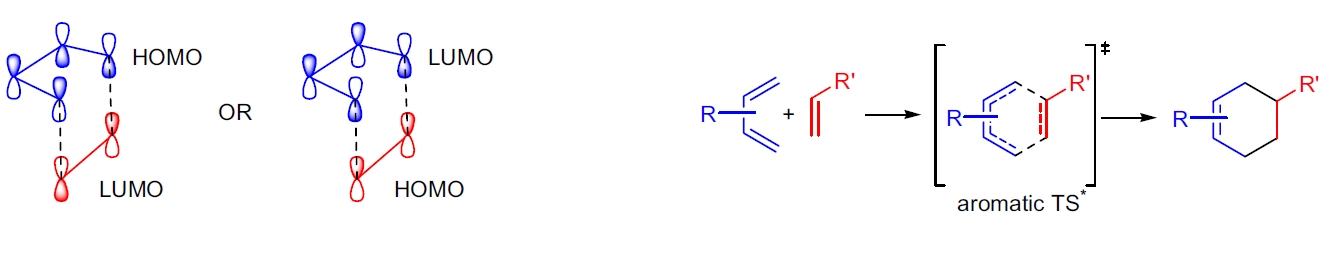
在机理上,D-A 反应被认为是一种协同的、周环反应,具有芳香过渡态。其驱动力是形成两个新的σ键。内环加成产物为动力学产物,其形成可用次轨道相互作用解释。⁸⁰ 一些机理研究表明,在某些情况下,可能涉及双自由基⁷⁹ 或双离子机理。⁸² 研究还表明,溶剂和盐类会影响反应动力学。³⁸
合成应用
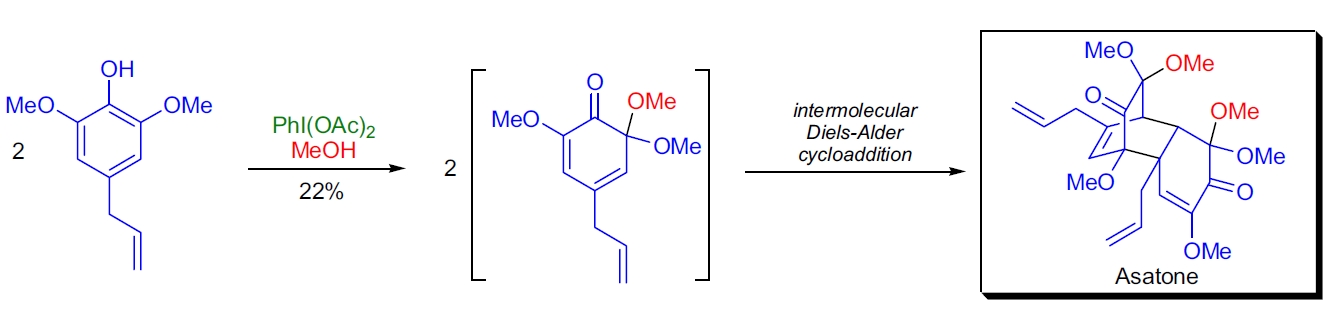
1. Diels-Alder 反应的应用:分子内 Diels-Alder 环加成反应是一种非常强大的合成工具,因为它可以在一步中产生构建多个手性中心。S. Antus 等人通过使用高价碘试剂 (例如 PIDA) 将邻甲氧基酚脱芳构化为反应性环己二烯酮。这些二烯酮迅速二聚,生成高度取代的三环化合物。用 PIDA/甲醇处理 2,6-二甲氧基-4-烯丙基酚,仅一步就生成天然产物 asatone。⁸⁷
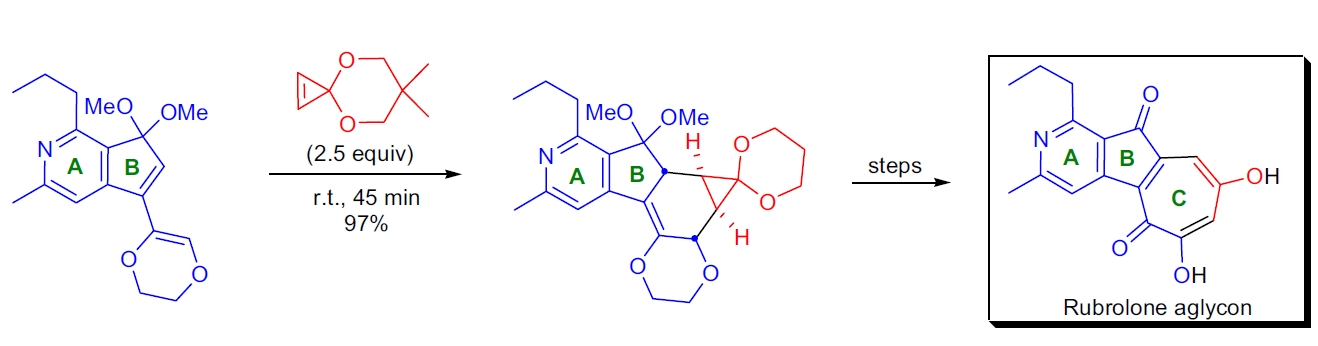
2. Rubrolone 的合成:D.L. Boger 的实验室完成了 rubrolone aglycon 的全合成,其中关键步骤是富电子二烯与高应力二烯亲和体的分子间 Diels-Alder 环加成反应。该环加成反应以 97% 的优异产率进行,且具有完全的对映选择性选择性。⁸⁸
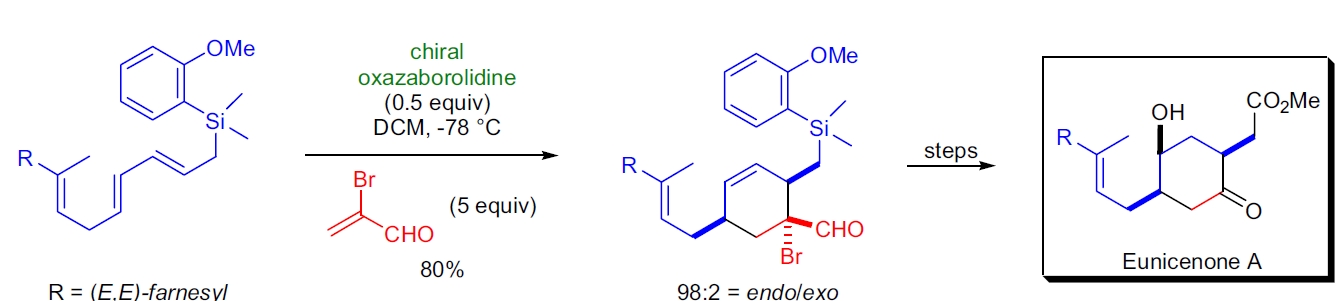
3. Eunicenone A 的合成:E.J. Corey 等人对 Eunicenone A 的全合成中,关键步骤是高效手性路易斯酸催化的分子间 Diels-Alder 环加成反应。在 CH₂Cl₂ 中,将二烯与 5 当量的 2-溴丙醛和 0.5 当量的手性氧杂硼啶催化剂混合,在 -78 °C 反应 48 小时。该反应以 80% 的产率生成所需的环加成产物,对映选择性为 97% ee,内环/外环选择性为 98:2。⁸⁹
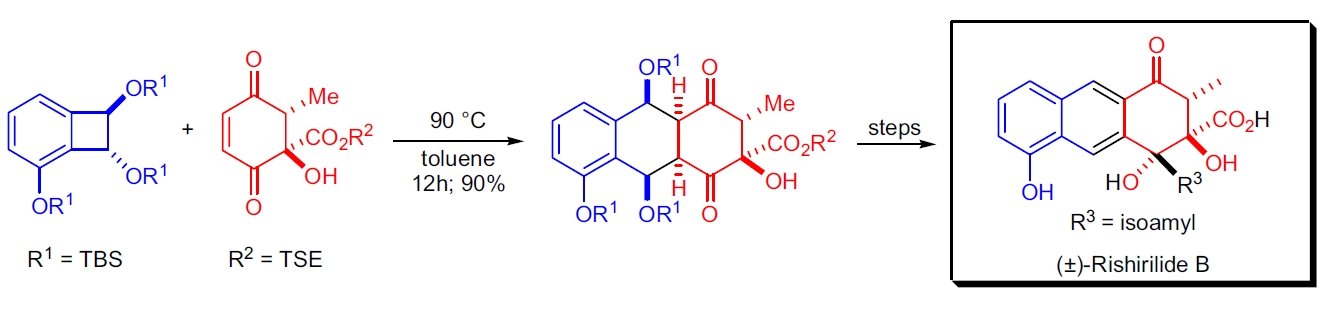
4. (±)-Rishirilide B 的合成:某些官能团通过氢键作用可诱导分子间 Diels-Alder 环加成反应。在 S.J. Danishefsky 的实验室中,全合成 (±)-Rishirilide B 的关键步骤通过热解生成的二烯与目标亲二烯体进行分子间 Diels-Alder 环加成。⁹⁰