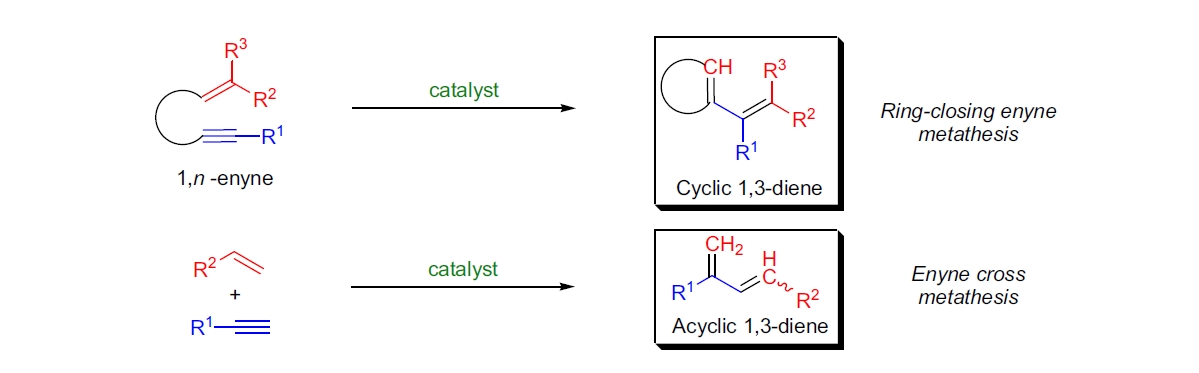
炔烯复分解反应(enyne metathesis)
重要性
[开创性文献1-5;综述6-16;改进与优化17-23;理论研究24,25]
1985年,T.J. Katz 报道了在生物芳基1,7-炔烯暴露于1 mol%钨 Fischer 卡宾配合物下,发生亚甲基迁移生成1,3-二烯的反应,产率为31%。1 这是首次报道金属卡宾催化炔烯中烯烃与炔之间碳-碳多键的分子内重分布。炔烯复分解主要有两种形式:环闭型炔烯复分解和交叉炔烯复分解。
- 1)单取代烯比双取代或三取代烯反应更快;
- 2)五元和六元环容易形成,而更大环通常需要含杂原子的炔烯链;
- 3)终端炔比内炔反应较慢,但烷基取代的炔能提高产率;
- 4)该反应对酯、酰胺、醚、酮等多种官能团具有良好的耐受性。
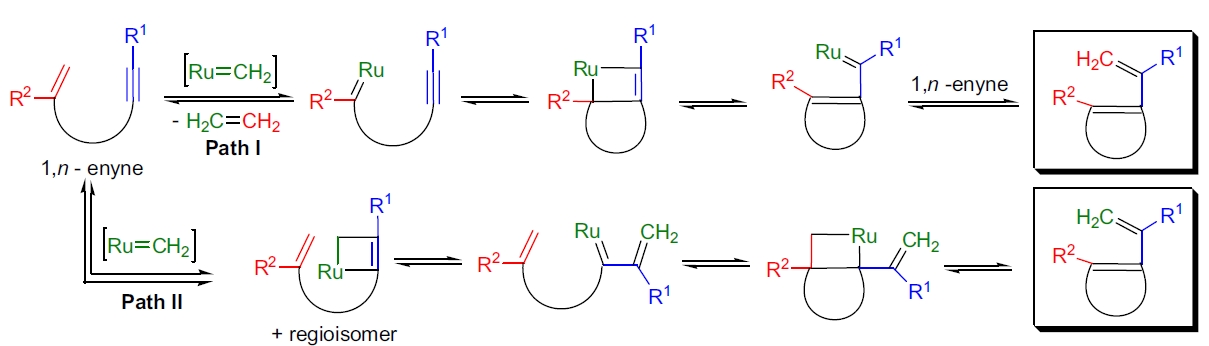
机理34-41
炔烯复分解的具体机制取决于所使用的催化剂。以Grubbs第二代钌卡宾催化剂为例,反应可以沿两条路径进行:路径 I 中,金属卡宾首先与烯烃反应形成金属环丁烷中间体,而路径 II 则是金属卡宾优先与炔烃反应生成金属环丁烯中间体。
合成应用
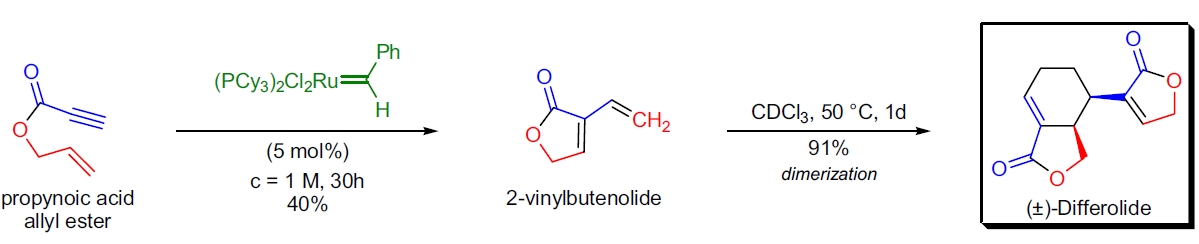
1. (±)-Differolide 的全合成: T.R. Hoye 使用 Grubbs 第一代催化剂在炔酸丙酯上进行环闭炔烯复分解,随后二烯体发生 [4+2] 环加成反应生成天然产物。42
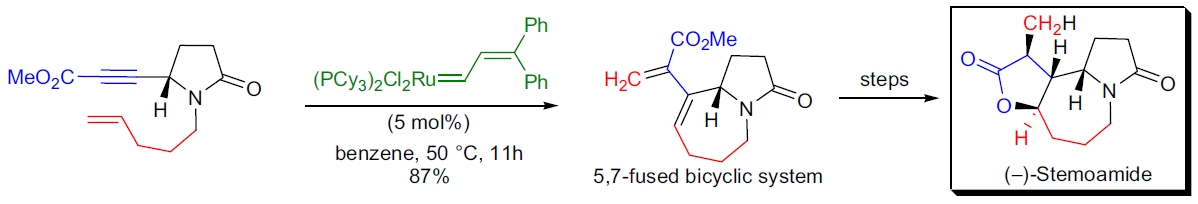
2. (−)-Stemoamide 的合成: M. Mori 实验室使用 5 mol% Grubbs 催化剂在苯中 50°C 下搅拌 11 小时,生成 87% 的5,7-融合双环体系。43
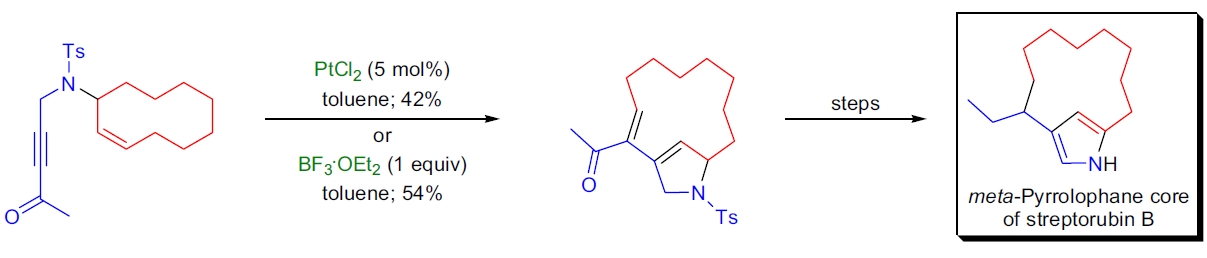
3. Streptorubin B 的形式全合成: A. Fürstner 使用铂和Lewis酸催化的炔烯复分解反应合成meta-吡咯环烷核心,进一步合成目标抗生素。37
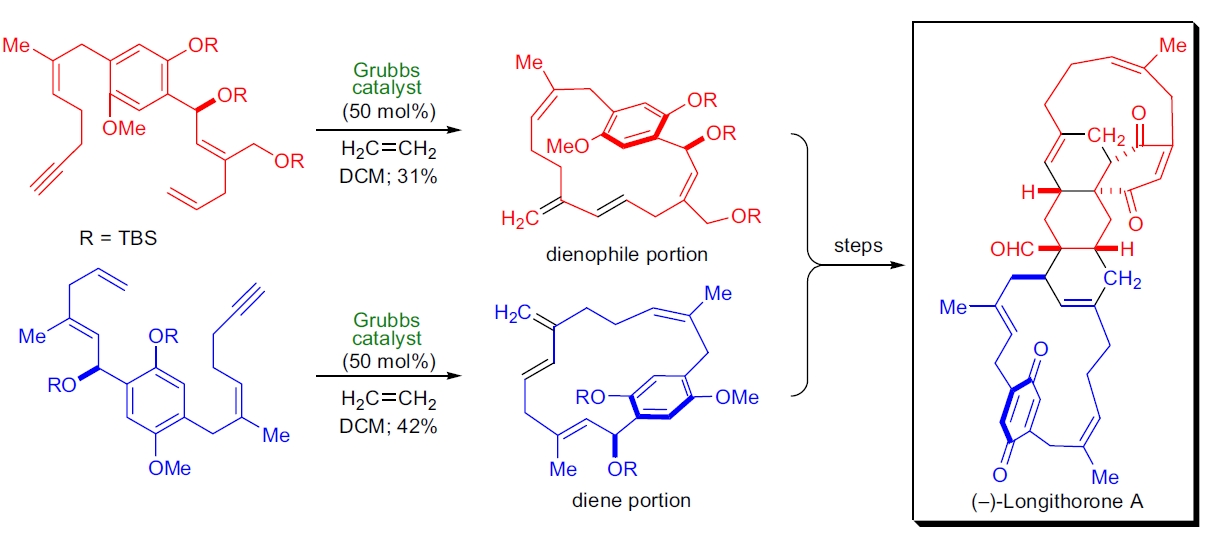
4. (−)-Longithorone A 的生物仿合成: M. Shair 使用 Grubbs 第一代催化剂实现大环化,并通过两次 Diels-Alder 环加成反应合成天然产物。44