Eschenmoser-Claisen 重排
重要性
[开创性文献1,2;综述3,4;改进与优化5]
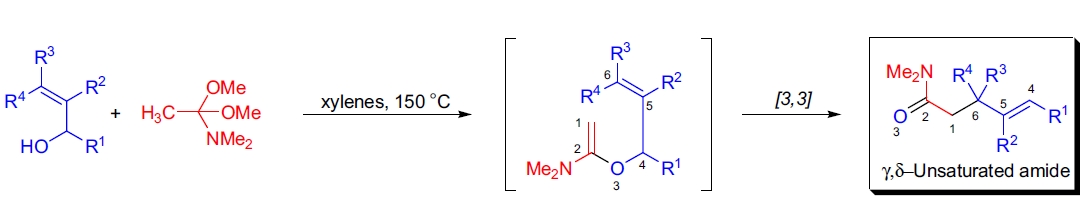
1964年,A. Eschenmoser 报道了一种反应,其中烯丙醇或苄醇与 N,N-二甲基乙酰胺二甲基缩醛在二甲苯中加热后发生类似 Claisen 的重排,生成 γ,δ-不饱和酰胺产物1。该反应具高度立体专一性,并在较低温度(100-150°C)下进行,优于其他变体如 Claisen 和 Johnson-Claisen 重排。对于 2-位取代的烯丙醇,该反应生成三取代烯烃产物,并表现出显著的非对映选择性,这与 Johnson-Claisen 重排一致6。
机理
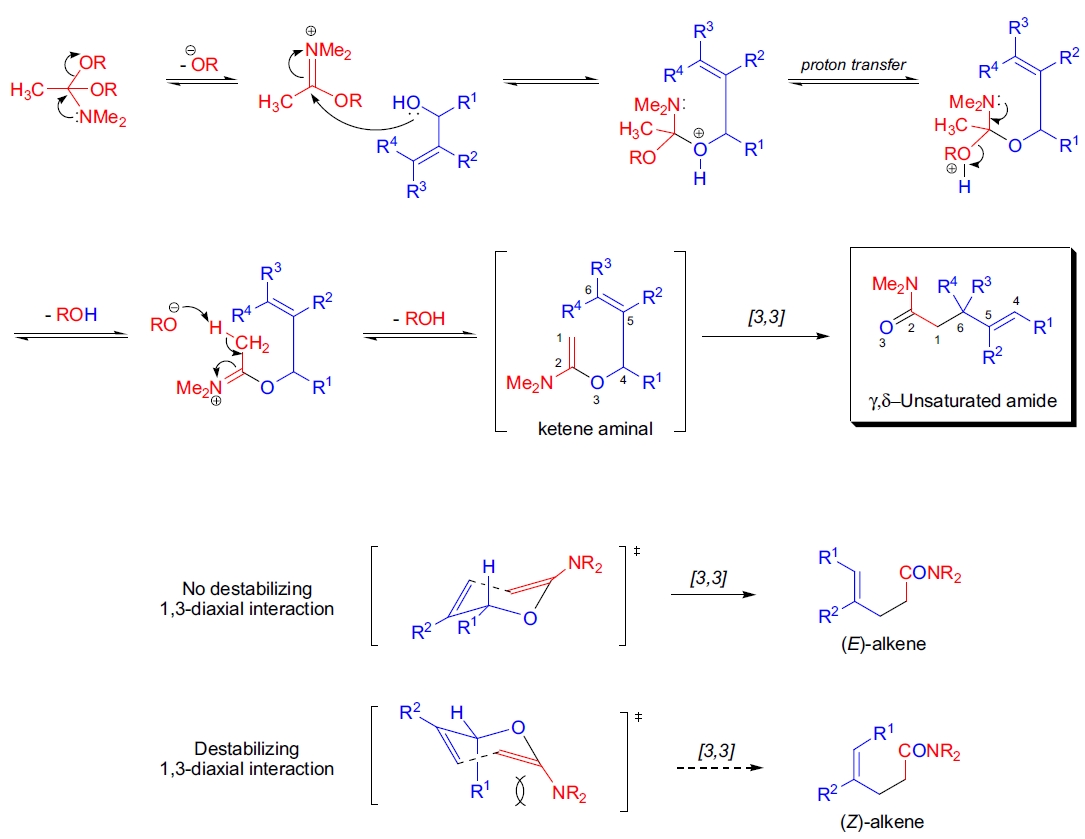
反应不需要酸催化,烯丙醇直接与 N,N-二甲基乙酰胺二甲基缩醛发生醇交换,生成混合缩醛后脱去甲醇形成酮亚胺中间体。在非环体系中,中间体通过类似椅式过渡态发生 [3,3]-σ迁移重排。在某些情况下,由于构象限制,环状体系可能倾向于舟式过渡态。产物的比例取决于过渡态之间的能量差异。一般来说,次级烯丙醇的 Eschenmoser-Claisen 重排由于过渡态中 1,3-轴向相互作用的去稳定化作用,具有很高的 (E)-选择性6。
合成应用
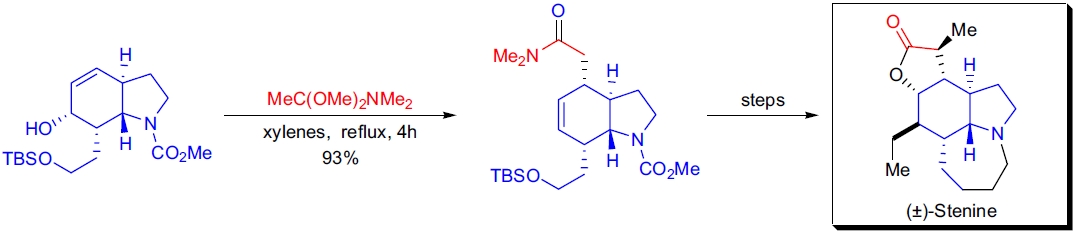
1. (±)-Stenine 的全合成: D.J. Hart 的实验室通过 Eschenmoser-Claisen 重排合成了关键的 γ,δ-不饱和酰胺,反应条件为将烯丙醇前体与 N,N-二甲基乙酰胺二甲基缩醛在二甲苯中回流4小时,产率达93%。7
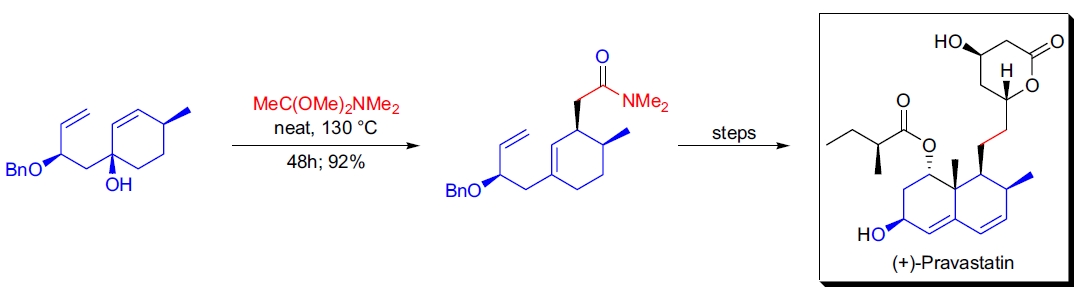
2. (+)-Pravastatin 的全合成: 在 A.R. Daniewski 等人的工作中,Eschenmoser-Claisen 重排被用于引入立体中心。中间体三级醇在 130°C 下与 N,N-二甲基乙酰胺二甲基缩醛反应48小时,副产物甲醇通过蒸馏移除,得到产率为92%的目标酰胺8。
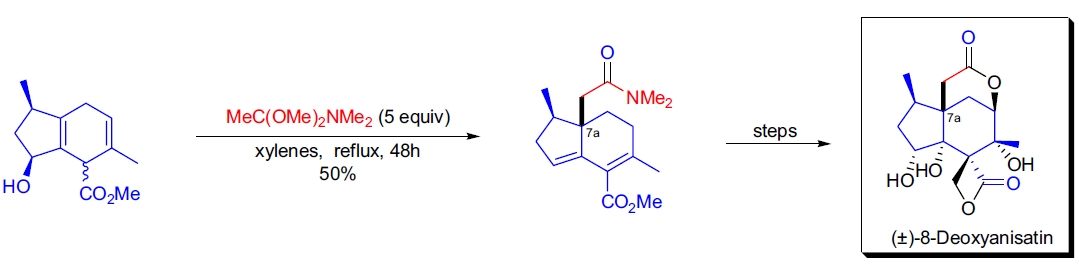
3. Anisatin 的合成: T.P. Loh 等通过 Eschenmoser-Claisen 重排高效构建天然产物 Anisatin 的 C7a 季碳手性中心,随后将生成的酰胺转化为 ε-内酯,从而完成对 (±)-8-Deoxyanisatin 的形式全合成9。
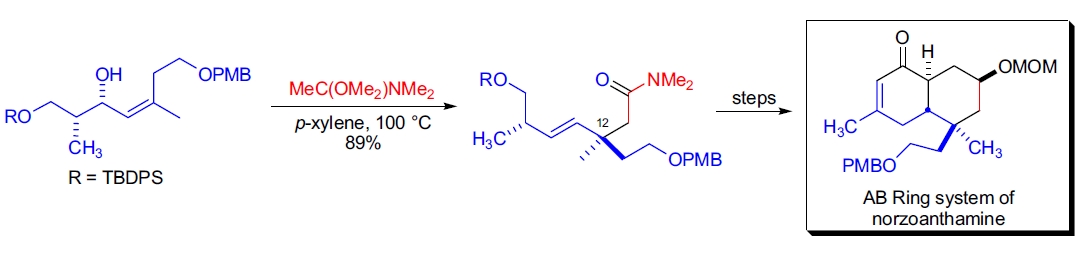
4. Norzoanthamine 的 AB 环合成: D.R. Williams 等通过 Eschenmoser-Claisen 重排引入了关键信息的 C12 季碳立体中心,为后续 Diels-Alder 环化构建 AB 环系提供了合适前体10。