Eschenmoser 亚甲基化反应(Eschenmoser methenylation)
重要性
[开创性文献1;综述2;改进与优化3,4]
通过使用 Eschenmoser 盐([CH2=NMe2]+I−)将 (二甲氨基)甲基基团引入羰基化合物 α-位,随后消除生成相应 α-亚甲基羰基化合物的反应称为 Eschenmoser 亚甲基化反应。1 反应分为两步:第一步为 Mannich 反应的改进形式,羰基化合物与 Eschenmoser 盐反应生成 α-(二甲氨基)甲基羰基化合物;第二步为通过加热、Hofmann 消除、Cope 消除或碱处理实现的消除反应。
机理
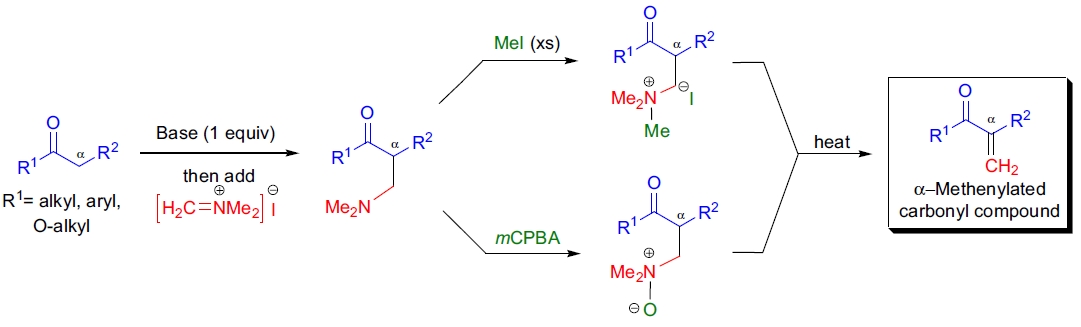
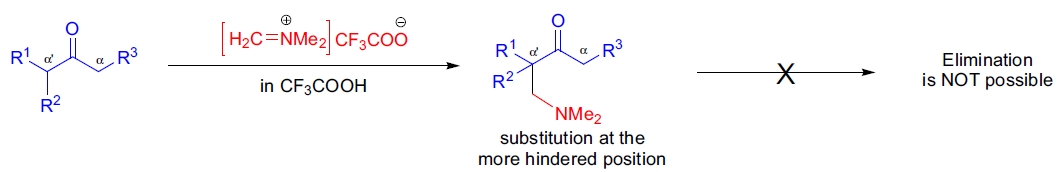
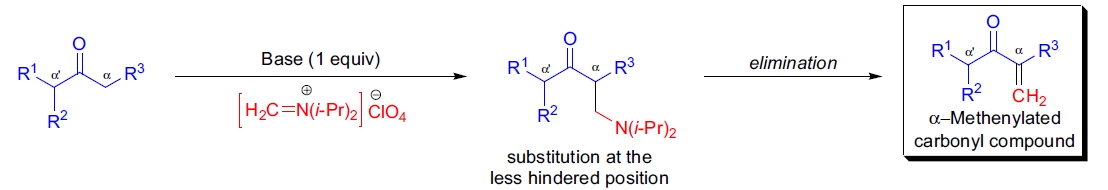
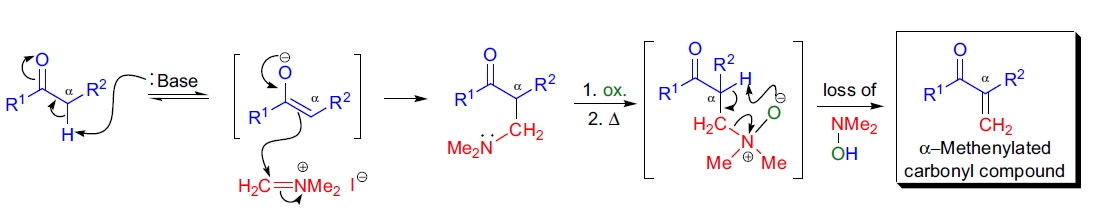
Eschenmoser 亚甲基化反应的第一步是底物在 α-位被去质子化生成烯醇负离子,随后与 Eschenmoser 盐反应生成 α-(二甲氨基)甲基羰基化合物。在第二步中,生成的化合物可通过以下方法消除形成 α-亚甲基羰基化合物:5-7
- 1)加热直接消除;
- 2)生成季铵盐后进行 Hofmann 消除;
- 3)生成 N-氧化物后进行 Cope 消除;
- 4)直接用碱处理。
合成应用
1. Guanacastepene 的合成中间体: S.J. Danishefsky 利用 Eschenmoser 亚甲基化反应在 hydroazulenone 上引入 exo-亚甲基,作为 Guanacastepene 合成的关键步骤。6

2. CP-263,114 的核心合成: J.L. Wood 实验室使用一锅法在五元内酯环上引入 exo-亚甲基,方便后续自由基环化反应的进行。7

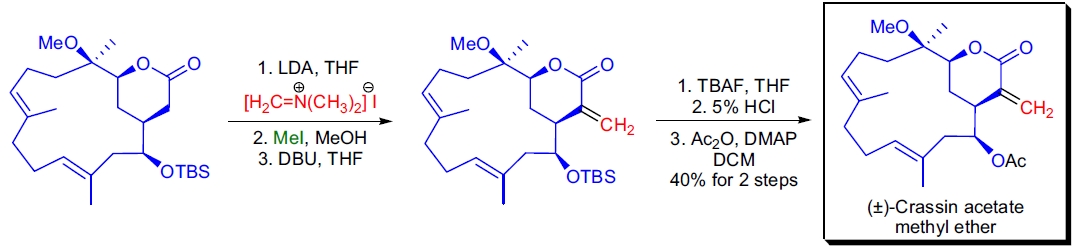
3. (±)-Crassin acetate methyl ether 的全合成: W.G. Dauben 等人在全合成的后期使用 Eschenmoser 亚甲基化反应在六元内酯环上引入敏感的 α-亚甲基基团。8
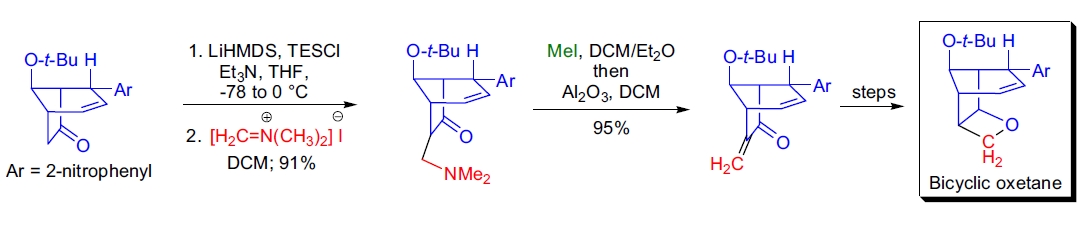
4. (±)-Gelsemine 的合成: 在 S.J. Danishefsky 的工作中,Eschenmoser 亚甲基化反应被用于制备关键的双环 α-亚甲基酮中间体,后续反应生成 oxetane。9