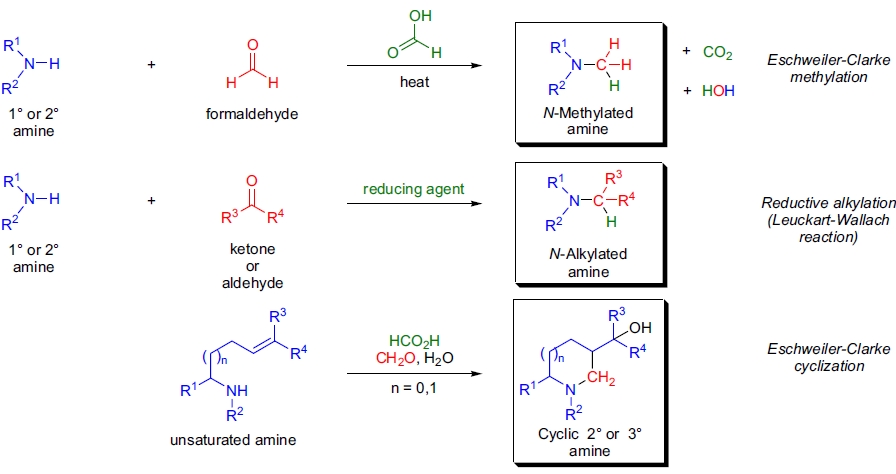
Eschweiler-Clarke 甲基化
还原烷基化(reductive alkylation)
重要性
[开创性文献1-4;综述5-7;改进与优化8-13]
Eschweiler-Clarke 甲基化是一种将伯胺或仲胺一锅还原甲基化为相应叔胺的方法。该反应属于胺的碳基化合物(醛和酮)还原烷基化,视为 Leuckart-Wallach 反应的改进形式14。早在 1885 年,R. Leuckart 首次报道了胺的还原烷基化,随后 Wallach 等对其进行了扩展研究15,16。1905 年,W. Eschweiler 和 1933 年 H.T. Clarke 分别展示了甲醛和甲酸的组合可以将伯胺和仲胺转化为叔胺1,2。
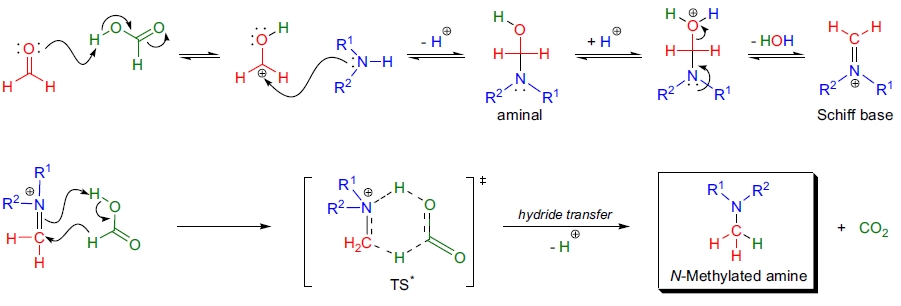
机理
Eschweiler-Clarke 甲基化的机理涉及以下步骤:1)甲醛和起始胺通过氨基醇(缩醛)中间体形成亚胺(Schiff 碱);2)还原剂(如甲酸、氰硼氢化钠等)将亚胺还原为 N-甲基胺,同时释放二氧化碳;3)对于伯胺,步骤 1 和 2 重复一次21-26,13。
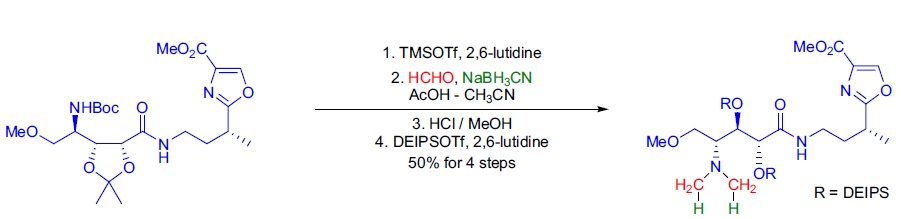
合成应用
1. (–)-Calyculin A 和 B 的全合成: A.B. Smith 团队利用改进的 Eschweiler-Clarke 甲基化将复杂的伯胺转化为相应的 N,N-二甲基胺衍生物27。先用 TMSOTf 去保护 N-Boc 伯胺,再用 HCHO/NaBH3CN 在 AcOH/CH3CN 溶剂中甲基化。随后去除乙缩醛保护基,并硅基化生成目标分子。
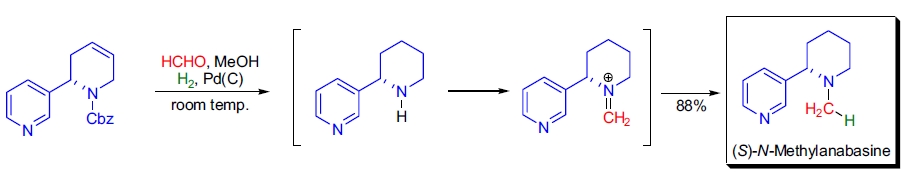
2. (S)-N-甲基阿那巴斯碱的全合成: J. Lebreton 等人在全合成末步骤中使用了一锅 Cbz 去保护-氢化-Eschweiler-Clarke 甲基化法20。用 HCHO/MeOH/Pd(C)/H2 体系在室温下处理底物,总收率为 88%。
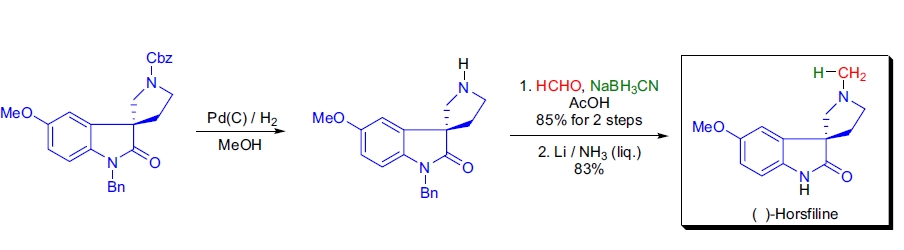
3. (–)-Horsfiline 的合成: 在 K. Fuji 团队的研究中,Eschweiler-Clarke 甲基化被用于五元环仲胺的 N-甲基化28。尽管原始条件(HCO2H/HCHO/回流)导致四级立体中心的消旋化,但改用氰硼氢化钠为还原剂后,保留了光学活性。
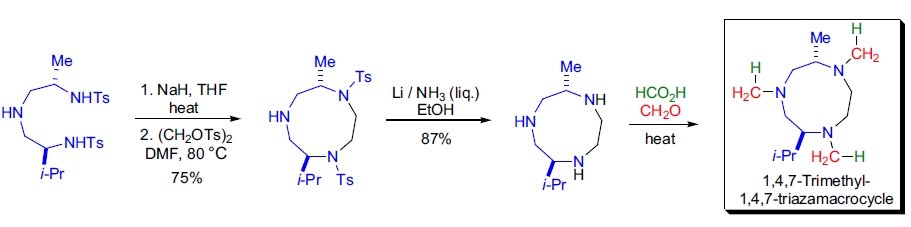
4. 环状催化剂的合成: C.L. Gibson 等人合成了手性 2,6-二取代 1,4,7-三甲基-1,4,7-三氮杂大环分子,用于稳定高氧化态的过渡金属29。末步骤使用了经典 Eschweiler-Clarke 甲基化条件完成三氮的 N-甲基化。