Evans 羟醛反应
重要性
[开创性文献1;综述2-10;改进与优化11-22;理论研究23-28]
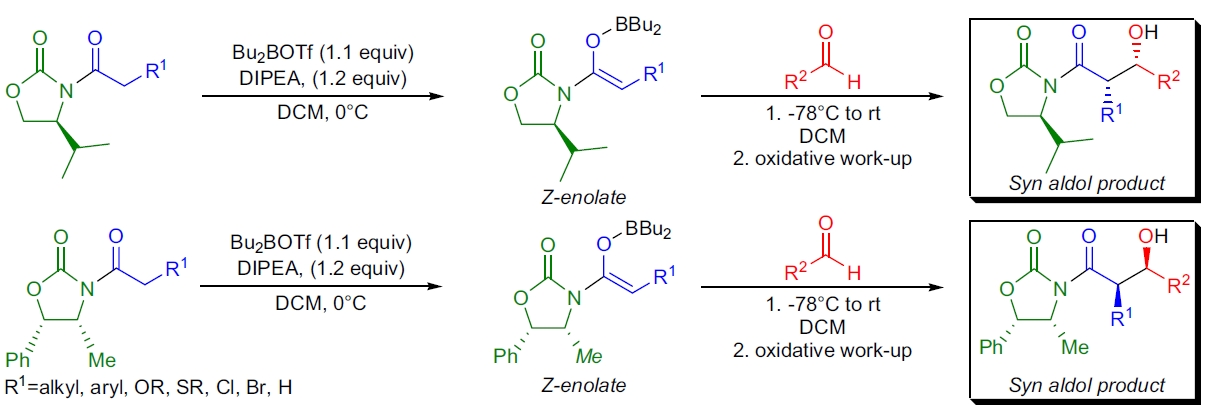
硼介导的羟醛反应是一种用于高立体选择性碳-碳键形成的强大方法。此过程的高非对映选择性可归因于硼烯醇负离子中相对较短的硼-氧键长(1.36-1.47 Å),29 其与醛反应时会形成紧密的六元椅式过渡态。用 (Z)-硼烯醇负离子与醛反应可得到 syn 羟醛产物,而 (E)-硼烯醇负离子可高非对映选择性地形成 anti 羟醛产物。30,31 通过在烯醇组分中应用共价连接的手性助剂,可以实现绝对立体化学的控制。D.A Evans 及其同事开发了一对基于噁唑烷酮的手性助剂,这些助剂可以从 (S)-缬氨醇和 (1S,2R)-去氧肾上腺素中以优异的对映纯度获得。1
- 1)在标准条件下对 N-酰基噁唑烷酮进行烯醇化(1.1 等摩尔 Bu2BOTf,1.2 等摩尔二异丙胺,0 °C,30 分钟)可获得 (Z)-烯醇负离子,选择性优异;
- 2)所得的 (Z)-硼烯醇负离子与多种醛的羟醛反应以极高的非对映选择性和对映选择性生成 syn 羟醛产物;
- 3)当使用手性醛时,烯醇负离子的面偏好性会覆盖醛的 π-面选择性;
- 4)从 N-乙酰噁唑烷酮(R1=H)衍生的硼烯醇负离子的羟醛反应提供低立体选择性的产物,但通过在 α-位引入含杂原子的取代基(如硫烷基组,R1=SR)可以克服这一问题,并可通过还原性去除;
- 5)存在几种非破坏性去除和回收手性助剂的方法:水解和酯交换(LiOH, LiOOH, LiOR, LiSEt),33-35 还原性去除(LiAlH4),33,36 和转胺化为 Weinreb 酰胺(Me(OMe)NH, Me3Al)。37
除了羟醛反应外,Evans 手性助剂还成功应用于烯醇负离子烷基化、33 酰化、33 胺化、38-41 和羟基化42 等过程中。
机理2
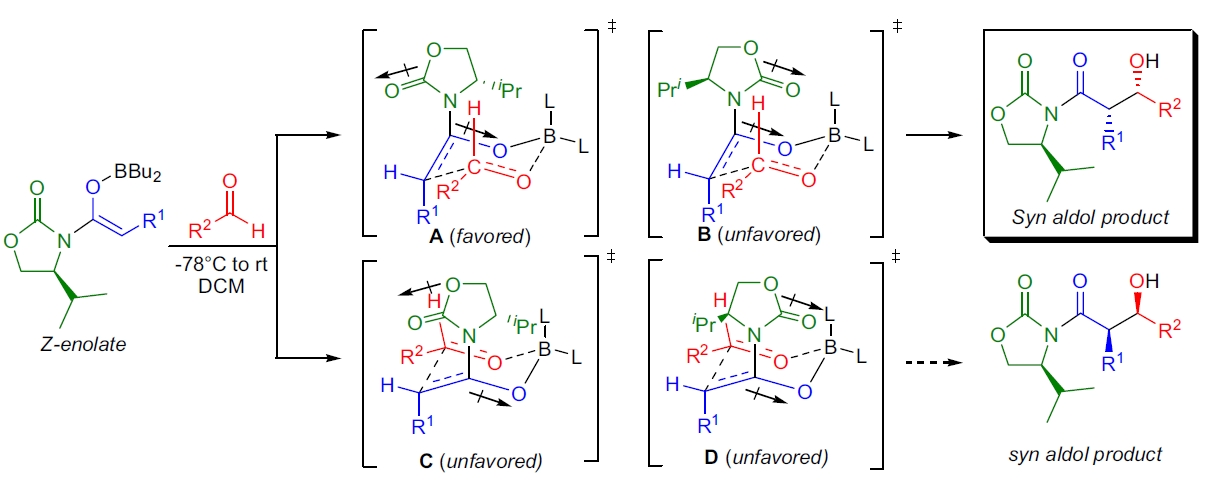
Evans 羟醛反应中观察到的立体选择性可以通过 Zimmerman-Traxler 过渡态模型来解释。
合成应用
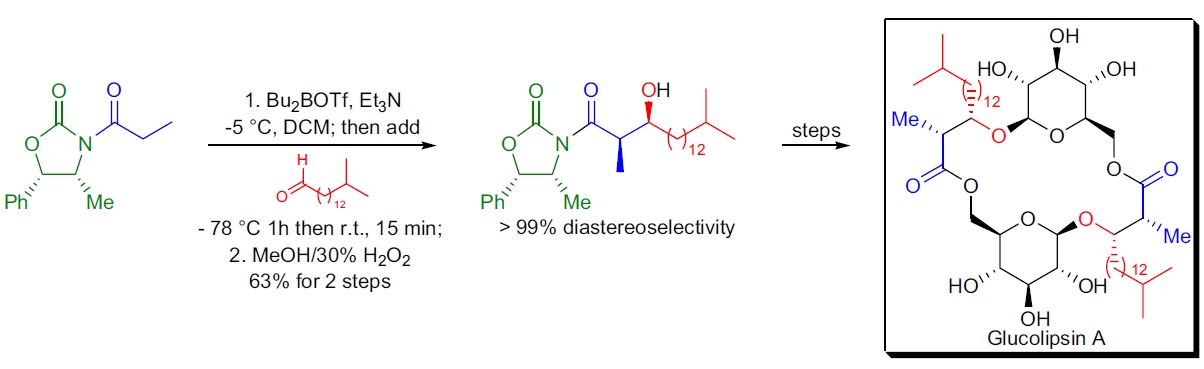
1. 糖脂 Glucolipsin A 的立体化学确认:A. Fürstner 等利用 Evans 羟醛反应确认了天然产物的绝对立体化学。43
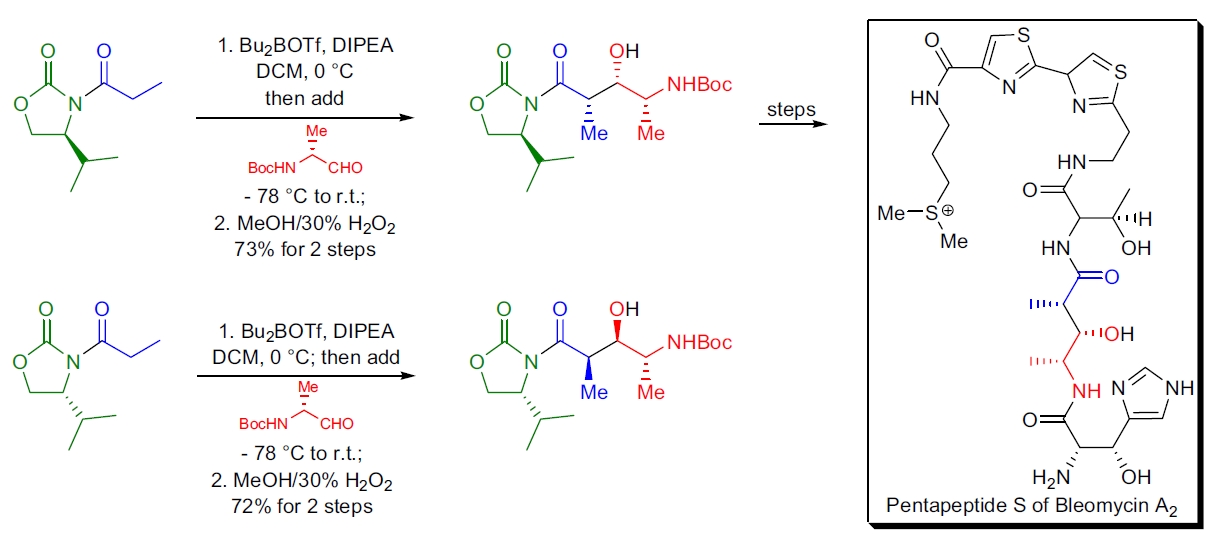
2. 博来霉素 A2 的全合成:D.L. Boger 等设计了用于天然产物三肽和五肽亚单元的高效合成方法,关键步骤为 Evans 羟醛反应。44,45
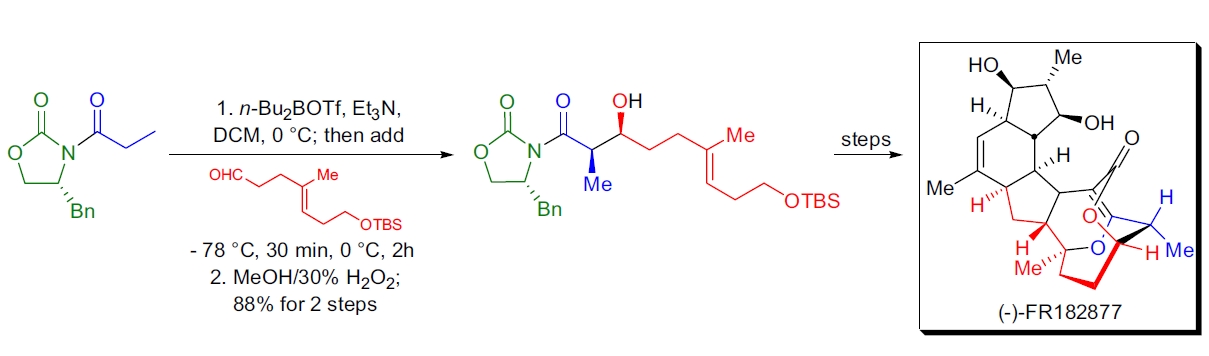
3. 细胞毒性天然产物 (–)-FR182877 的不对称全合成:D.A. Evans 和团队使用硼介导的羟醛反应生成 syn 羟醛产物,建立了关键的绝对立体化学。46,47