Favorskii 重排
重要性
[开创性文献1,2;综述3-8;改进与优化9-12;理论研究13,14]
α-卤代酮(具有至少一个α-氢)在碱和亲核试剂(如醇、胺或水)存在下进行处理时,会通过环丙酮中间体发生骨架重排,生成羧酸或羧酸衍生物(酯或酰胺)。该反应称为 Favorskii 重排,广泛用于高支化羧酸的合成。卤素取代基可以是氯、溴或碘,而碱通常是烷氧化物或氢氧化物。在重排过程中,脂肪族 α-卤代酮生成脂肪族羧酸衍生物,而环状 α-卤代酮底物发生环缩反应,生成比原环少一个碳的环状羧酸衍生物。15,16,12
- 1)对结构因子(如取代基体积、烷基取代程度)和反应条件(碱、溶剂、温度)敏感;
- 2)卤素所在碳上的烷基或芳基取代会加速重排;
- 3)在环状 α-卤代酮中,重排适用于 6-10元环;
- 4)产率从中等到较高不等。
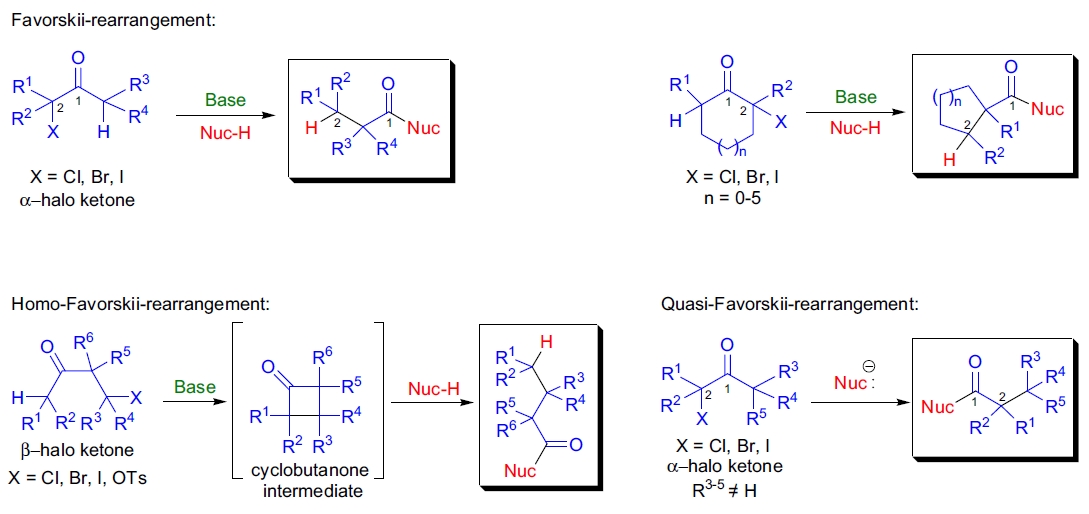
Favorskii 重排的两种重要变体是:
- 1)当 β-卤代酮在碱和亲核试剂存在下处理时,通过环丁酮中间体发生同系 Favorskii 重排;20,21
- 2)如果 α-卤代酮没有可烯醇化的氢(R3-5≠H),则会发生准 Favorskii 重排。
机理22-26
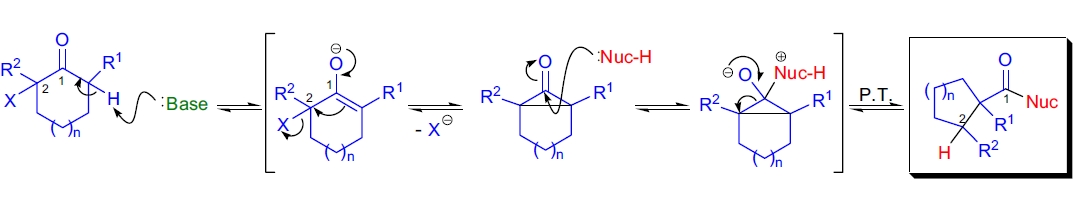
目前被广泛接受的 Favorskii 重排机制包括以下步骤:
- 在 α-碳处去质子化形成烯醇负离子;
- 烯醇负离子对含离去基的 α’-碳进行分子内进攻,生成环丙酮中间体;
- 中间体的区域选择性开环生成最稳定的碳负离子;
- 碳负离子接受质子转移生成产物。
合成应用
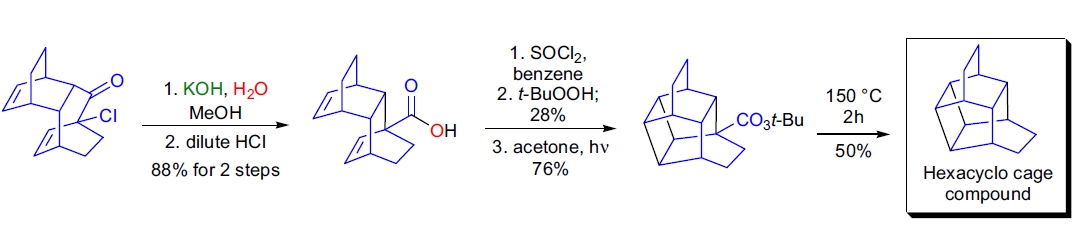
1. 六环笼状化合物的全合成:H. Takeshita 的实验室利用连续的 Diels-Alder 环加成、Favorskii 重排和 [2π+2π] 光环加成作为关键步骤,实现了对六环笼状化合物 hexacyclo[6.4.2.02,7.03,11.06,10.09,12]tetradecene 的全合成。32
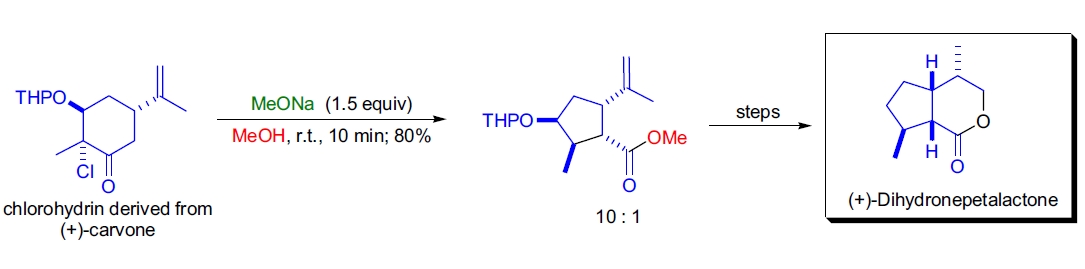
2. (+)-二氢荆芥内酯的合成:E. Lee 等人展示了从 (+)-香茅酮衍生的氯醇经过立体选择性的 Favorskii 重排生成高度取代的环戊烷羧酸衍生物。33
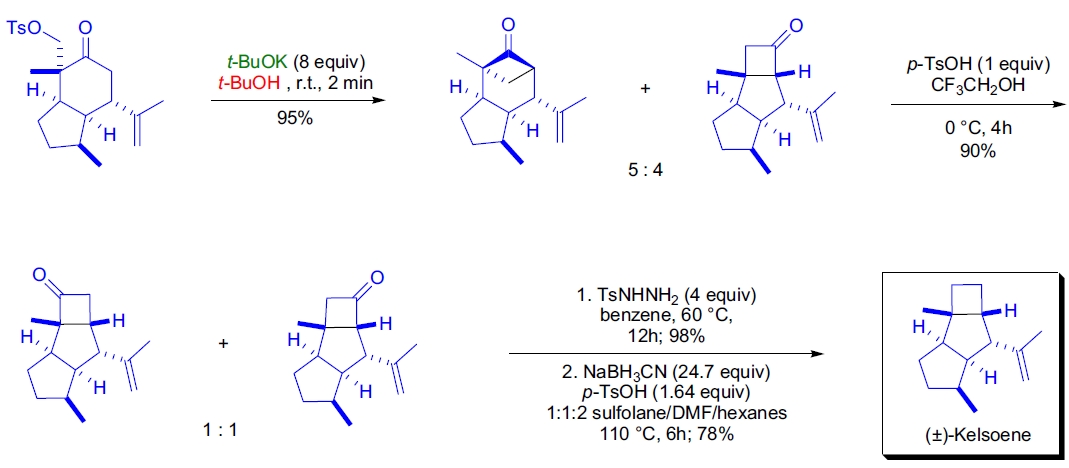
3. (±)-kelsoene 的立体控制全合成:M. Koreeda 等人通过 γ-酮对甲苯磺酸酯的碱催化同系 Favorskii 重排实现了目标分子的 4-5 融合环部分的合成。34