Ferrier 反应/重排
重要性
[开创性文献1,2;综述3-8;改进与优化9-24]
不饱和碳水化合物在路易斯酸催化下的重排被称为 Ferrier 反应/重排。1914年,E. Fischer 首次报道了三-O-乙酰基-D-葡萄糖苷在加热水时发生烯丙位重排生成相应的 2,3-不饱和半缩醛的现象。1,25
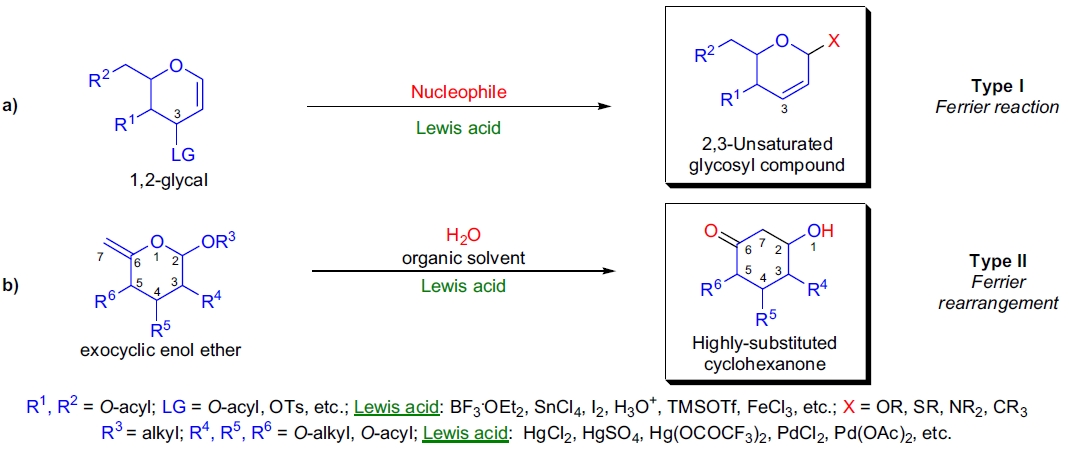
1960年代初,R.J. Ferrier 发现了该反应的合成价值,他成功地通过 1,2-糖苷与亲核试剂(如醇、硫醇、胺)在路易斯酸催化下制备 O-、S-、N-连接的不饱和糖苷化合物。这种反应被称为 Ferrier I 型反应,其特点包括:
- 1)3 位具有良好离去基团(例如酰氧基)的底物在强亲核试剂(如醇和酚)存在下,即使没有催化剂也可以加热完成重排;
- 2)常用的路易斯酸包括 BF3·OEt2、SnCl4、I2、FeCl3、TMSOTf-AgClO4 等;21-24
- 3)在 Mitsunobu 反应条件下,3 位的羟基可以被活化而无需使用路易斯酸或质子酸;20
- 4)2,3-不饱和糖苷产物的苷中心立体化学取决于起始物中 3 和 4 位基团的相对立体化学,但 α-苷通常占主导。
1979年,首次报道了将外环烯醚转化为取代环己酮的 Ferrier II 型重排,该反应在汞(II)盐存在下进行。5 Ferrier II 型重排的特点包括:
- 1)底物可通过碳水化合物容易制备,能合成手性、高取代环己酮衍生物;
- 2)大多数反应中,可分离单一非对映异构体并获得高产率;
- 3)路易斯酸可以以催化量使用,可合成具有酸敏感官能团的复杂目标化合物。
研究表明,3 位基团与 β 位新生成羟基的立体化学之间具有强相关性:产物中这些基团通常呈反式分布。
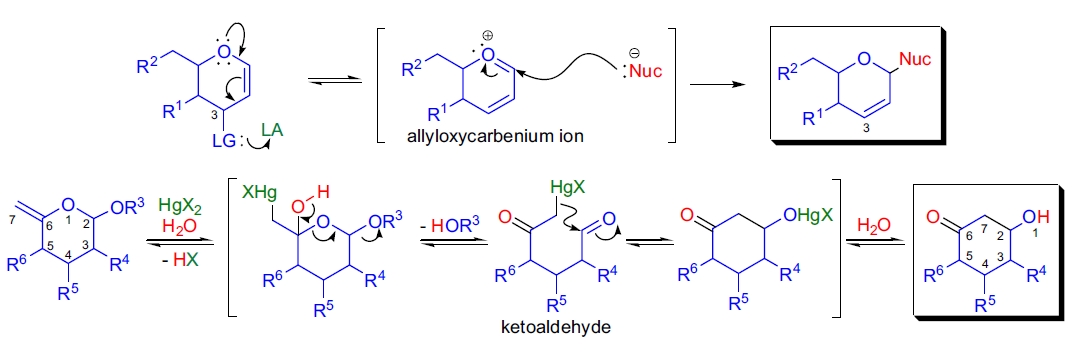
机理27-33,15
在 Ferrier I 型反应中,第一步为在路易斯酸作用下,3 位离去基团离去生成烯氧基碳正离子。随后,亲核试剂捕获该碳正离子生成相应糖苷。在 Ferrier II 型重排中,烯醚首先发生区域专一的羟基汞化生成酮醛中间体。然后该中间体通过 Aldol 类分子内环化生成产物环己酮。
合成应用
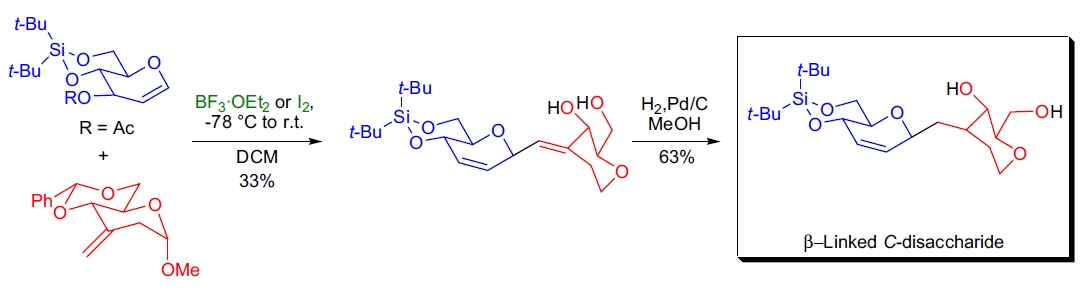
1. C-糖二糖的合成:H.M.I. Osborn 的研究表明,使用环己烯衍生物作为亲核试剂在路易斯酸介导的 Ferrier I 型反应中可以合成不饱和 β-连接的 C-糖二糖。34
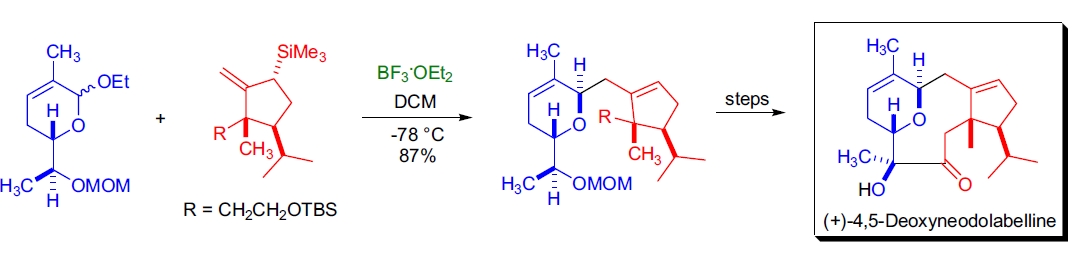
2. (+)-4,5-脱氧新杜拉贝林的全合成:D.R. Williams 等人利用 Ferrier I 型反应构建了关键的反式-2,6-二取代二氢吡喃,立体选择性完全。35
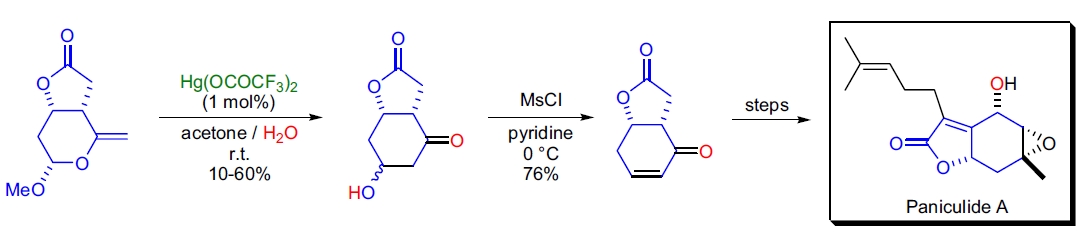
3. Paniculide A 的合成:N. Chida 等人利用 Ferrier II 型重排构建了该天然产物的取代环己烷亚基。36
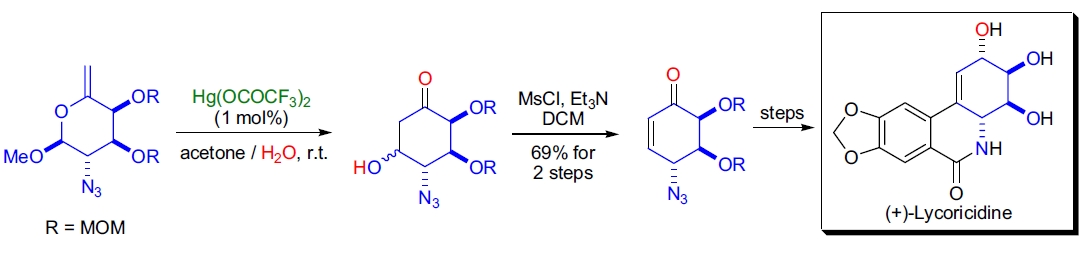
4. (+)-Lycoricidine 的全合成:S. Ogawa 等人通过催化 Ferrier II 型重排合成了光学活性的取代环己烯酮片段。37