Finkelstein 反应
重要性
[开创性文献1;综述2-10;改进与优化3-9;理论研究10-14]
烷基卤化物中的卤素原子与另一种卤素原子进行平衡交换的反应被称为 Finkelstein 反应。最早的卤素交换反应例子是由 W.H. Perkin 在19世纪中期报道的15,但系统研究是在1910年由 H. Finkelstein 开展的。1
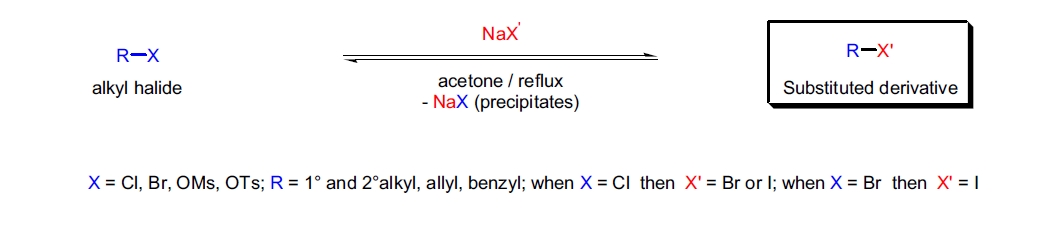
Finkelstein 观察到,当各种烷基氯化物和溴化物(1°, 2°, 3°, 苄基等)在丙酮中与15 wt% NaI 溶液一起煮沸时,相应的烷基碘化物以较高产率生成。他还注意到反应时间差异很大,伯、烯丙基和苄基卤化物反应时间最短,而叔烷基卤化物时间最长。Finkelstein 反应是一个平衡过程,利用钠盐在有机溶剂(如丙酮、2-丁酮)中溶解度的显著差异。15,16
- 1)NaI 在丙酮中溶解度高,而 NaBr 和 NaCl 在有机溶剂中的溶解度非常低。
- 2)根据勒夏特列原理,生成的 NaBr 和 NaCl 从溶液中沉淀出来,从而将平衡推动至卤素交换方向。
- 3)该反应广泛用于将烷基溴化物、氯化物、对甲苯磺酸酯和甲磺酸酯转化为相应的烷基碘化物,而这些碘化物通常难以通过其他方法制备。
此外,其他卤化化合物(如 α-卤代酮和酸)也可容易地发生 Finkelstein 反应。以下是一些改进方法:
- 1)固相支持 KI 避免了试剂的过量使用;5
- 2)高压微波辐射显著提高了反应速度;6,8
- 3)脂溶性季铵盐氟化物(TBAF)可以在低极性非质子溶剂中将其他烷基卤化物转化为烷基氟化物;7
- 4)KF/18-冠-6 在极性非质子溶剂中的应用;16
- 5)使用 TMSI 可以置换烷基氟化物中的氟原子;4
- 6)用 NaI/CS2 在路易斯酸(如 AlMe3, ZnCl2, FeCl3)存在下可将位阻较大的二级和三级烷基卤化物转化为烷基碘化物。3
机理17-27
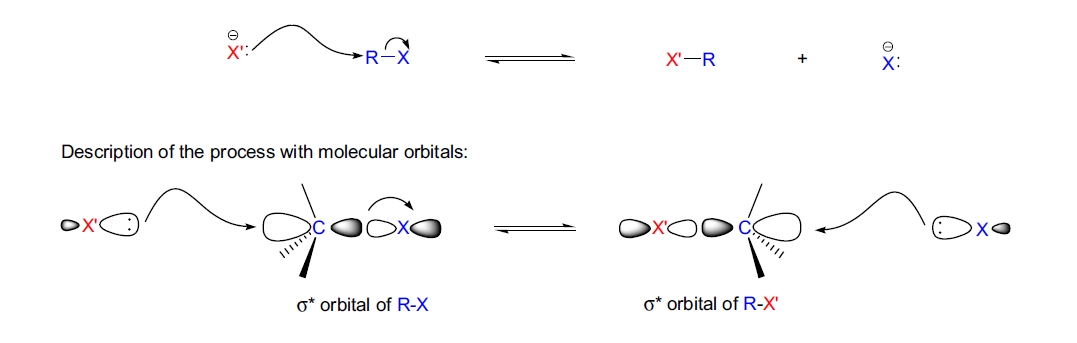
Finkelstein 反应的机理通常被描述为典型的 SN2 反应,其中亲核试剂(卤离子)的充满轨道与碳-卤键的σ*轨道相互作用,反应以构型反转进行。17-27 此机理适用于大多数涉及伯、仲烷基、烯丙基或苄基卤化物的转化。
合成应用
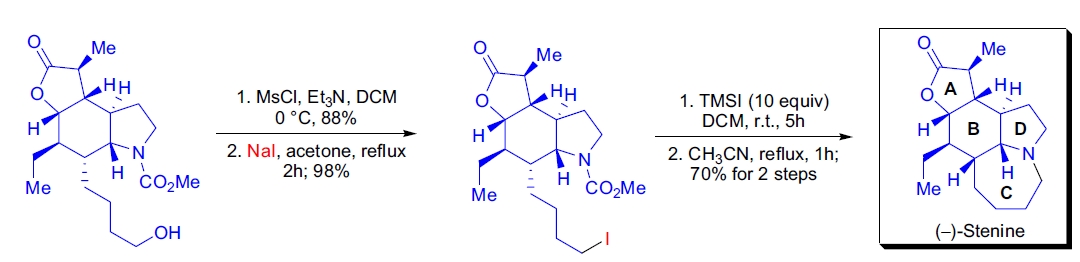
1. (−)-Stenine 的全合成:Y. Morimoto 等人在(−)-Stenine 全合成的最后阶段利用 Finkelstein 反应将伯烷基甲磺酸酯转化为伯烷基碘化物。28
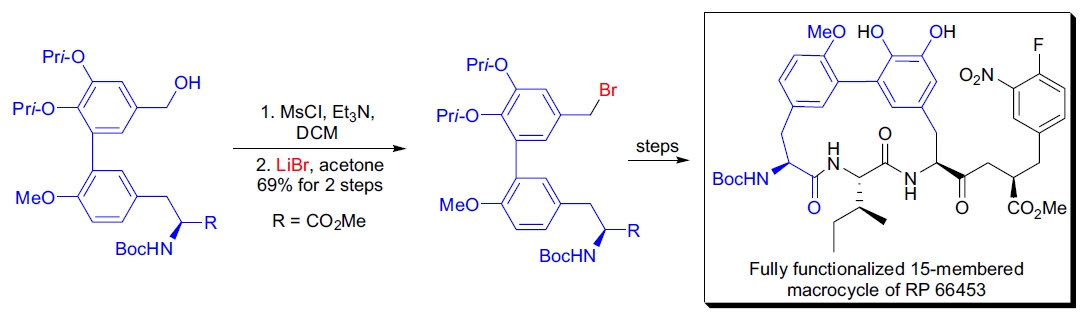
2. RP 66453 的 15 元大环的合成:J. Zhu 实验室通过 Finkelstein 反应制备了复杂的双芳基苄基溴化物,用于 Corey 对甘氨酸模板的手性烷基化。29
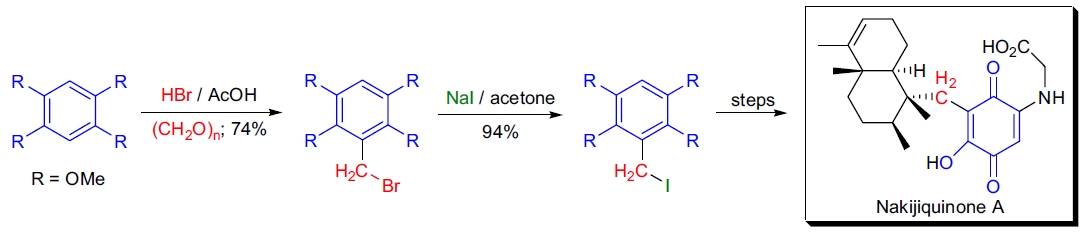
3. Nakijiquinones 的合成:H. Waldmann 等人通过两步法使用 Finkelstein 反应制备了四甲氧基苯基碘化物,用于还原烷基化步骤。30
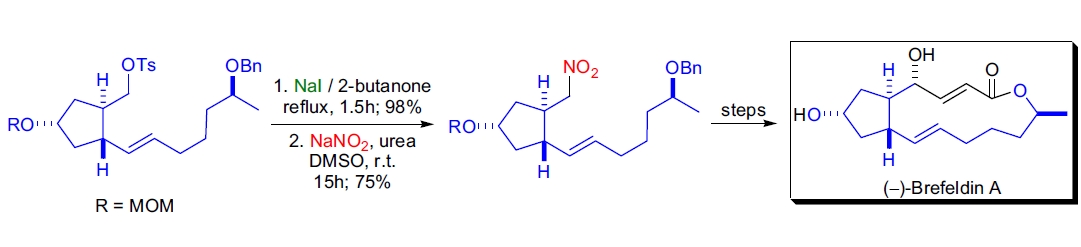
4. (−)-Brefeldin A 的全合成:D. Kim 等人通过双 Finkelstein 反应制备了用于环加成底物的烷基硝基化合物。31