Fischer 吲哚合成
重要性
[开创性文献1,2;综述3-9;改进与优化10-13;理论研究14-21]
1883年,E. Fischer 和 F. Jourdan1 将丙酮酸1-甲基苯基肼与醇性氯化氢反应,产物后来被确定为1-甲基吲哚-2-羧酸。2 通过加热酮或醛的芳基肼在质子酸或路易斯酸催化剂存在下制备吲哚的反应被称为 Fischer 吲哚合成。自发现以来,该反应成为制备取代吲哚最重要的方法。
成功催化吲哚化的催化剂包括:
- 1)强酸(如 PTSA, PPA, HCl, H2SO4);
- 2)弱酸(如吡啶盐酸盐,醋酸);
- 3)固体酸(如蒙脱石 KSF 黏土,沸石 Y,离子交换树脂);
- 4)路易斯酸(如 PCl3, 聚磷酸三甲硅酯,ZnCl2)。
路易斯酸催化的反应通常在较温和条件下(室温而非高温)进行。对于杂芳基肼,酸的使用存在问题(因杂原子的质子化),这些化合物在高温下简单加热(热非催化方法)也可导致吲哚化。
Fischer 吲哚合成的主要特点:
- 1)无需分离芳基肼,可通过将醛与肼混合一锅完成吲哚化;
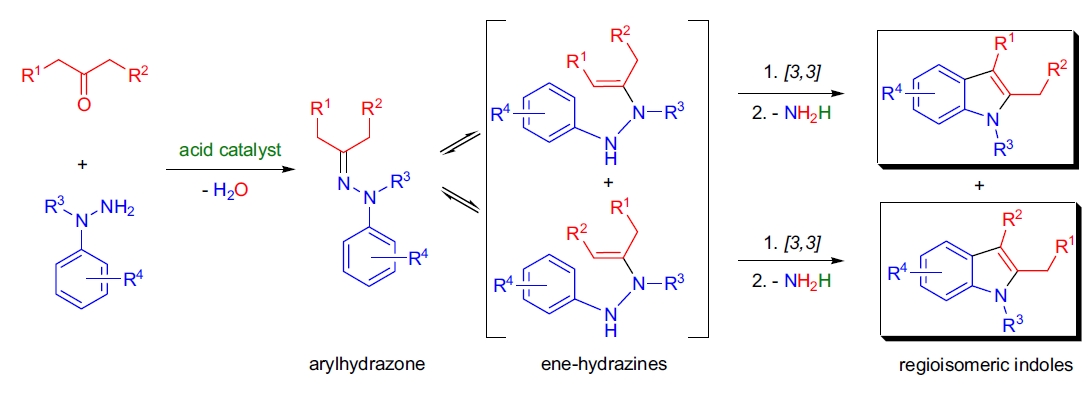
- 2)不对称酮产生两个区域异构的2,3-二取代吲哚,其区域选择性取决于多种因素;
- 3)α,β-不饱和酮的吲哚化通常失败,因为会生成惰性吡唑啉;
- 4)1,2-二酮可生成单吲哚和双吲哚,通常强酸催化剂在回流醇中形成单吲哚;
- 5)1,3-二酮和β-酮酯不是理想底物;
- 6)醛通常以保护形式使用;
- 7)肼通常以其 HCl 盐或 Boc 保护形式使用;
- 8)芳基肼上的电子吸收取代基使吲哚化的收率低且速率慢;
- 9)邻位取代的芳基肼反应通常比间位取代的慢;
- 10)Japp-Klingemann 反应是获得芳基肼的一种简单方法。
机理22-39
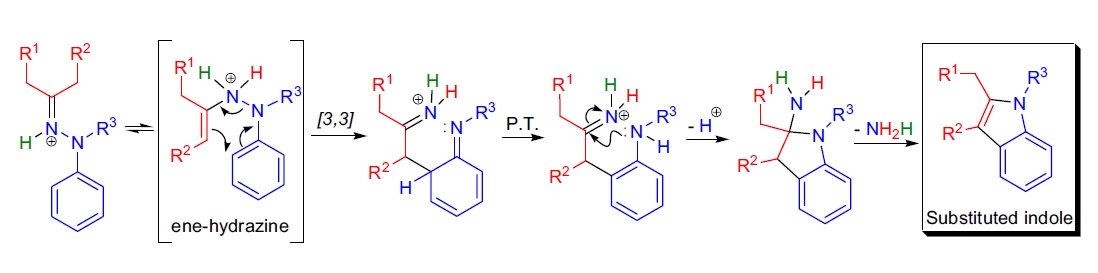
目前接受的 Fischer 吲哚合成机理最初由 R. Robinson 在1924年提出。22 该机理包括以下五个步骤:
- 路易斯酸(如质子)与亚胺氮配位;
- 肼酮互变异构为相应的烯肼;
- 通过 [3,3]-σ迁移中断芳环;
- 通过质子转移重新芳香化,并通过有利的 5-exo-trig 环化形成五元环;
- 失去一分子氨生成吲哚系统。
合成应用
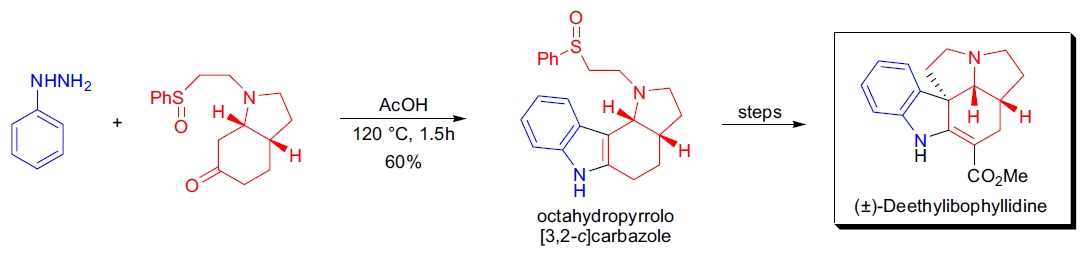
1. (±)-Deethylibophyllidine 的全合成:J. Bonjoch 等人应用一种区域选择性的 Fischer 吲哚合成作为关键步骤,合成了八氢吡咯并[3,2-c]咔唑。40
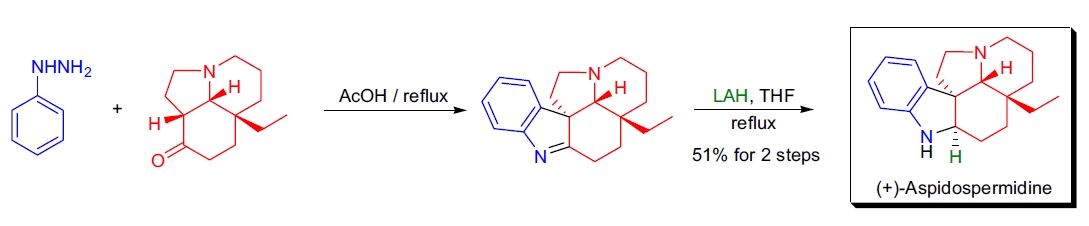
2. (+)-Aspidospermidine 的全合成:J. Aubé 等人在最后步骤中对复杂的三环酮进行了高效的 Fischer 吲哚化。41
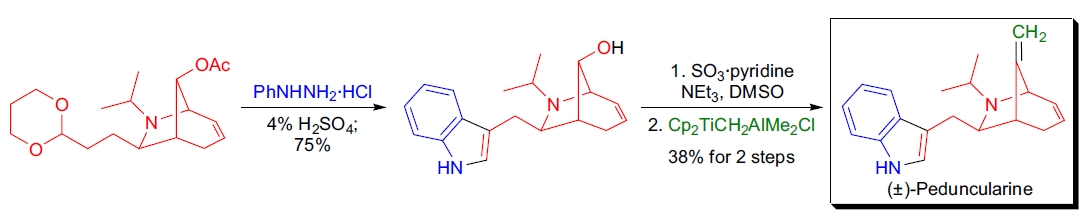
3. (±)-Peduncularine 的全合成:K.A. Woerpel 等人使用 Fischer 吲哚合成完成了其6-氮杂双环结构的合成。42
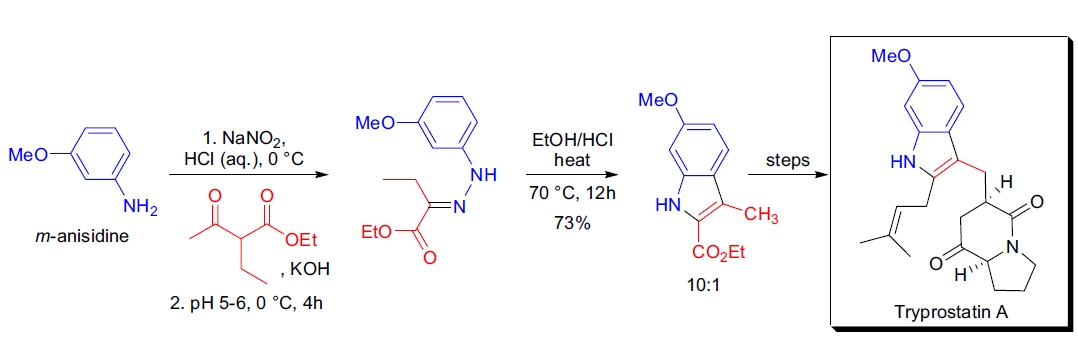
4. Tryprostatin A 的全合成:J.M. Cook 等人通过 Japp-Klingemann 反应制备必要的芳基肼酮,随后应用 Fischer 吲哚合成完成了关键步骤。43