Fries 重排反应
重要性
[开创性文献1-4;综述5-14;改进与优化15-31;理论研究32-38]
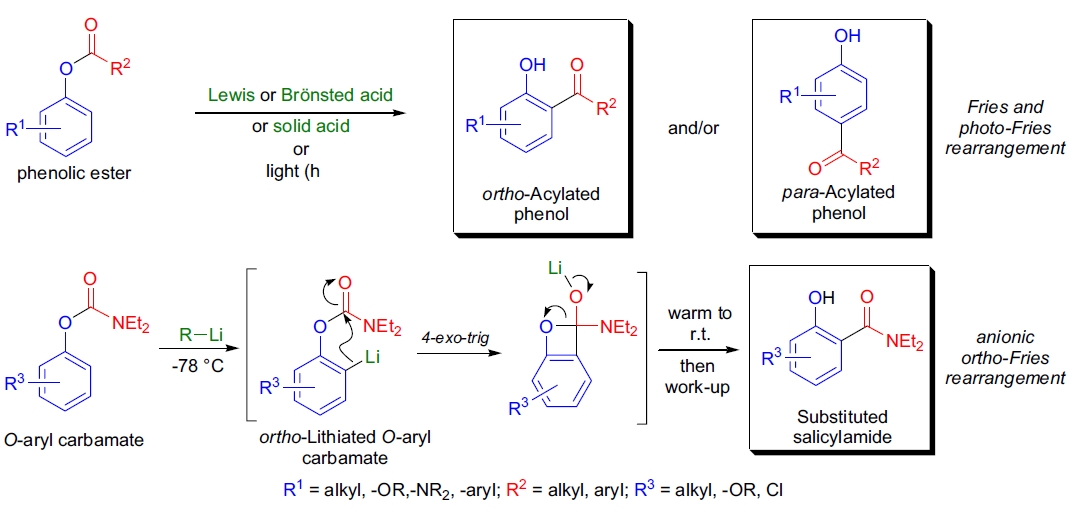
20 世纪初,K. Fries 和同事用氯化铝处理乙酸和氯乙酸的酚酯,分离得到了邻位和对位的乙酰酚和氯乙酰酚混合物。3,4 文献报道了类似的 Lewis 酸催化重排反应,甚至可以追溯到 19 世纪晚期,1,2 但 Fries 认识到这一现象在酚酯中具有普遍性,因此这种反应以他的名字命名。Fries 重排反应的特点如下:
- 1)通常需要在高温(80-180 °C)下进行,并至少使用 1 个当量的 Lewis 酸或 Brönsted 酸(如 HF、HClO4、PPA)。
- 2)反应时间从几分钟到数小时不等。
- 3)Friedel-Crafts 酰化的 Lewis 酸催化剂均适用,而近来固体酸催化剂(如沸石)和金属三氟甲磺酸盐也被使用。12,30
- 4)酚酯中的酚和酸部分可以有多种结构变化,重排具有普遍性。
- 5)酚上的电子给体取代基提高产率,而电子吸引基显著降低产率甚至不反应。
- 6)多烷基取代的酚在反应条件下经常发生烷基迁移。
机理39-49
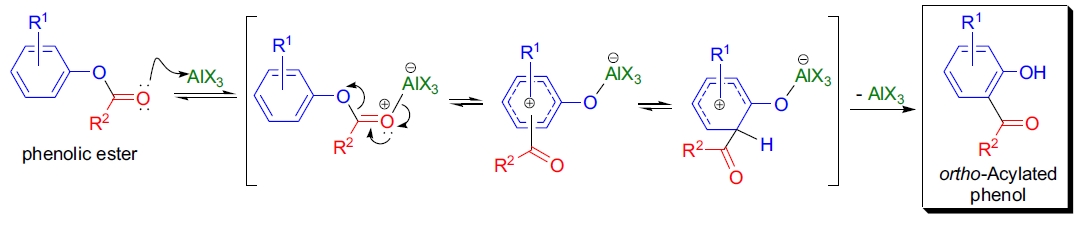
Fries 重排反应通过离子中间体进行,但其具体的机理路径(分子内或分子间)仍存在争议。许多文献为两种路径都提供了证据,而具体路径取决于底物结构和反应条件。该图展示了使用氯化铝催化剂时,酚酯生成邻位酰化酚的路径。
合成应用
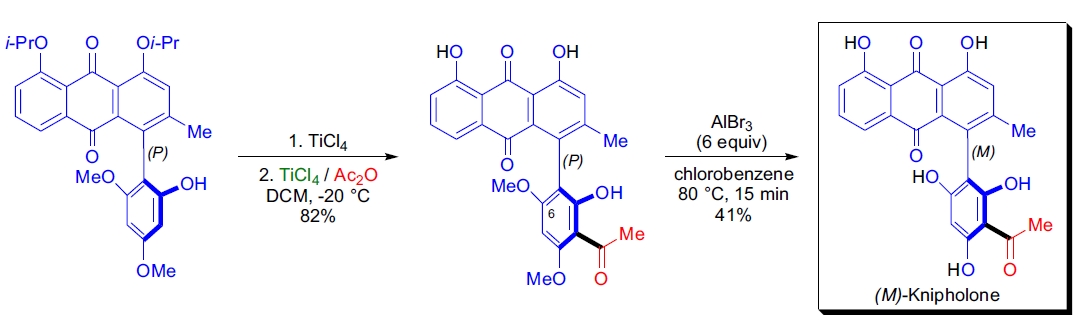
1. G. Bringmann 等首次报道了手性选择性苯基蒽醌天然产物(M)-knipholone 的全合成。51 在合成的后期阶段,需要在温和条件下引入乙酰基。将取代的蒽醌先用 TiCl4 去保护后,再用 Ac2O 和 TiCl4 酰化,随后的 Fries 重排反应高产率地生成邻位酰化产物。通过 AlBr3 选择性去甲基化后获得目标天然产物。
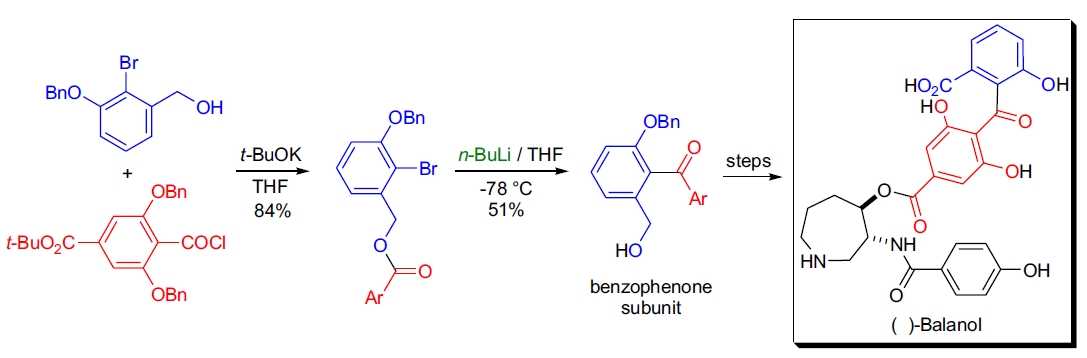
2. J.W. Lampe 等人在合成蛋白激酶 C 抑制剂(–)-balanol 时,利用了阴离子 homo-Fries 重排反应合成了空间阻碍大的二苯甲酮亚基。52 首先用三取代苯甲酰氯酰化 2-溴-3-苄氧基苄醇,生成酯前体(84% 产率)。然后用 n-BuLi 在 -78 °C 下进行金属-卤交换,快速生成亚芳基锂,并通过阴离子 homo-Fries 重排反应生成目标化合物。
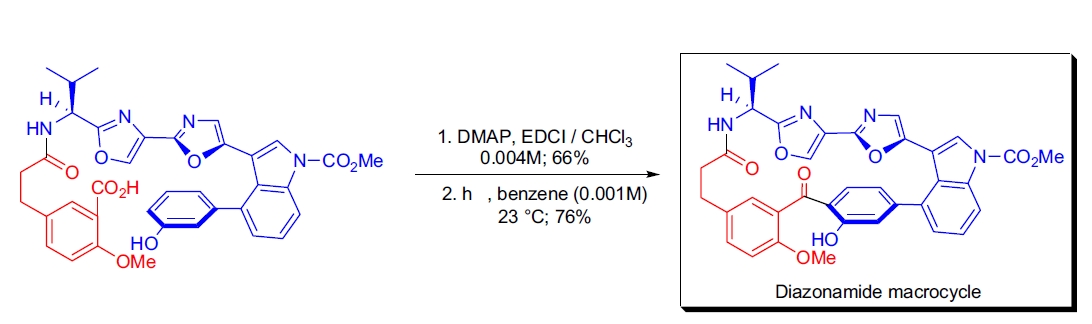
3. P. Magnus 的研究显示,光-Fries 重排反应可用于合成 diazonamide 的大环骨架。53 首先用 EDCI 将芳基羧酸和酚耦合形成酚酯大环内酯,再在高稀释条件下经光照反应生成 ortho 酰化的酚大环骨架。