Gabriel 合成法
重要性
[开创性文献1;综述2-4;改进与优化5-16]
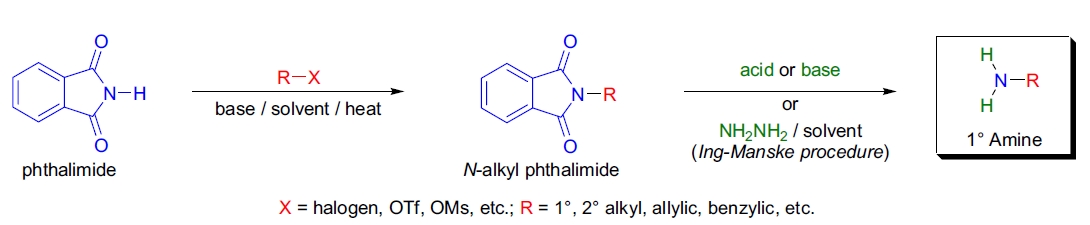
通过两步温和方法从相应的烷基卤化物制备伯胺的过程,其中首先对邻苯二甲酰亚胺钾进行烷基化,然后将生成的N-烷基邻苯二甲酰亚胺进行水解,被称为加布里埃尔合成。最早在1884年报告了使用简单烷基卤化物对邻苯二甲酰亚胺进行烷基化的反应,但直到1887年,S. Gabriel 才认识到这一过程的普适性,并提出了合成伯胺的两步法。该烷基化反应可以在无溶剂或有溶剂的条件下进行。最优溶剂为DMF(适用于SN2反应),但DMSO、HMPA、氯苯、乙腈和乙二醇也可使用。
以下烷基化试剂在制备所需的N-烷基邻苯二甲酰亚胺时表现出良好到优异的收率:
- 1. 立体无阻的1°和2°烷基卤化物效果最佳,其中碘化物反应性最高(I > Br > Cl),其次为烯丙基、苄基和炔丙基卤化物;
- 2. 烷基磺酸酯(如甲磺酸酯、对甲苯磺酸酯)通常比烷基卤化物收率更高且更易获得;
- 3. α-卤代酮、酯、腈和β-酮酯(如二溴代丙二酸二乙酯);
- 4. O-烷基异脲;
- 5. 烷氧基和烷基硫基膦鎓盐;
- 6. 在Mitsunobu反应条件(DEAD/Ph₃P/邻苯二甲酰亚胺)下,1°和2°醇;
- 7. 带有多个电子吸引基的芳基卤化物(通过SNAr反应制备1°芳胺);
- 8. 在Cu(I)催化剂存在下的芳基卤化物;
- 9. 环氧化物和氮杂环丙烷(用于制备氨基醇和二胺);
- 10. α,β-不饱和化合物在邻苯二甲酰亚胺阴离子的作用下发生Michael加成。
原始的加布里埃尔合成存在以下限制,限制了其广泛应用:
- 1. 在无溶剂条件下,邻苯二甲酰亚胺钾和烷基卤化物需要高温(120-240°C),热敏底物无法使用;
- 2. 水解通常在高温下用强酸(如H₂SO₄、HBr、HI)进行,因此不适用于含酸敏感基团的底物;
- 3. 强碱性水解法同样与碱敏感基团不兼容。
1926年,H.R. Ing 和 R.H.F. Manske 提出了改进方法,即在回流乙醇中使用水合肼裂解N-烷基邻苯二甲酰亚胺,在温和中性条件下进行(Ing-Manske方法)。过去一个世纪中,原始方法还进行了以下改进:
- 1. 开发新的加布里埃尔试剂(用其他氮源替代邻苯二甲酰亚胺)以实现更温和的脱保护条件;
- 2. 在邻苯二甲酰亚胺钾与烷基卤化物的反应混合物中添加催化量的冠醚或穴醚,几乎达到定量产率;
- 3. 在异丙醇中使用NaBH₄以实现超温和的邻苯二甲酰亚胺裂解。
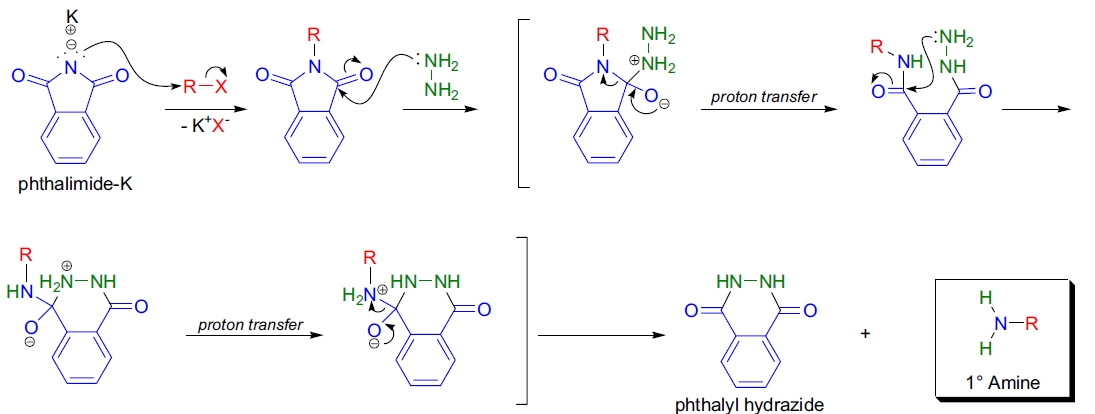
机理2,15
Gabriel 合成的第一步是邻苯二甲酰亚胺钾与卤代烷的烷基化,遵循 SN2 机理。第二步是 N-烷基邻苯二甲酰亚胺的肼解,通过肼与邻苯二甲酰亚胺的一个羰基的亲核加成反应实现。随后发生开环、质子转移、分子内 SNAc 反应、另一次质子转移,最终四面体中间体分解生成目标伯胺和副产物邻苯二甲酰肼。
合成应用
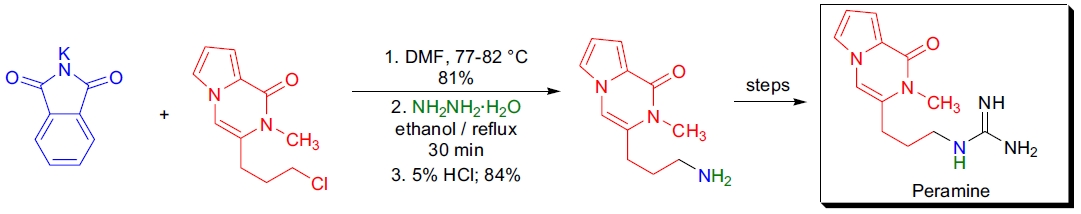
1. D.J. Dumas 在 du Pont 实验室完成了昆虫摄食抑制剂 peramine 的全合成。25 在合成的最后步骤中,使用 Gabriel 合成法。将伯烷基氯化物在 77-82 °C 下用邻苯二甲酰亚胺钾和 DMF 反应 1.5 小时。生成的 N-烷基邻苯二甲酰亚胺通过 Ing-Manske 方法高产率地裂解。
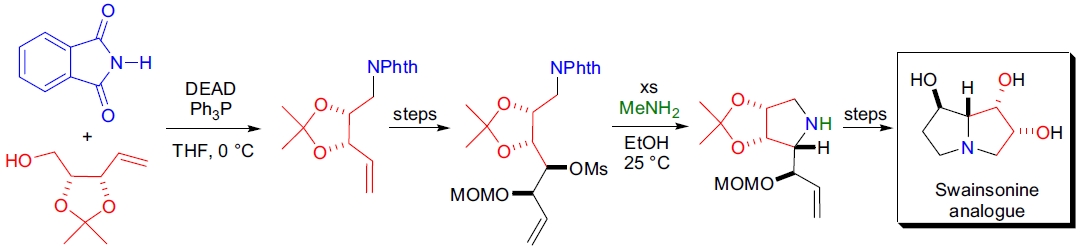
2. 在 swainsonine 和 castanospermine 的类似物(氨基糖)合成中,K. Burgess 等人使用 Mitsunobu 反应条件将伯羟基转化为邻苯二甲酰亚胺。26 在几个步骤中携带邻苯二甲酰基,但由于生成的二酰亚胺显著氢化了末端烯烃,肼解步骤被甲胺取代,干净地得到脱保护的伯胺。
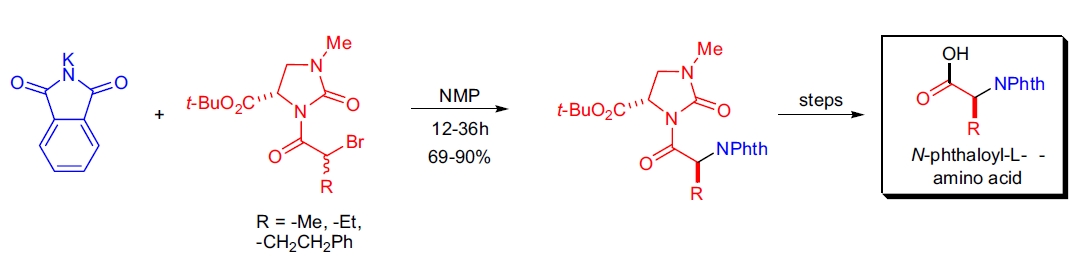
3. K. Nunami 等人利用动态动力学拆分技术高立体选择性地完成了 Gabriel 合成 α-氨基酸。27 底物叔丁基-(4S)-1-甲基-3-2-(溴代酰基)-2-氧代咪唑烷-4-羧酸叔丁酯在室温下与邻苯二甲酰亚胺钾反应,仅得到一种非对映异构体且收率良好。拆除手性辅基后得到 N-邻苯二甲酰基-L-α-氨基酸。
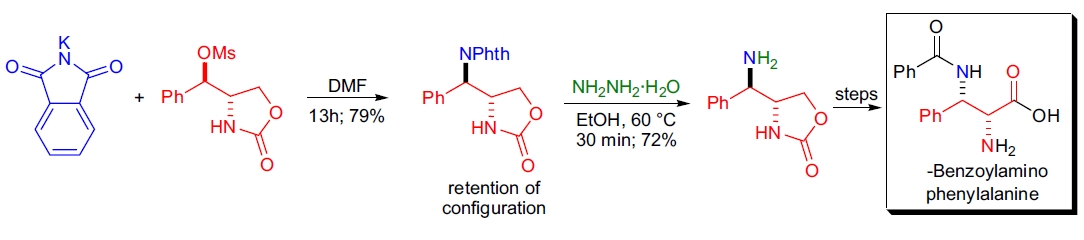
4. F.M. Rossi 等人研究了以对映选择性方式制备邻二胺的方法,并完成了 taxol 侧链类似物 α-苯甲酰氨基-苯丙氨酸的合成。28 研究表明,对映纯的恶唑烷酮中的仲醇被甲磺酸化后与邻苯二甲酰亚胺钾反应。由于邻苯二甲酰亚胺氮原子的邻基参与,配置呈净保留。