Gattermann-Koch 醛基化反应
重要性
[开创性文献1-3;综述4-8;改进与优化9-16]
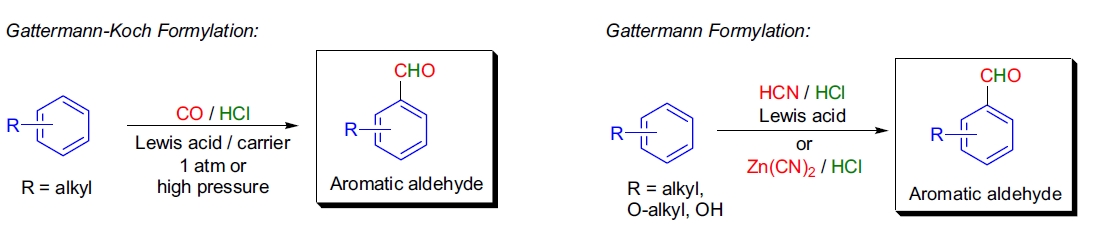
在 1897 年,L. Gattermann 和 J.A. Koch 成功地使用甲酰氯 (HCOCl) 作为酰化试剂,在 Friedel-Crafts 酰基化条件下将甲酰基 (CHO) 引入到甲苯中。1 尽管研究人员无法单独制备甲酰氯,他们假设通过一氧化碳 (CO) 和氯化氢 (HCl) 的反应可以在体系内原位生成甲酰氯,并在 AlCl3-Cu2Cl2 催化下实现芳环的醛基化反应。这种通过 CO/HCl/Lewis 酸催化剂(如 AlX3, FeX3,X = Cl, Br, I)将甲酰基引入到富电子芳环中的方法被称为 Gattermann-Koch 醛基化反应。
Gattermann-Koch 醛基化反应具有以下一般特征:
- 1)在常压下,活性芳香化合物(如烷基苯)可以作为底物使用;
- 2)在高压 CO(100-250 atm)条件下,反应速率显著增加,甚至非活性芳香化合物(如氯苯和苯)也可以被醛基化;
- 3)带有间位定位基(电子吸收基团)的非活性芳香化合物无法通过此法进行醛基化;
- 4)在常压下需要催化剂的载体/活化剂(如 Cu2Cl2, TiCl4, NiCl2),但在高压下则无需活化剂;
- 5)催化剂的用量和纯度非常重要,通常需要一个当量的催化剂;
- 6)单取代底物几乎只在对位被醛基化,但当底物中已有对位取代基时,甲酰基会引入到邻位;
- 7)与 Friedel-Crafts 反应类似,高度烷基化芳香底物会发生烷基迁移;
- 8)由于需要高压,这种方法主要用于工业应用。
Gattermann-Koch 反应在适用底物范围方面有所局限,主要用于烷基苯类化合物。Gattermann 引入了一种改进方法,即将 HCN 与 HCl 混合,并在 ZnCl2 存在下对苯酚、酚类醚和杂芳香化合物(如吡咯和吲哚)进行醛基化。这种改进方法被称为 Gattermann 醛基化反应或 Gattermann 合成法。2,3
Gattermann 醛基化的主要缺点是需要使用无水 HCN,这是一种非常有毒的化合物。为了避免处理 HCN,R. Adams 通过反应 Zn(CN)2 和 HCl,在芳香底物存在下原位生成 HCN 和 ZnCl2(Adams 改进法)。10 这种方法自此成为有机合成中最广泛使用的变体。其他改进方法成功使用了 NaCN 和 CNBr 代替 HCN。9 两种反应的一个严重限制是无法用于芳香胺的醛基化,因为会发生许多副反应。
合成应用
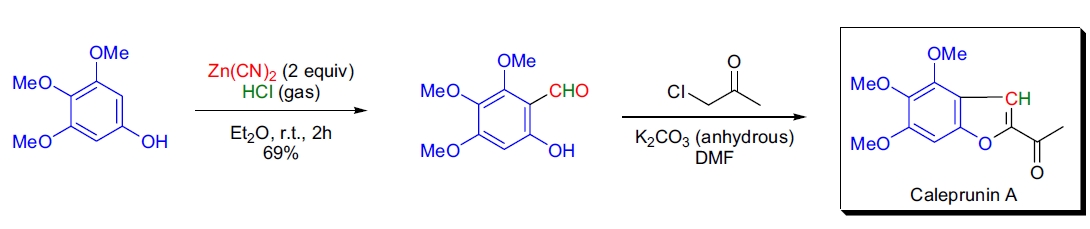
1. R. Stevenson 等人利用 Gattermann 醛基化法合成了苯并呋喃类天然产物 caleprunin A。24 起始原料 3,4,5-三甲氧基苯酚与 Zn(CN)2 在乙醚中反应,同时通入干燥的 HCl 气体。所得苯甲醛衍生物进一步与氯丙酮在 DMF 中反应,产物通过无水 K2CO3 催化生成。
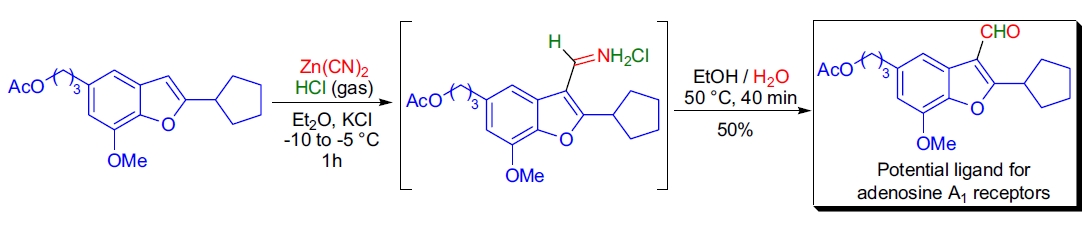
2. H.N.C. Wong 等人使用 Gattermann 醛基化的 Adams 改进法,在 2,5-二烷基-7-甲氧基苯并呋喃的 C3 位置成功引入甲酰基。25 在 Zn(CN)2 存在下,于 -10°C 条件下通入 HCl 气体反应 1 小时。生成的亚胺盐酸盐随后用水-乙醇混合溶液水解,获得目标化合物。
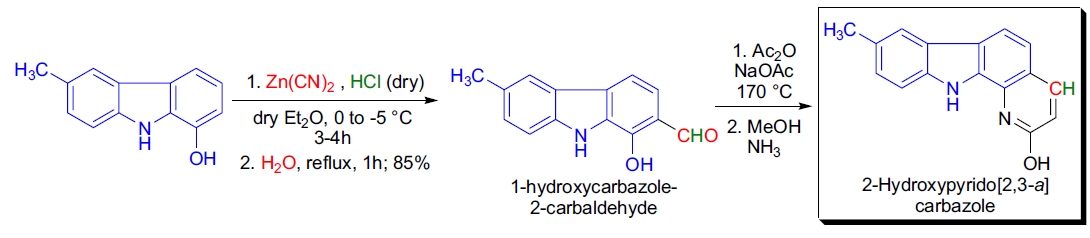
3. R. Prasad 等人通过 Gattermann 醛基化合成了具有抗肿瘤活性的吡啶并[2,3-a]咔唑衍生物。26 以 1-羟基咔唑为起始原料,经 Gattermann 醛基化生成 1-羟基咔唑-2-甲醛,随后通过 Perkin 反应进一步合成目标化合物。
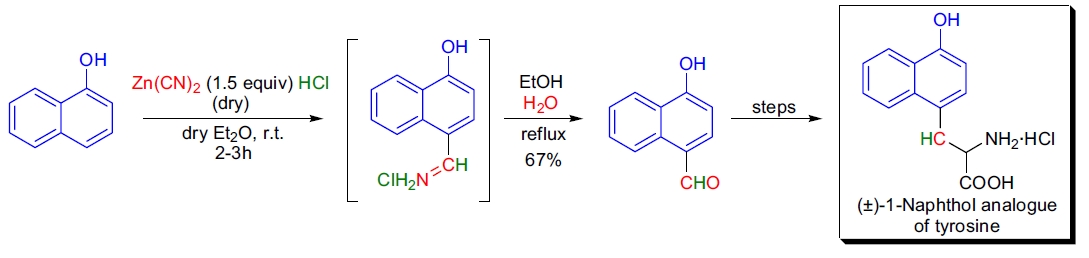
4. M.L. McLaughlin 的研究团队合成了荧光氨基酸类似物 1- 和 2- 萘酚酪氨酸衍生物。27 在 1-萘酚的 Adams 改进 Gattermann 醛基化反应中,以 Zn(CN)2 为催化剂,通过生成 4-羟基-1-萘甲醛,最终以 67% 收率获得目标化合物。