Glaser 偶联反应
重要性
[开创性文献1-3;综述4-8;改进与优化9-13;理论研究14,15]
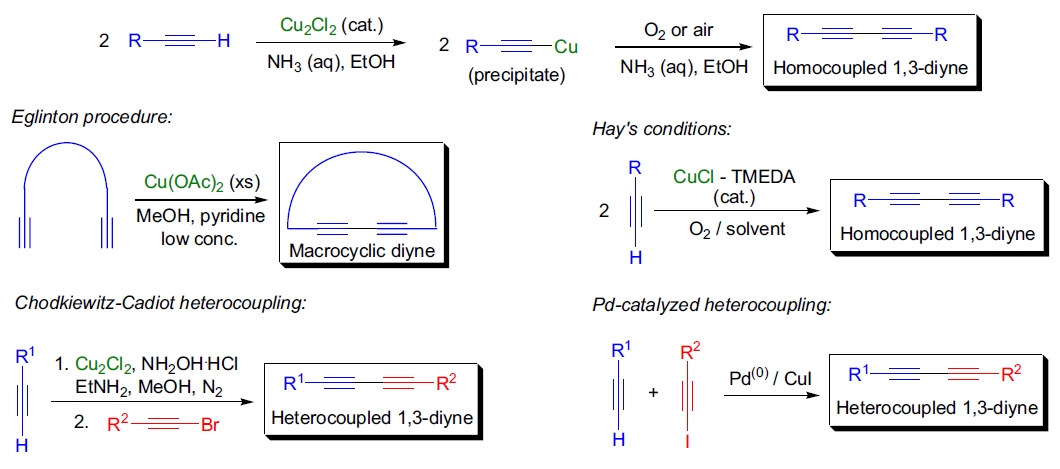
1869年,C. Glaser 发现苯基乙炔在铜(I)盐与氨水的作用下形成沉淀,经空气氧化后得到对称化合物1,4-二苯基-1,3-丁二炔(二苯二炔)。1 通过在铜盐存在下,氧化偶联末端炔烃制备对称共轭二炔和多炔(线性或环状)的反应被称为 Glaser 偶联。原始 Glaser 方法有许多版本,主要区别在于所用氧化剂的种类和用量:
- 1)除了氧气和空气,还常用 CuCl2 和 K3Fe(CN)6 作为氧化剂;
- 2)Glaser 的方法是异相反应且较慢,但 G. Eglinton 和 A.R. Galbraith 显示使用乙酸铜(Cu(OAc)2)和甲醇吡啶混合物可以加速反应(Eglinton 方法)。此方法被成功用于大环二炔的合成;10
- 3)A.S. Hay 使用三级胺如吡啶或 TMEDA 等双齿配体溶解铜(I)盐,随后通入氧气,可在室温下数分钟内获得几乎定量的偶联产物(Hay 偶联条件)。11,12
Glaser 偶联及其相关方法的特点包括:
- 1)适用于酸性末端炔,但炔烃酸性较弱(如烷基或硅基取代末端炔)时产率降低;
- 2)加入少量 DBU(强碱)可显著提高反应速率;7
- 3)反应条件可耐受多种官能团,因为氧化主要限于三键;
- 4)对于对氧敏感的底物或产物,可通过缩短反应时间或使用惰性气氛以及大量 Cu(II)盐来减少副反应;
- 5)杂环炔的偶联产率与溶剂密切相关,发现 DME 是最佳溶剂;
- 6)对于聚合反应,邻二氯苯是最佳溶剂;
- 7)最近的改进中使用了超临界 CO2 和离子液体进行偶联。
Glaser 偶联不适合制备非对称二炔,因此开发了其他方法,包括氧化和非氧化条件:
- 1)Chodkiewitz-Cadiot 反应通过铜(I)盐和脂肪胺(如 EtNH2)耦合末端炔和1-溴炔;17-19
- 2)铜(I)和钴(I)盐可催化炔基格氏试剂与1-卤炔的偶联;4
- 3)Pd(0)催化末端炔与1-碘炔在铜(I)盐存在下成功偶联。20
机理
[参考文献21-29]
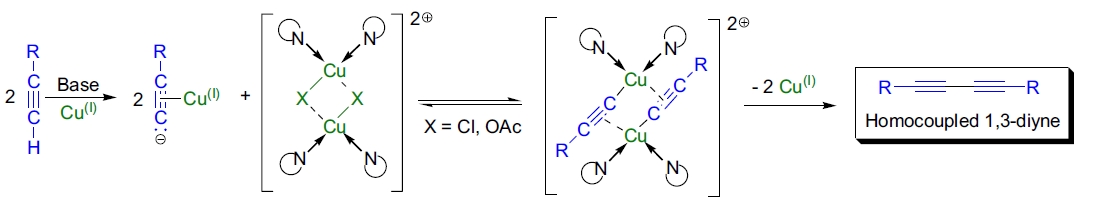
Glaser 偶联及其相关方法的机理非常复杂,目前尚未完全理解。研究表明,该机理高度依赖于实验条件。早期提出的自由基机理已被否定。 当前被接受的机理涉及二聚铜(II)乙炔化物的形成。
合成应用
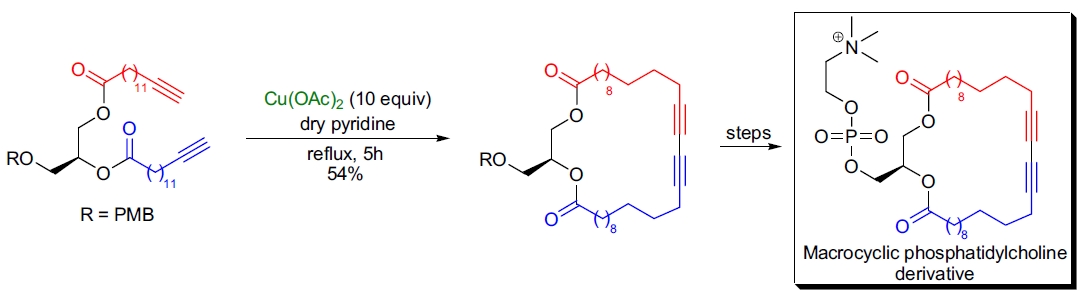
1. 新型可聚合磷脂酰胆碱的合成: G. Just 的研究团队成功合成了新型可聚合磷脂酰胆碱。为了制备32元大环二炔,采用了 Eglinton 改良的 Glaser 偶联。 二酯二炔起始物被缓慢加入至干吡啶中含10当量乙酸铜的回流溶液中,经柱层析后以54%的产率分离出大环化合物。
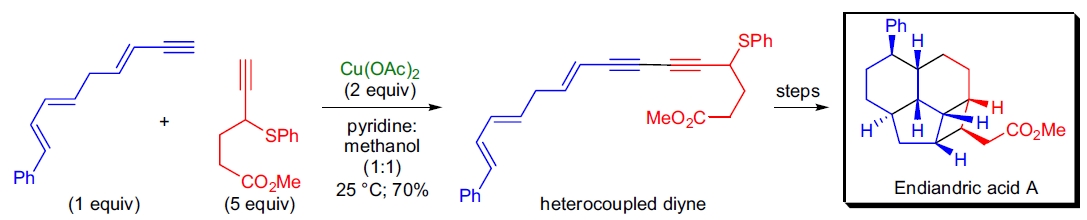
2. Endiandric 酸类天然产物的仿生全合成: K.C. Nicolaou 和其合作者通过两种不同末端炔的 Glaser 偶联组装了关键多不饱和前体。 为了最大化非对称二炔的产率,其中一种炔被过量使用。在吡啶和甲醇(1:1)混合溶剂中,两种炔烃与 Cu(OAc)2 于25°C 反应,得到70%的目标二炔产率。
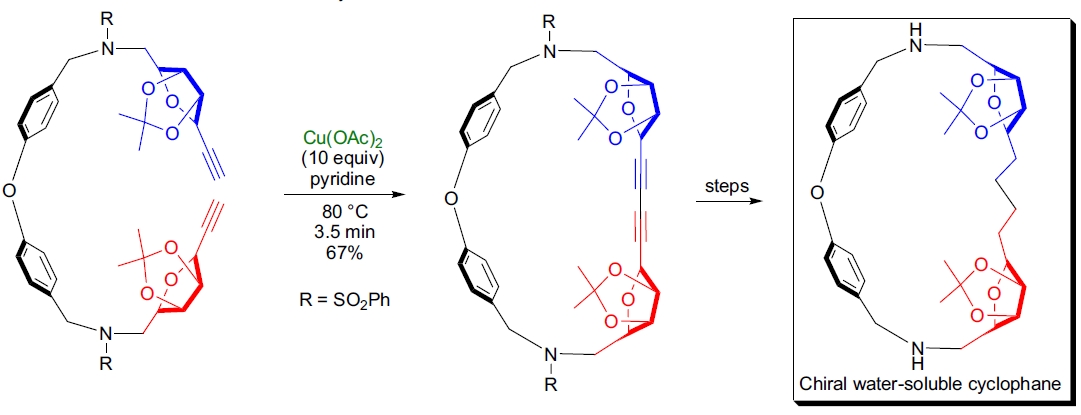
3. 手性水溶性环酚的合成: C.S. Wilcox 和其研究团队设计并合成了基于碳水化合物前体的手性水溶性环酚。这些化合物被称为“糖酚”,在模拟酶模型中具有潜在价值。 关键的环化步骤利用了 Glaser 偶联,该反应在80°C 的热流反应器中以67%的产率进行。
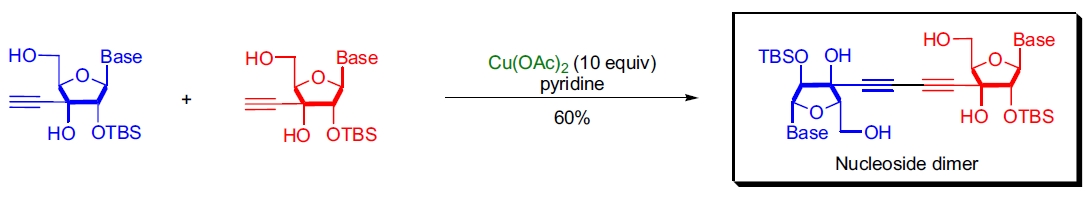
4. 二炔连接的核苷二聚体的制备: A. Burger 等人通过 Eglinton 改良的 Glaser 偶联制备了 3'-C-乙炔核苷的二聚体。36