Grob 裂解反应
重要性
[开创性文献1-3;综述4-6;理论研究7-9]
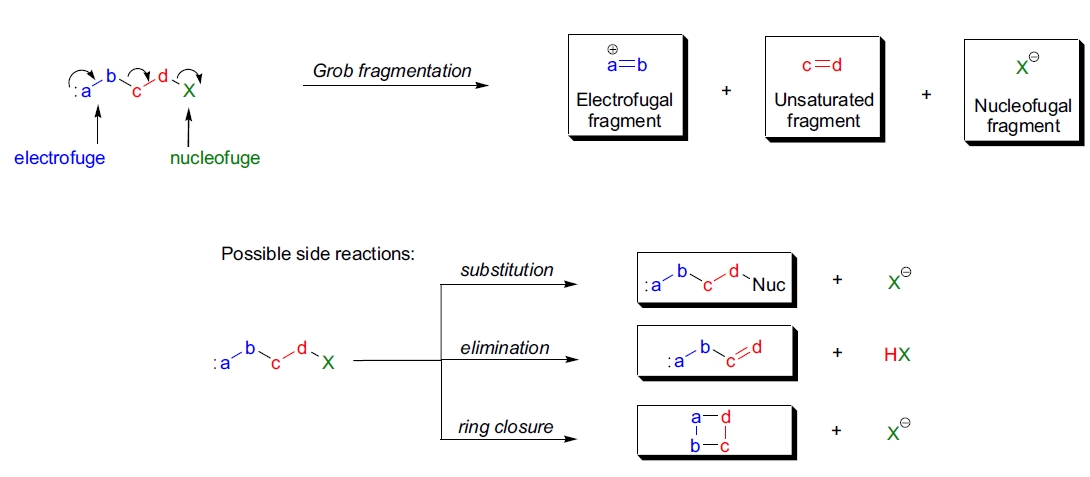
1950年代,C.A. Grob 首次系统性地研究了含有特定碳和杂原子组合(例如 B、O、N、S、P、卤素)的分子发生的有规裂解反应。此类裂解反应称为 Grob 裂解,最终形成三个片段(产物)。 “a-b-c-d-X” 的通式表示三个嵌入的组成部分:1)“a-b” 是电离基(electrofuge),其在不带有键合电子对的情况下离开,生成电离基片段; 2)“c-d” 在反应结束时成为不饱和片段;3)“X” 是亲核基(nucleofuge),其带着键合电子对离开。 典型的电离基片段是羰基化合物、二氧化碳、亚胺离子、碳正离子和酰正离子、烯烃以及氮气。“b” 原子上生成的正电荷的稳定性以及“a” 原子的诱导效应共同决定了电离基片段的生成难度。 不饱和片段通常是烯烃、炔烃、亚胺或腈,而亲核基片段则通常是卤化物、羧酸根或磺酸根离子。亲核基在裂解发生之前可能带有电荷(例如重氮离子),这会加速 b-c 和 d-X 键的裂解。 Grob 裂解通常伴有副反应,例如取代、消除或闭环反应。在刚性双环或多环体系中,Grob 裂解以协同和高度立体选择性的方式发生时,最具合成价值,因此产物的立体化学结果是可预测的。
机理
[参考文献10,5,11-13]
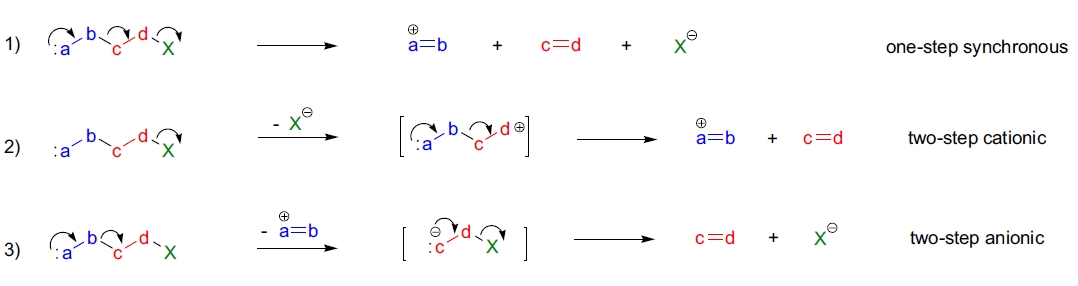
如 Grob 裂解等异裂反应可通过几种不同的机制进行,具体途径取决于底物的结构、空间位阻和电子因素。主要有三种机制途径: 1)一步同步(协同)裂解,其中 a=b 和 X 片段同时从中间的 c=d 组离开; 2)两步裂解,首先失去 X,a=b 片段从碳正离子中间体中离开; 3)两步裂解,首先失去 a=b,X 从碳负离子中间体中失去(这种情况很少见)。 同步机制具有非常严格的结构和立体化学要求,因为在过渡态中涉及到五个原子:所有五个原子的轨道都需要重叠。这些要求在刚性多环体系中最容易满足, 刚性分子的 Grob 裂解表现出与非协同裂解相比显著的反应速率增加(frangomeric 效应)。当由于应变无法实现协同过程的立体化学排列时,就会发生所谓的 syn 裂解或副反应(如消除)。6
合成应用
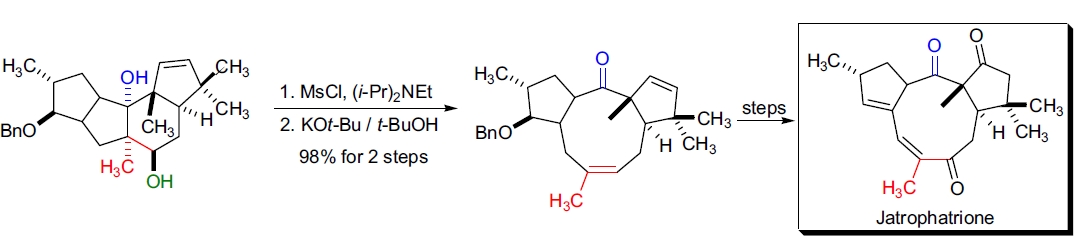
1. (±)-Jatrophatrione 的立体选择性全合成: L.A. Paquette 及其研究组成功实现了抗白血病剂 jatrophatrione 的首次全合成。14 该天然产物具有 [5.9.5] 融合三环骨架,并具有 trans-B/C 环融合。他们的方法的关键步骤是通过 Grob 裂解得到三环骨架。 四环 1,3-二醇在较少受阻的羟基上进行单一甲磺酰化,然后用叔丁醇钾处理,触发协同裂解,几乎定量地获得所需的三环产物。
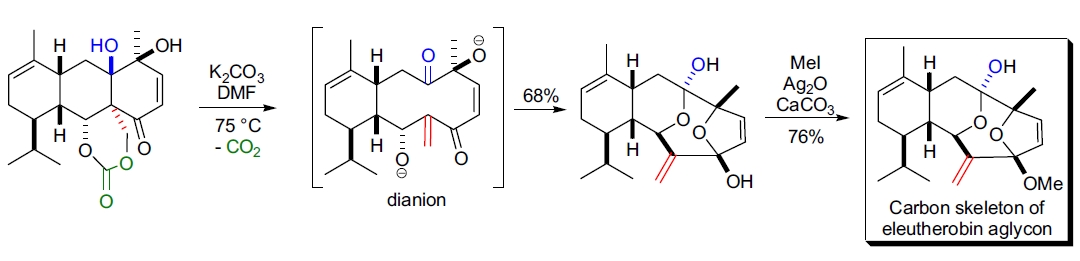
2. Eleutherobin 的合成: 在 J.D. Winkler 的实验室中,使用串联 Diels-Alder 反应和 Grob 裂解作为关键步骤合成了 eleutherobin 配基的碳框架。15 三环裂解前体在 75 °C 下于 DMF 中用碳酸钾处理,通过生成的二负离子中间体自发发生半缩醛化反应,最终得到 68% 收率的裂解产物。
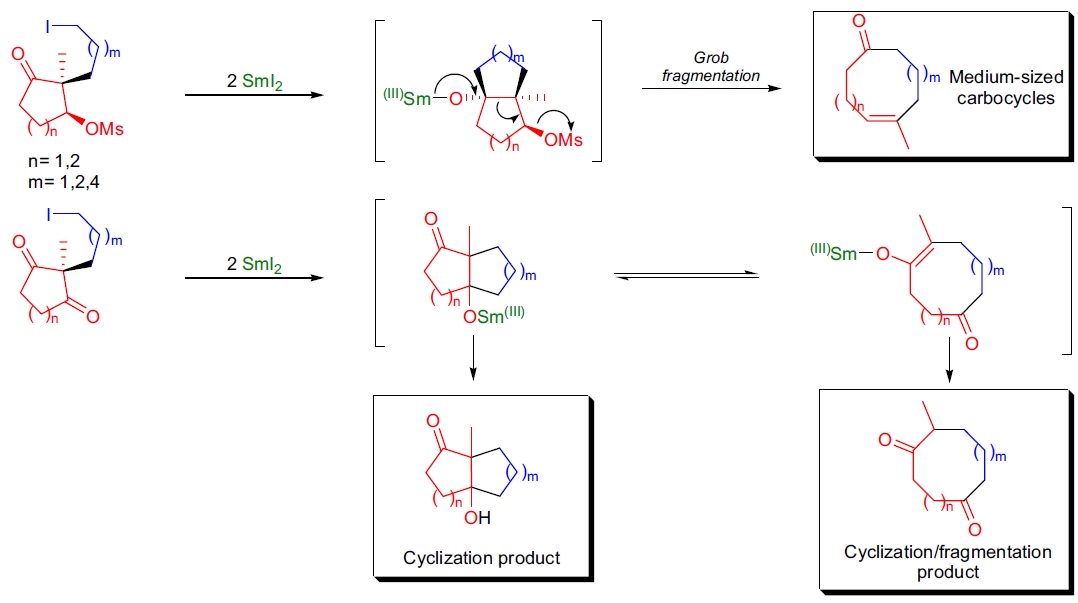
3. 中型环的高效合成: G.A. Molander 等人使用二价碘化钐通过包含环化/裂解过程的多米诺反应合成了高度官能化的立体定向中型碳环(8、9 和 10 元环)。16 该方法包括在 Barbier 反应条件下还原含有碘烷基、烯丙基或苄基侧链的取代酮甲磺酸酯。分子内 Barbier 反应在环己酮酮基和碘烷基链之间发生,生成二环醇盐, 随后发生 Grob 裂解。该反应在温和条件下以高收率和高度立体选择性方式进行。类似条件下还观察到环己二酮的环化反应,得到完全非对映选择性的多环羟基酮类。