Hajos-Parrish 反应
重要性
[开创性文献1-4;综述5-12;改进与优化13-18;理论研究19-22]
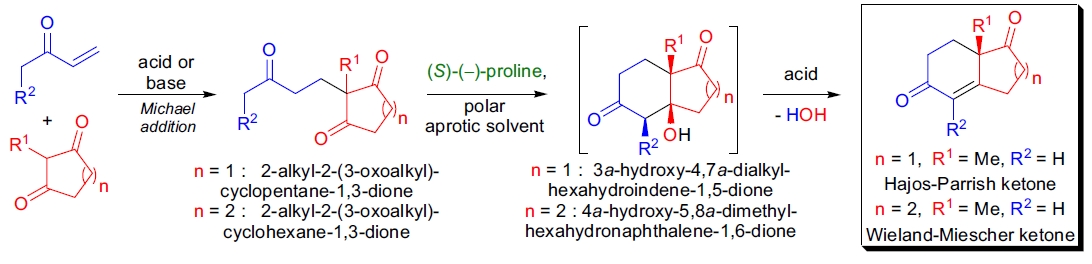
1970年代早期,两个工业研究团队独立研究了使用氨基酸催化的 2-烷基-2-(3-氧代烷基)-环戊烷-1,3-二酮的非对称分子内醇醛缩合反应。在 Hoffmann-LaRoche,Z.G. Hajos 和 D.R. Parrish 发现 (S)-(–)-脯氨酸的催化量足以促使 2-甲基-2-(3-氧代丁基)-环戊烷-1,3-二酮发生环化,并引发对映选择性3,4。在 DMF 等极性非质子溶剂中,在室温下加入 3 mol% 的 (S)-(–)-脯氨酸,反应定量生成产物,对映体过量率 (ee) 达到 93.4%。随后通过对甲苯磺酸催化脱水生成相应的双环酮 (Hajos-Parrish 酮),且光学纯度未降低。
机理
[参考文献4,25-28,20-22]
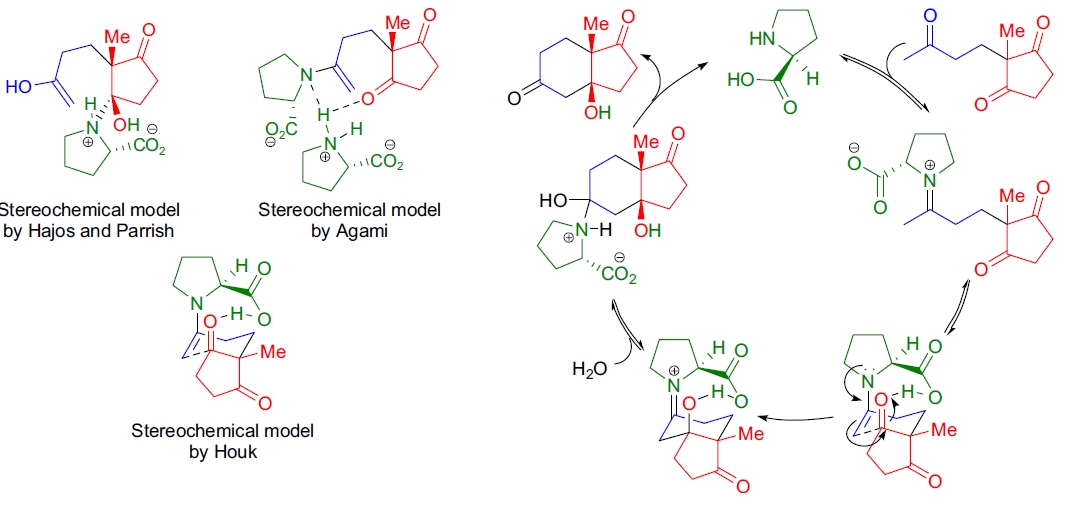
Hajos 和 Parrish4 最初提出的立体化学模型被 M.E. Jung25 和 A. Eschenmoser26 否定。他们提出了一种涉及侧链烯胺的单脯氨酸醇醛酶型机理。最广泛接受的过渡态模型由 C. Agami 等人提出,表明涉及两个 (S)-(–)-脯氨酸分子14,27-29。最近,K.N. Houk 等人重新研究了 (S)-(–)-脯氨酸催化的分子内和分子间醇醛缩合反应的机理。他们的理论研究、动力学、立体化学和稀释实验支持一种单脯氨酸机理,其中反应通过六元环状过渡态进行19-22。
合成应用
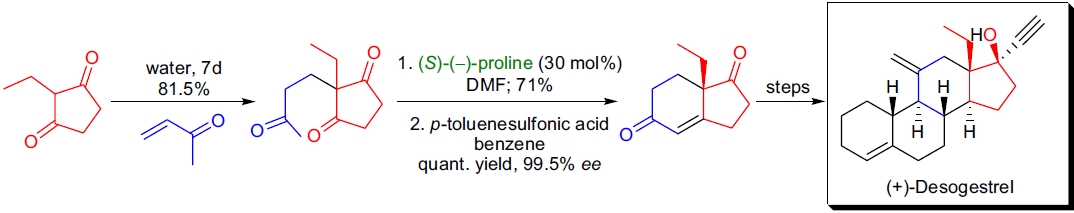
1. (+)-去甲炔诺酮的对映选择性全合成: E.J. Corey 等人完成了第三代口服避孕药 (+)-去甲炔诺酮的简短对映选择性全合成30。起始原料为 (S)-(+)-7a-乙基-2,3,7,7a-四氢-6H-茚-1,5-二酮,其通过 Hajos 和 Parrish 的原始方法制备4。通过 Michael 加成生成 2-乙基环戊烷-1,3-二酮与甲基乙烯基酮的产物,在 30 mol% 的 (S)-(–)-脯氨酸存在下进行分子内醇醛缩合和脱水,产率高,对映选择性优异。最终产物通过 16 步连续反应转化为去甲炔诺酮。
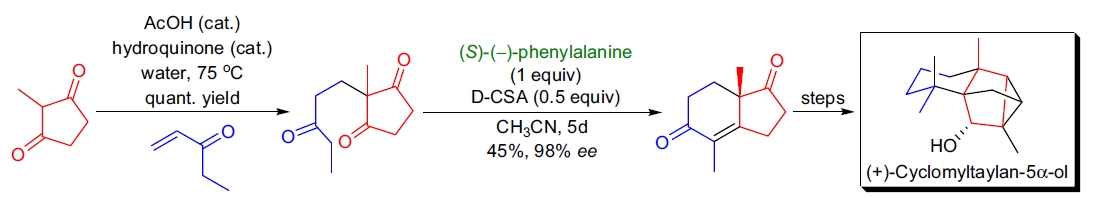
2. (+)-cyclomyltaylan-5α-ol 的全合成: H. Hagiwara 等人首次实现了从台湾地衣中分离的四环倍半萜醇 (+)-cyclomyltaylan-5α-ol 的对映选择性全合成31。反应起始于 Hajos-Parrish 酮的类似物,经过乙烯基甲酮的 Michael 加成和分子内醇醛缩合,最后通过重结晶获得 98% ee 的产物。
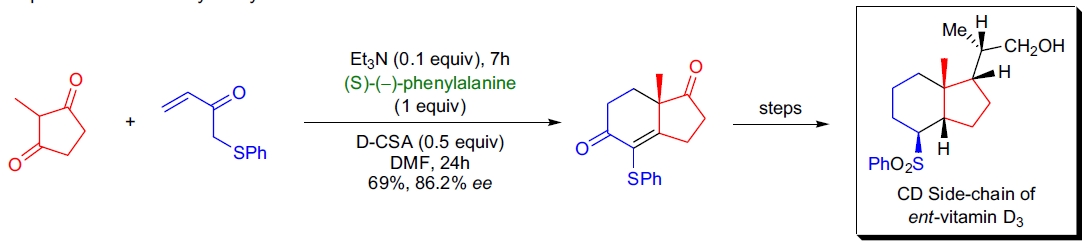
3. ent-维生素 D₃ 的部分合成: J. Wicha 等人报道了 ent-维生素 D₃ CD 侧链部分的对映选择性合成18。关键步骤为氨基酸催化的 Robinson 环化反应,反应优化后获得 69% 收率和 86.2% ee,光学纯度通过重结晶进一步提升至 95.6%。