Heck 反应
重要性
[开创性文献1-4;综述5-39;改进与优化40-47;理论研究48-54]
1970年代初,T. Mizoroki 和 R.F. Heck 独立发现芳基、苄基和苯乙烯基卤化物在升高温度下,与烯烃化合物在大位阻胺碱和 Pd(0) 催化剂的存在下发生反应,生成芳基、苄基和苯乙烯基取代的烯烃1-3。目前,钯催化的烯烃芳基化或烯基化反应被称为 Heck 反应。Heck 反应已经成为有机合成中最广泛使用的催化碳-碳键形成工具之一。
该反应的特点包括:
- 最适用于由单取代烯烃制备双取代烯烃;
- 烯烃上取代基的电子性质对反应结果的影响有限,通常缺电子烯烃的收率较高;
- 反应条件对烯烃组分中的多种官能团具有耐受性,例如酯、醚、羧酸、腈、酚和二烯等,但烯丙基醇容易发生重排;
- 烯烃的取代程度对反应速率影响显著,取代越多,反应速率越慢;
- 不对称烯烃(如末端烯烃)倾向于在最少取代的烯烃碳上发生取代;
- 芳基或乙烯基组分上的 X 基团性质对反应速率至关重要,其顺序为:I > Br ~ OTf >> Cl;
- R₁ 组分通常为芳基、杂芳基、烯基、苄基,很少为烷基(若烷基不含 β-位氢);
- 活性钯催化剂通过前驱物(如 Pd(OAc)₂、Pd(PPh₃)₄)原位生成,反应通常需要单齿或双齿膦配体和碱;
- 反应对水不敏感,溶剂无需严格去氧;
- Heck 反应是立体专一性的,钯络合物向烯烃的迁移插入和 β-氢消除均为 syn 立体化学过程。
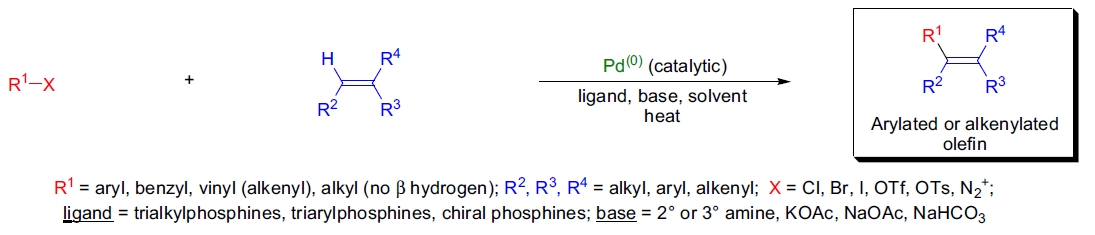
机理
[参考文献58,59,21,22,51,53]
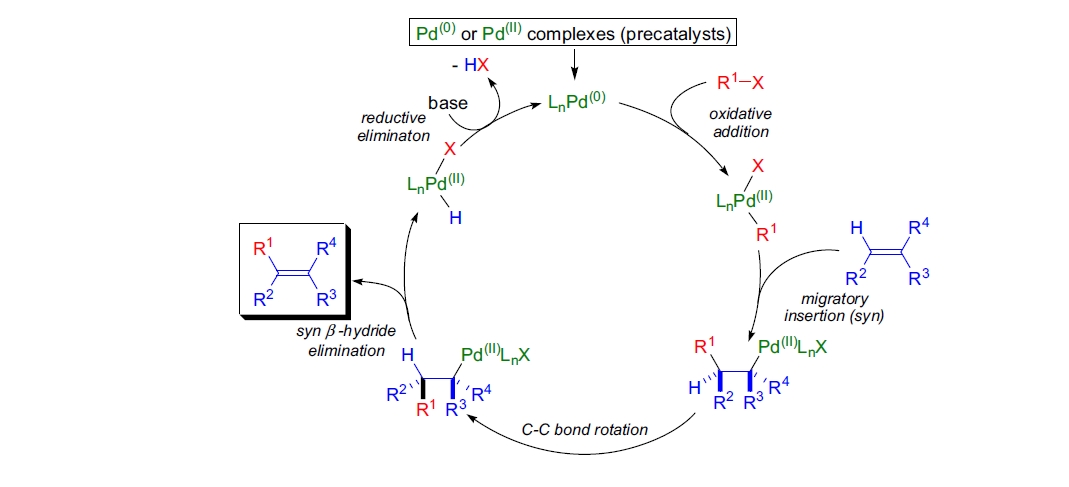
Heck 反应的机理尚未完全理解,其确切机理路径因反应条件的不同而略有变化。通常机制包括 Pd(0) 催化剂的生成,随后为 C-X 键的氧化加成(限速步骤)。为解释各种实验现象,提出了经过阴离子、阳离子或中性活性物种的精细催化循环21,36。
合成应用
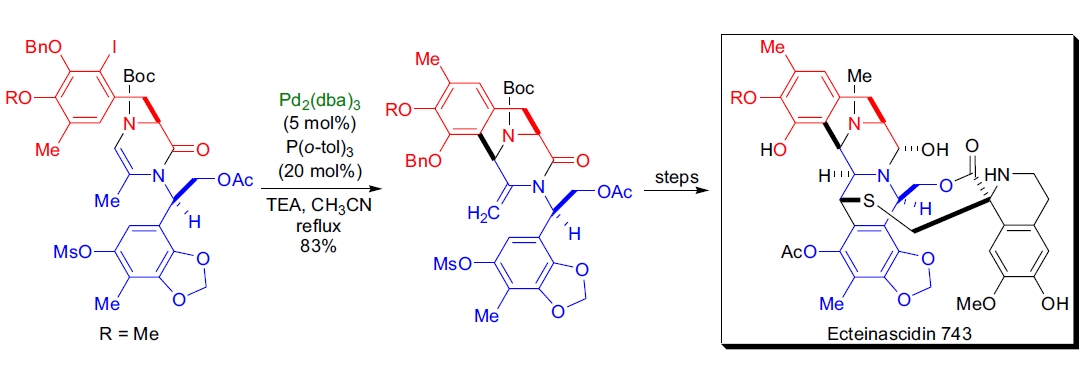
1. Ecteinascidin 743 的全合成: T. Fukuyama 等人利用分子内 Heck 反应作为关键步骤,构建了双环[3.3.1]环系。反应使用 5 mol% 钯催化剂和 20 mol% 膦配体,在回流的乙腈中进行,83% 收率获得三环中间体60。
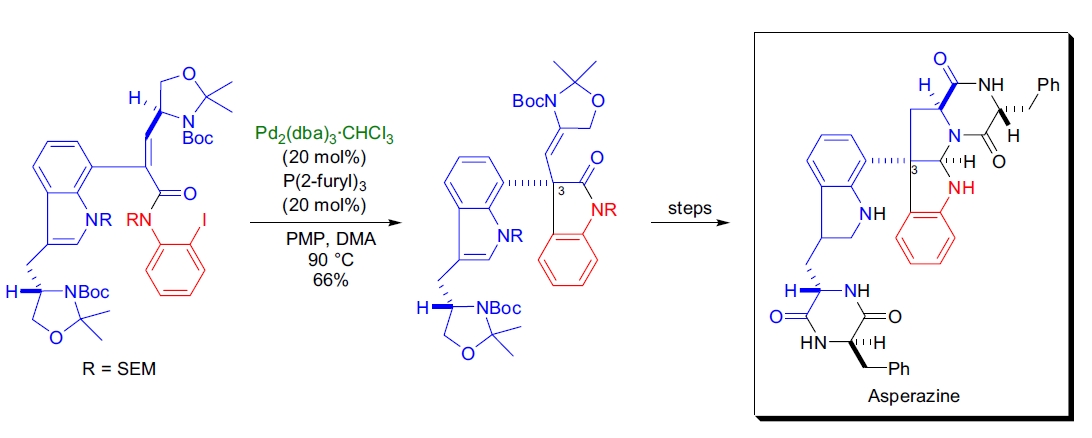
2. Asperazine 的全合成: L.E. Overman 等人通过对映选择性分子内 Heck 反应解决了 C3 季碳中心的构建难题。反应在 Pd₂(dba)₃⋅CHCl₃ 和 (2-呋喃基)₃P 配体存在下进行,66% 收率获得目标六环产物61。

3. Lasiodiplodin 的全合成: A. Fürstner 团队利用间二甲苯基三氟甲磺酸酯与乙烯的 Hecks 反应合成了宏环抗癌天然产物 Lasiodiplodin 的关键中间体62。