Heine 反应
重要性
[开创性文献1-4;综述5-9]
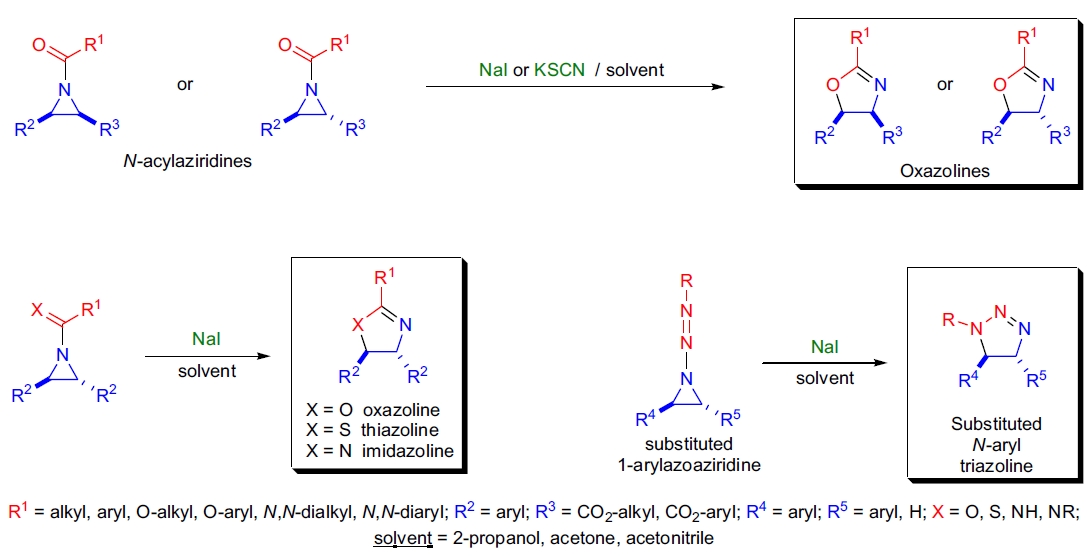
1959年,H.W. Heine 描述了 1-芳酰基氮丙啶在过量碘化钠和丙酮中于室温或回流条件下异构化为相应的 2-芳基-2-噁唑啉的反应1。该异构化反应几乎可以定量进行。取代的 N-酰基氮丙啶在亲核试剂(如 NaI 或 KSCN)作用下的分子内扩环反应生成相应的取代噁唑啉被称为 Heine 反应。尽管酸性或热条件下氮丙啶转化为噁唑啉的反应广为人知,但 Heine 反应是唯一能在温和中性条件下实现这一转化的反应5,6,9。
Heine 反应的主要特点包括:
- 仅碘离子和硫氰酸根离子能够诱导异构化2;
- 溶剂选择对反应影响很大,丙酮、乙腈和异丙醇效果最佳2;
- Heine 反应具有立体专一性;当使用非外消旋氮丙啶作为底物时,产物的立体化学结果为净构型保持;
- 3-芳基取代的 N-酰基氮丙啶羧酸酯或具有 C2 对称性的芳基双取代 N-酰基氮丙啶是最佳底物,因为这对环开裂的区域选择性至关重要;
- 环开裂不具区域选择性的底物会生成产物混合物;
- 1位带有吸电子基团的氮丙啶在与碘化钠反应时容易发生二聚反应5,6。
机理
[参考文献5,6,9]
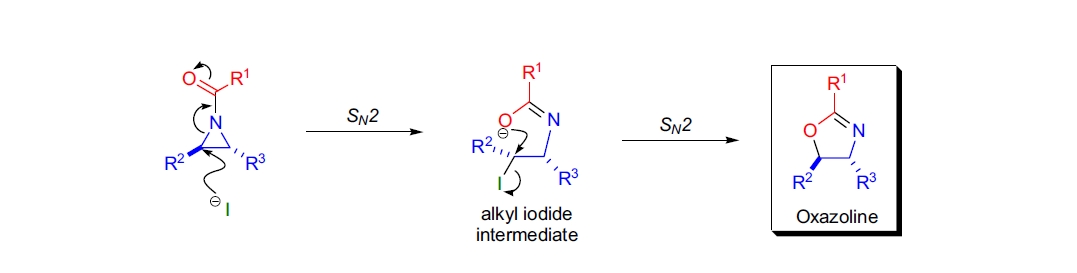
Heine 反应的第一步是碘离子对 C3 碳原子的区域选择性 SN2 进攻,导致氮丙啶环的开裂并在 C3 位发生构型反转。接着,次级碘代烷被带负电的氧原子以 SN2 方式进攻,导致 C3 位再次发生构型反转。由于在 C3 发生了两次连续反转(双重反转),Heine 反应的立体化学结果为净构型保持。
合成应用
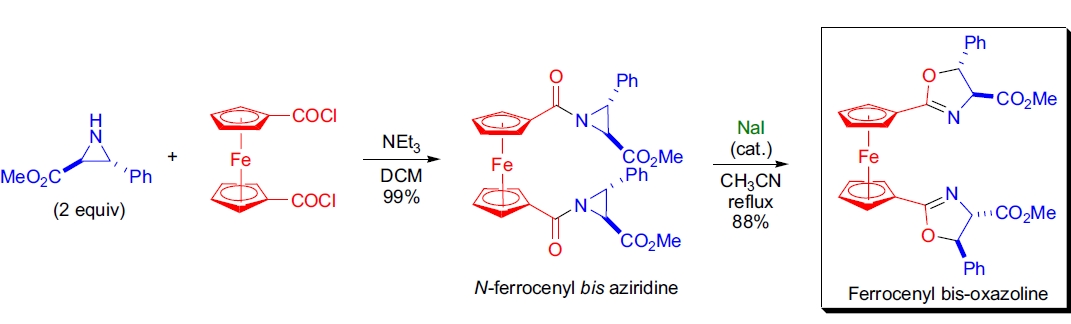
1. 铁酚基噁唑啉的合成: B. Zwanenburg 等人利用 Heine 反应作为关键步骤构建噁唑啉环,合成了铁酚基噁唑啉和铁酚基双噁唑啉10。
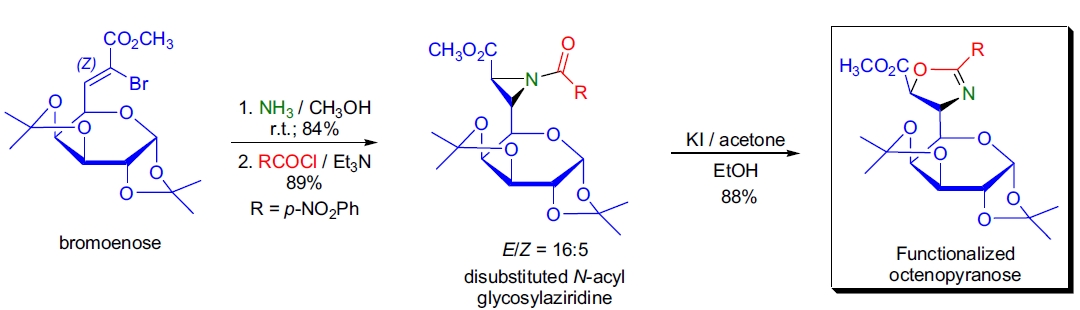
2. 八碳糖吡喃衍生物的制备: J.M.J. Tronchet 等人通过氮丙啶衍生物的环扩展反应制备了功能化的八碳糖吡喃衍生物11。
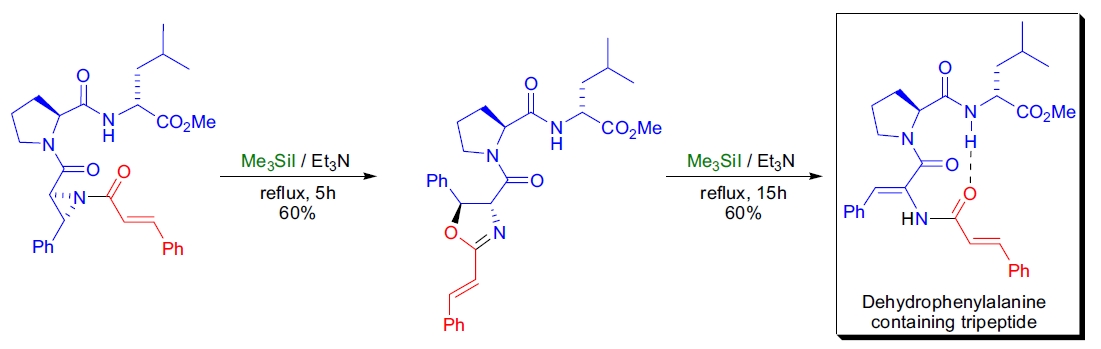
3. 脯氨酸三肽的合成: J. Iqbal 等人通过 Heine 反应将含苯丙氨酸类似物氮丙啶和脱氢苯丙氨酸残基的三肽转化为目标产物,这些三肽是研究 HIV 蛋白酶机制的良好模型12。