Henry 反应
重要性
[开创性文献1,2;综述3-18;改进与优化19-38;理论研究39]
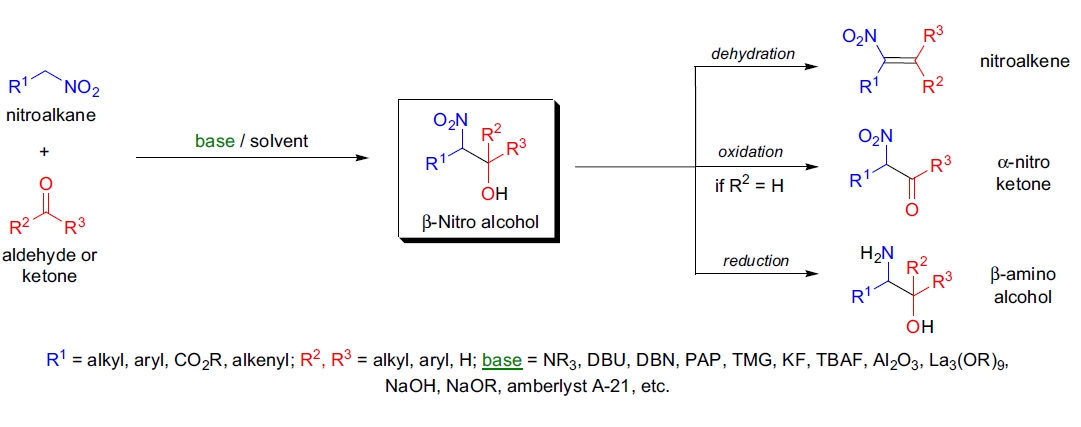
1895年,L. Henry 发现硝基烷在碱的存在下可与醛和酮反应生成 β-硝基醇1,2。自发现以来,硝基烷与羰基化合物之间的醇醛缩合(即硝基醇反应)成为了形成碳-碳键的重要工具,被称为 Henry 反应。β-硝基醇可以容易地转化为其他有用的合成中间体:
- 通过脱水生成硝基烯,可作为:
- 二烯体和二烯亲电试剂40-42;
- Michael 受体43;
- 隐性酮(通过 Nef 反应转化为相应的酮)。
- 通过氧化次级醇基团生成 α-硝基酮;
- 通过还原硝基基团生成 β-氨基醇;
- 通过自由基脱硝生成次级醇。
Henry 反应的主要特点包括:
- 仅需催化量的碱;
- 可以使用离子型或非离子型碱,例如碱金属氢氧化物、烷氧化物、碳酸盐、氟离子来源(如 TBAF44、KF45、氧化铝负载的 KF46)、固体支持碱47、稀土金属盐48、过渡金属配合物31,33,34以及有机氮碱(如胺类49、TMG50、DBU51、DBN52 和 PAP27);
- 溶剂和碱对反应结果影响不大;
- 底物的空间性质起重要作用:位阻较大的底物(通常是酮类)反应较慢,并且容易发生副反应;
- β-硝基醇通常以二面体异构体(syn 和 anti)混合物的形式生成,但通过改变反应条件可以实现高水平的二面体选择性6,17;
- 硝基基团所附的立体中心容易发生表面化作用。
Henry 反应常伴随以下副反应:
- β-硝基醇容易脱水,尤其是当芳醛作为底物时,但通过仔细选择条件可以抑制这一现象;
- 对于空间位阻较大的羰基化合物,可能发生碱催化的自缩合或 Cannizzaro 反应;
- 逆 Henry 反应可能阻碍反应完成。
已有多种改进方法被开发:
- 将不活泼的烷基硝基化合物转化为相应的二阴离子,以加快其与羰基化合物的反应19,20;
- 使用 PAP 作为碱可加速酮类的反应27;
- 高压和无溶剂条件下提高了反应的化学选择性和区域选择性;
- 醛与 α,α-双去质子化硝基烷反应生成硝酸酯醇盐,并通过动力学质子化主要生成 syn-硝基醇6;
- 硝酸酯阴离子中醇氧原子被硅基保护时,通过动力学质子化主要生成 anti-β-硝基醇6;
- 硝酸酯阴离子中硝基基团的一氧原子被硅基保护时,在催化量氟离子存在下与醛反应主要生成 anti-β-硝基醇6;
- 在手性催化剂存在下,可以实现不对称 Henry 反应13,15,17,18,34;
- 当亚胺替代羰基化合物作为底物时,会发生 aza-Henry 反应生成硝胺;硝胺还原后得到相邻二胺28,37。
机理
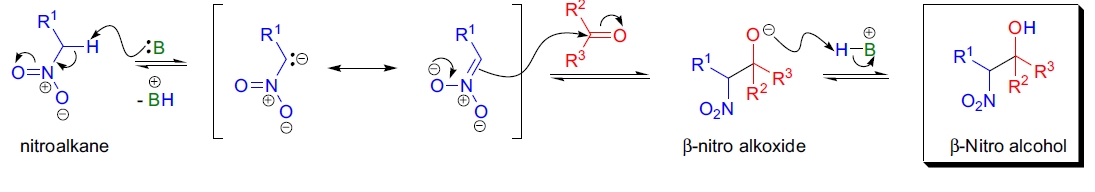
[参考文献53,51]
Henry 反应的所有步骤均为可逆过程。首先,碱对硝基烷的 α-位去质子化,生成共振稳定的硝基负离子。随后,该负离子与羰基化合物发生醇醛缩合(C-烷基化),生成二面体 β-硝基烷氧化物。最后,β-硝基烷氧化物通过质子化生成预期的 β-硝基醇。
合成应用
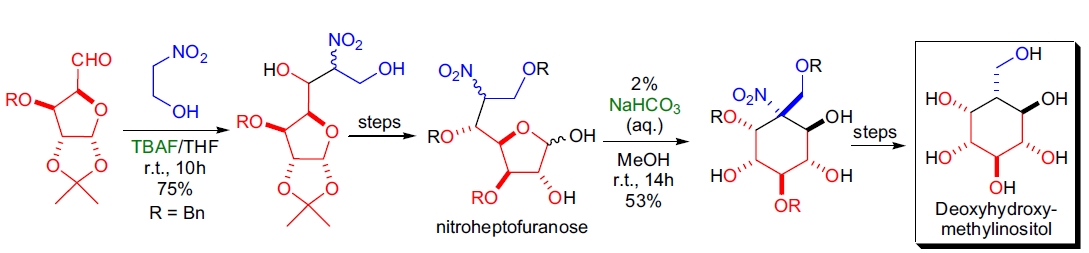
1. Deoxyhydroxymethylinositols 的合成: R.J. Estévez 和其团队利用分子内 Henry 反应将硝基庚呋喃糖转化为羟甲基肌醇。通过去除硝基和保护基得到目标产物54。
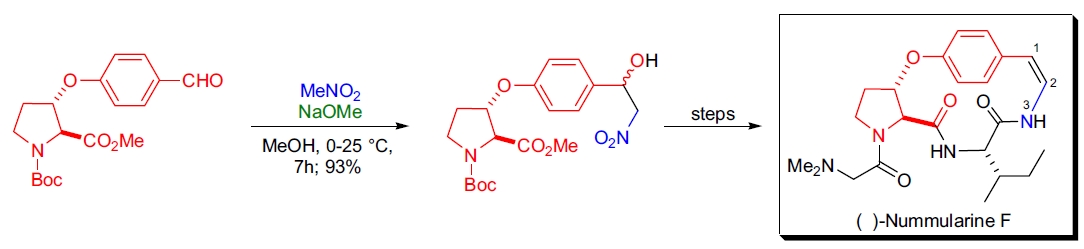
2. (–)-Nummularine F 的全合成: M.M. Joullié 团队利用 Henry 反应引入 N3 氮原子,完成了 14 元大环环肽生物碱 (–)-Nummularine F 的全合成55。
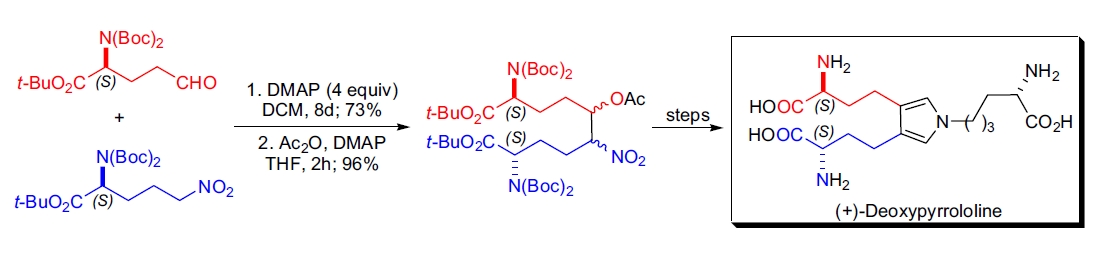
3. (+)-Deoxypyrrololine 的全合成: M. Adamczyk 团队利用 Henry 反应在硝基烷和醛片段间构建关键 β-硝基醇,用于合成骨胶原交联 (+)-Deoxypyrrololine56。
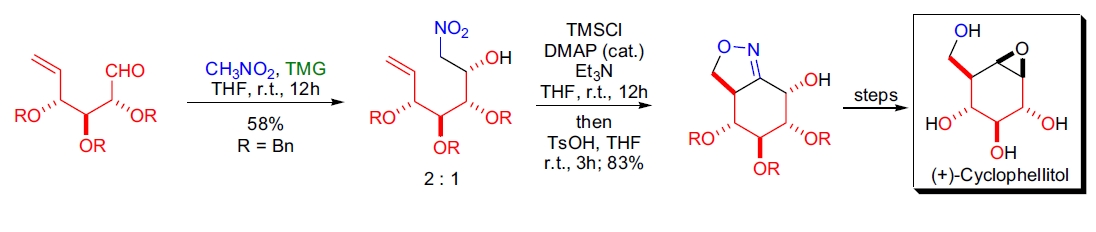
4. (+)-Cyclophellitol 的全合成: T. Ishikawa 等通过 Henry 反应构建前体,并利用分子内硝酸酯 [3+2] 环加成完成目标分子的合成57。