杂Diels-Alder 反应
重要性
[开创性文献1-3;综述4-43;理论研究44-59]
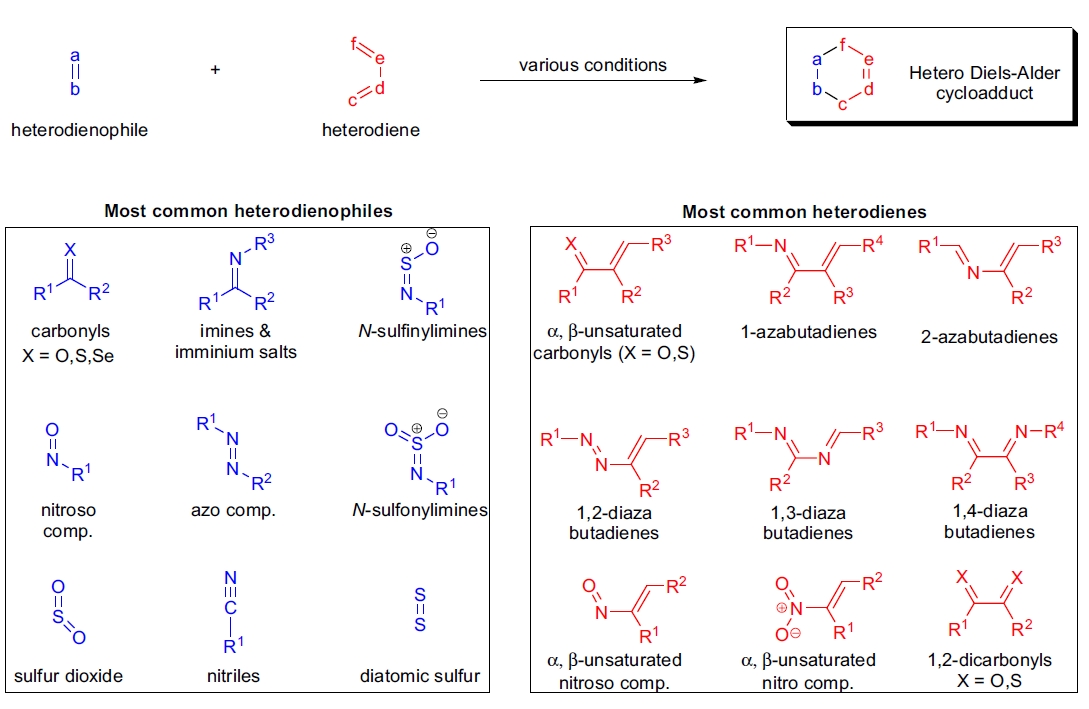
二烯体和亲二烯体通过 [4π + 2π] 环化生成环己烯衍生物的反应被称为Diels-Alder 反应(DA 反应)。如果其中一个或多个原子为非碳原子,则称为杂 D-A 环加成反应(HDA)。1943年,K. Alder 首次报道了亚胺作为异亲二烯体参与的 HDA 反应1。自首次报道以来,HDA 反应已被广泛用于杂环化合物的合成。
HDA 反应的主要特点包括:
- 具有高度的区域选择性和二面体选择性,其反应结果与全碳 D-A 反应同样可预测;
- 当二烯体不含杂原子且异亲二烯体因杂原子的存在而电子缺乏时,反应按照正常电子需求 D-A 反应机理进行(二烯体的 HOMO 与异亲二烯体的 LUMO 相互作用);
- 当二烯体含有一个或多个杂原子和/或吸电子基团时,二烯体表现为电子缺乏,需要电子丰富的亲二烯体,反应按反向电子需求 D-A 反应机理进行(杂二烯的 LUMO 与亲二烯体的 HOMO 相互作用);
- 当杂二烯被强电子供给基团取代时,其电子缺乏性质可能被逆转,从而与适当的电子缺乏亲二烯体发生正常电子需求 HDA 反应;
- HDA 反应可被路易斯酸催化,通常表现出比未催化过程更高的区域选择性和立体选择性;
- 通过使用手性辅助剂或催化剂,可以实现不对称 HDA 反应22,31,38。
机理
[参考文献60-69,51,53]
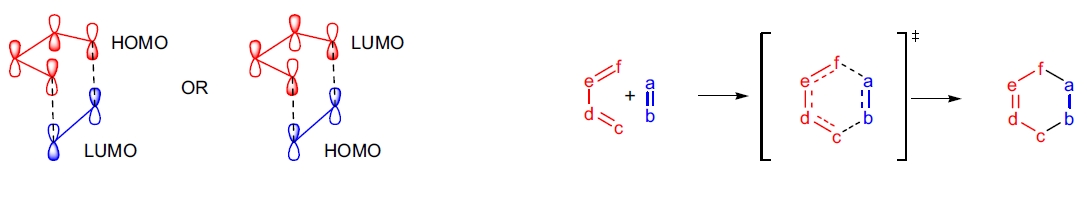
从机理上讲,全碳 Diels-Alder 反应通常被认为是协同的周环反应,其过渡态具有芳香性,但也有证据表明该反应可能以逐步(双自由基或双离子)方式进行。对于 HDA 反应,理论研究表明其过渡态通常是协同的,但对称性较差。根据反应条件及底物的取代基种类和数量,HDA 反应可能呈现出极性过渡态并以逐步方式进行。
合成应用
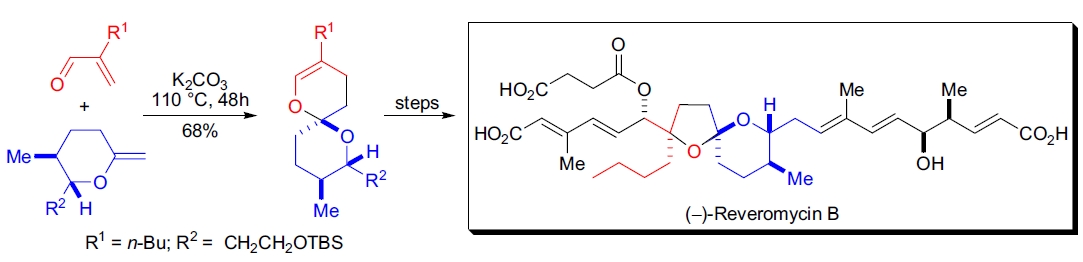
1. (–)-Reveromycin B 的全合成: M.A. Rizzacasa 等人利用 HDA 反应完成了表皮生长因子抑制剂 (–)-Reveromycin B 的全合成。关键步骤是 α,β-不饱和醛(正丁烯醛)与光学纯亚甲基吡喃之间的环加成。将反应物加热至 110 °C,在无溶剂条件下反应两天,获得单一对映体的 6,6-螺缩醛70。
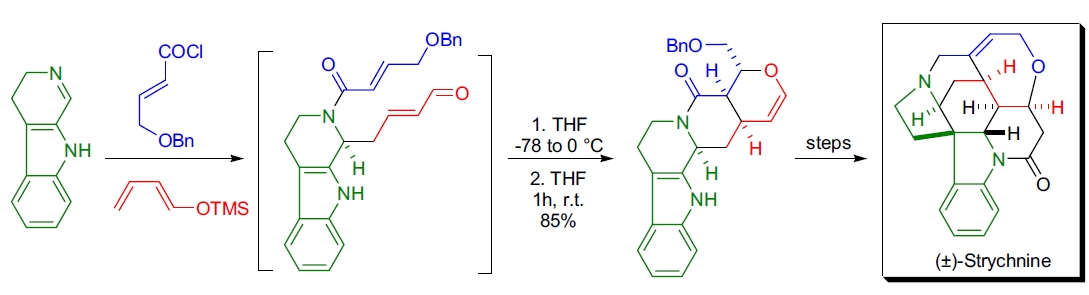
2. (±)-Strychnine 的全合成: S.F. Martin 实验室通过串联的共轭 Mannich 加成和 HDA 反应合成了天然产物五环杂氧辛环核。反应底物为 4,9-二氢-3H-β-咔啉,先转化为相应的 N-酰离子,再与 1-三甲基硅氧基丁二烯进行反应,随后通过 HDA 反应以 85% 收率生成目标化合物71。
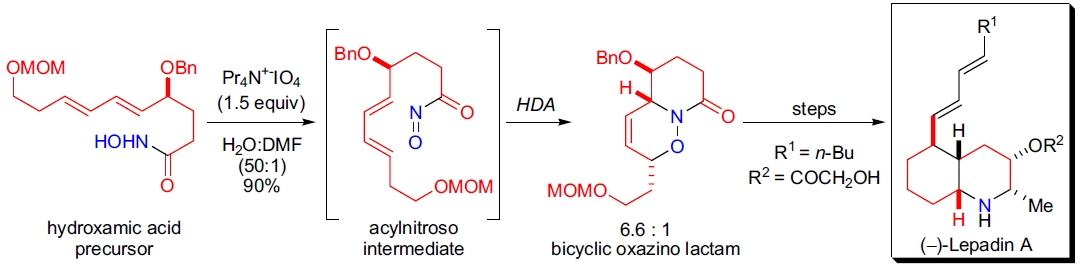
3. (–)-Lepadin A 的全合成: C. Kibayashi 等报道了十氢喹啉类生物碱 (–)-Lepadin A 的首次全合成。作者采用分子内 HDA 反应,以原位生成的酰亚硝基化合物作为反应底物。在 Pr₄N(IO₄)、水-二甲基甲酰胺(50:1)溶液中氧化羟肟酸后,生成酰亚硝基化合物并顺利进行 [4+2] 环加成,形成产物为 6.6:1 的二面体异构体混合物72。
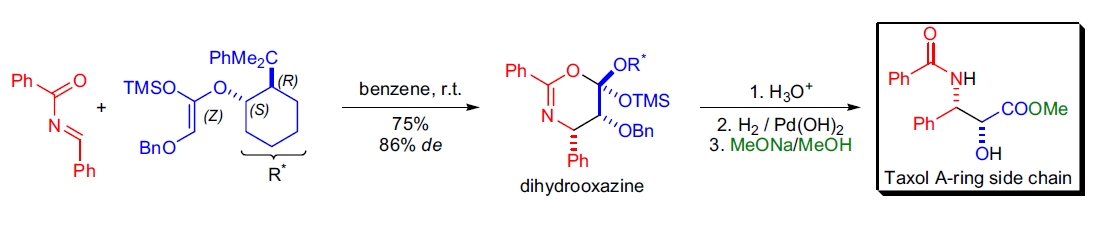
4. Taxol A-环侧链的合成: C.H. Swindell 等人利用热反向电子需求 HDA 反应合成了 Taxol 的 A-环侧链。以 (Z)-烯酮醇为起始物,连接手性辅助剂后与 N-苯甲酰亚胺反应,生成二氢噁嗪,产率为 75%,且具有良好的二面体选择性73。