Hofmann 消除反应
重要性
[开创性文献1-4;综述5-9;改进与优化10,11;理论研究12]
1851年,A.W. Hofmann 发现三甲基丙基铵氢氧化物在加热时分解生成叔胺(三甲胺)、烯烃(丙烯)和水1,2。直到1881年,Hofmann 将这一方法应用于研究哌啶和含氮天然产物(如生物碱)的结构时,这一转化才得到广泛使用3,4。季铵氢氧化物的热分解生成叔胺、烯烃和水的过程被称为 Hofmann 消除反应。
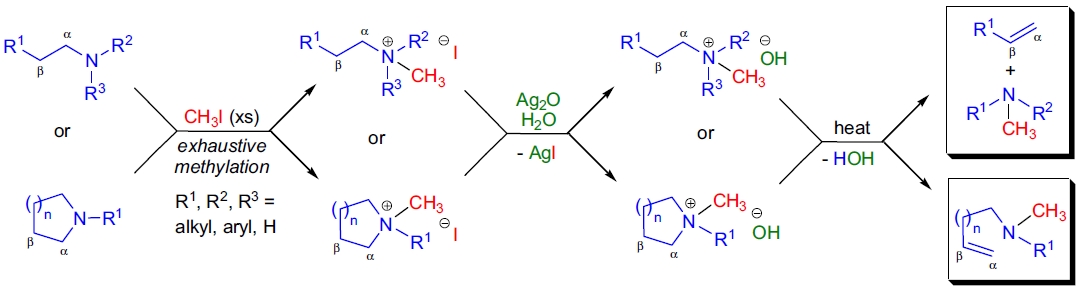
这一过程包括三个步骤:
- 用过量碘甲烷对伯胺、仲胺或叔胺进行完全甲基化,生成相应的季铵碘化物;
- 用氧化银和水处理,将碘离子交换为氢氧根离子;
- 将季铵氢氧化物的水溶液或醇溶液在减压条件下浓缩,并加热至 100-200 °C,引发消除反应。
在减压条件下,反应通常在较低温度下进行,且产率更高。当底物为杂环化合物或氮原子位于环交界处或桥头时,需要重复上述步骤多次以完全消除分子中的氮。在早期研究中,重复次数常用来指示氮原子在原始分子中的位置,并为未知物质的结构提供重要线索。
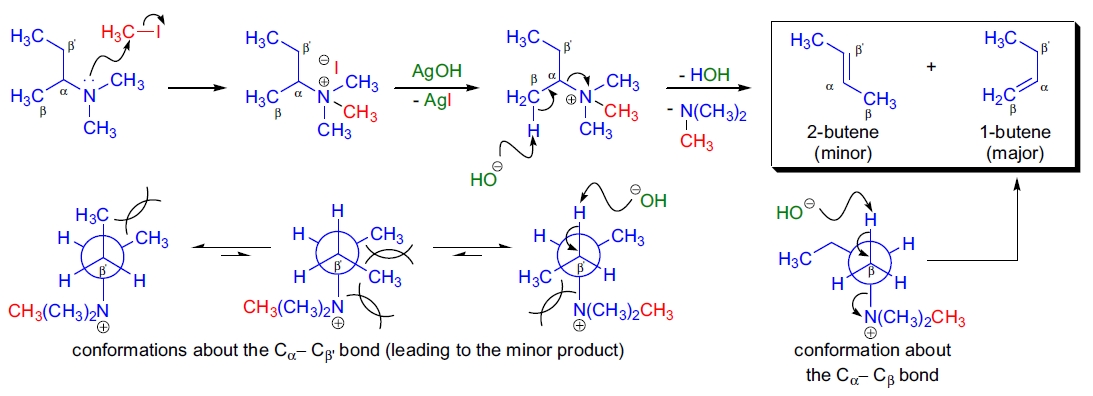
Hofmann 消除是一种 β-消除,即碱(氢氧根离子)从 β-碳原子上抽取一个氢。在不对称化合物(其中多个与氮相连的烷基具有 β-氢原子)的情况下,碱优先抽取位于最少取代碳上的 β-氢,形成较少取代的烯烃(Hofmann 规则)1。
Hofmann 消除的副反应较少:偶尔碱可以作为亲核试剂,生成取代产物。当底物不含有 β-氢的烷基时,热解的主要产物是取代产物(水为溶剂时为醇,无溶剂时为醚)13。Hofmann 消除的一个重要变体是 Wittig 改进,其中用强碱(如烷基锂、KNH₂/液氨等)处理季铵卤化物,通过 Ei 机制生成烯烃和叔胺11。
机理
[参考文献14-27,11,28-30,12,31-34]
Hofmann 消除的机理通常为 E2 机制,即反消除(离去基团必须处于反二轴/反平面位置)。然而,对于某些底物,当反消除过程不利且化合物含有足够酸性的烯丙基或苄基 β-氢原子时,机制可能偏向于碳负离子 E1cb 方向。在非环状底物中,消除反应通常生成最少取代的烯烃(Hofmann 产物)。
消除产物的形成受以下三个因素影响:
- 双键在过渡态中的发展程度;
- β-氢原子的酸性;
- 过渡态中的空间相互作用(这一点最广泛被接受)。
在环状铵盐中,消除过程的最重要因素是反 β-氢原子的可得性。当环状底物中既有 β 反 β 的氢原子时,消除反应生成最取代的烯烃(Saytzeff 规则)。
合成应用
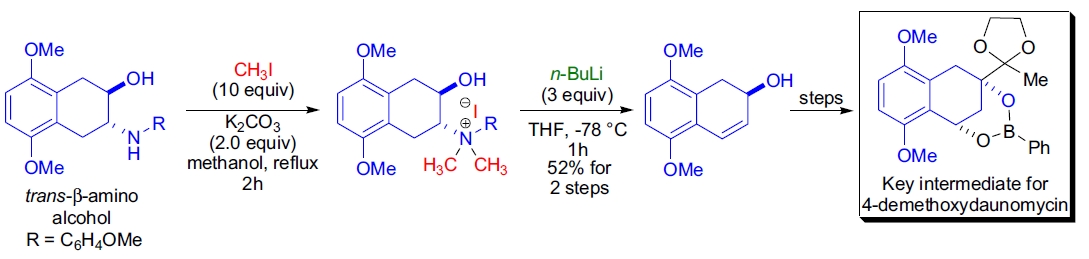
1. 4-去甲氧基柔红霉素的全合成: M. Shibasaki 实验室通过 Hofmann 消除反应实现了 4-去甲氧基柔红霉素的对映选择性正式全合成。关键中间体来源于光学纯 trans-β-氨基醇,首先将其完全甲基化为相应的季铵盐,再用过量正丁基锂处理,生成目标烯丙醇,产率中等35。
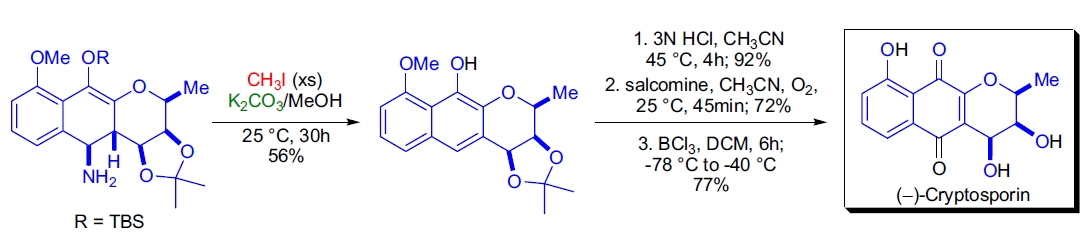
2. (–)-Cryptosporin 的全合成: 在 (–)-Cryptosporin 的全合成中,R.W. Franck 等人开发了一种高效方法,用于特异性合成天然存在的萘并[2,3-b]吡喃醌和[2,3-b]呋喃醌。苄位伯胺的 Hofmann 消除是合成的最后步骤。用过量 MeI 和 MeOH/K₂CO₃ 对伯胺进行完全甲基化后,季铵盐在室温下自发消除36。
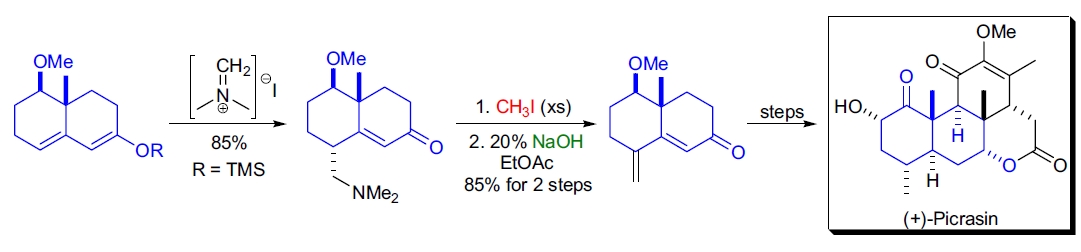
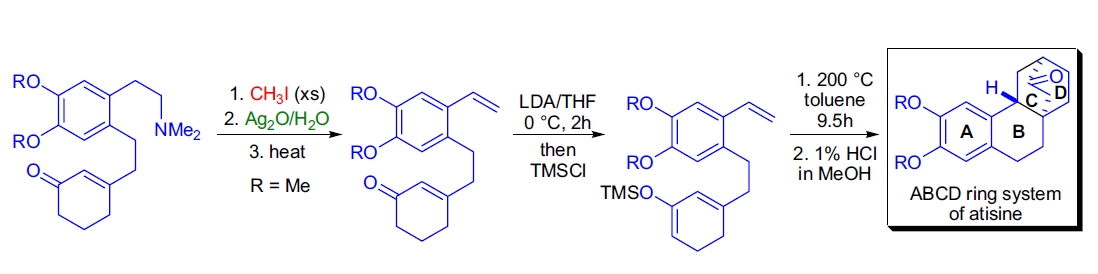
3. 地榄素 ABCD 环系的合成: T. Kametani 等人通过分子内 Diels-Alder 环加成反应合成了地榄素的 ABCD 环系。该二烯体通过传统的 Hofmann 消除反应从相应的二甲氨基前体制得37。
4. (+)-Picrasin B 的全合成: 在 D.S. Watt 实验室中,利用 (–)-Wieland-Miescher 酮对 (+)-Picrasin B 进行了对映选择性全合成。合成早期阶段,通过两步法引入环外双键:首先用 Eschenmoser 盐对双环共轭 TMS 烯醇醚进行 γ-位烷基化,随后对二甲氨基基团进行 Hofmann 消除38。