Hofmann-Löffler-Freytag 反应
重要性
[开创性文献1-4;综述5-14;改进与优化15-22;理论研究23]
19世纪80年代早期,A.W. Hofmann 试图通过暴露于氢卤酸或溴来确定哌啶是否为不饱和化合物(当时哌啶的结构尚不明确)。在这些研究中,他制备了各种 N-卤胺和 N-卤酰胺,并研究了它们在酸性和碱性条件下的反应。通过将 1-溴-2-丙基哌啶用热硫酸处理,然后碱性处理,生成了八氢吲哚里嗪(一种双环叔胺)1-3。1909年,K. Löffler 和 C. Freytag 将这一转化应用于简单的仲胺,并意识到它是一种制备吡咯烷的通用方法4。
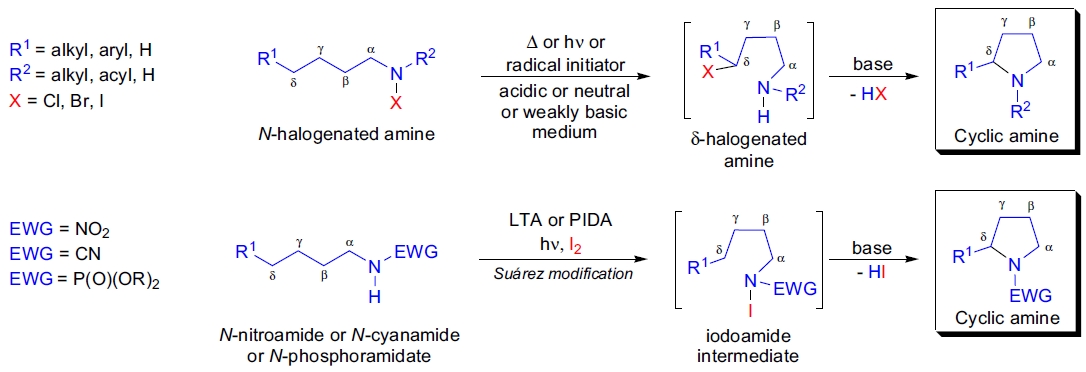
N-卤代胺通过分子内 1,5-氢原子转移到氮自由基形成环胺的反应称为 Hofmann-Löffler-Freytag 反应(HLF 反应)。该反应的主要特点包括:
- 可以在酸性溶液中进行,但中性甚至弱碱性反应条件也能成功应用24,25;
- 如果中间体烷基自由基因杂原子(如氮)而得到稳定,则反应可以在较温和条件下进行24;
- 自由基过程的启动可通过加热、光照或自由基引发剂(如二烷基过氧化物、金属盐)实现;
- 最初生成的氮中心自由基主要从 δ-位置(或 5-位置)抽取 H-原子,优先生成五元环;
- 在刚性环状体系中,偶尔会形成六元环24,15。
原始的强酸性反应条件通常不适合复杂底物的敏感官能团和保护基,因此引入了多种改进方法:
- 在中性条件下,N-溴酰胺的光解可以进行26;
- 在过硫酸盐和金属盐存在下,磺酰胺可在中性条件下发生远程 γ-和 δ-卤化27;
- 最重要的变体是 Suárez 改进,其中 N-硝酰胺20、N-氰酰胺18 和 N-磷酰胺22 在高价碘试剂和碘(I₂)存在下反应,通过假定的碘酰胺中间体生成氮中心自由基。
HLF 反应与著名的 Barton 硝酸酯反应密切相关,后者通过烷氧自由基进行,在类固醇合成中的远程官能团化中被广泛使用。
机理
[参考文献28-31]
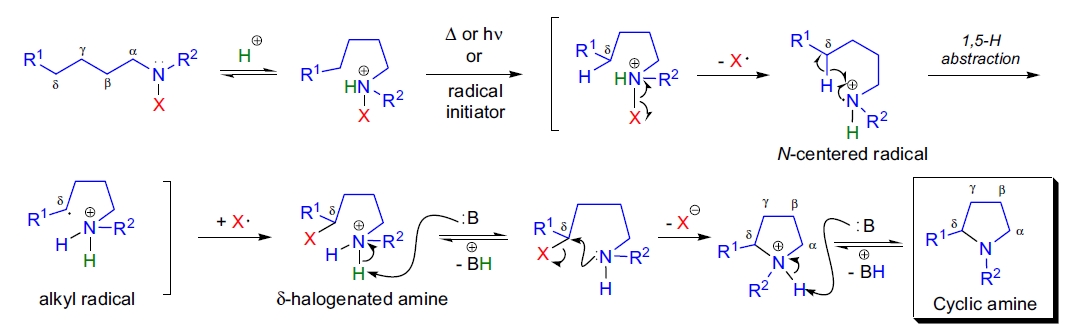
HLF 反应的机理是自由基链反应。当反应在酸性介质中进行时,第一步是 N-卤胺的质子化,生成相应的 N-卤化铵盐。通过热解、光照或自由基引发剂处理,N-卤键发生均裂生成氮中心自由基,该自由基迅速发生分子内 1,5-氢原子抽取。接着,新生成的烷基自由基进行分子间卤原子抽取。用碱处理 δ-卤代胺生成目标环胺产物。
合成应用
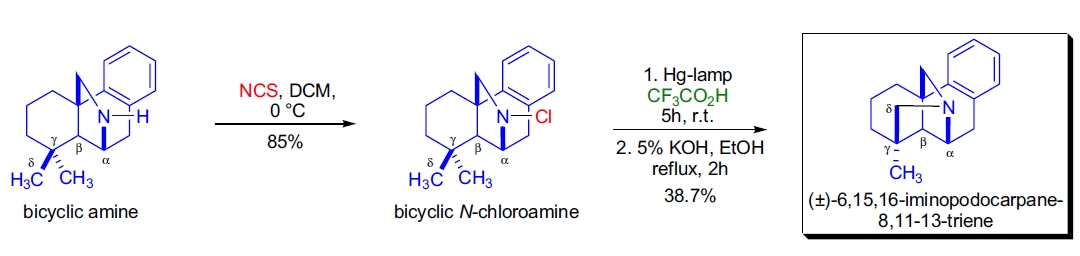
1. Kobusine 的合成: Y. Shibanuma 团队开发了一种新颖的合成方法,用于构建二萜类生物碱 Kobusine 的桥环氮环系。通过 Hofmann-Löffler-Freytag 反应,从二环氯胺出发,合成了目标化合物 (±)-6,15,16-亚氨基 podocarpane-8,11,13-三烯。首先用 NCS 在二氯甲烷中处理二环胺,生成相应的 N-氯衍生物;然后将该溶液在三氟乙酸中用 400 W 高压汞灯在氮气气氛下照射数小时,获得中等产率的产物32。
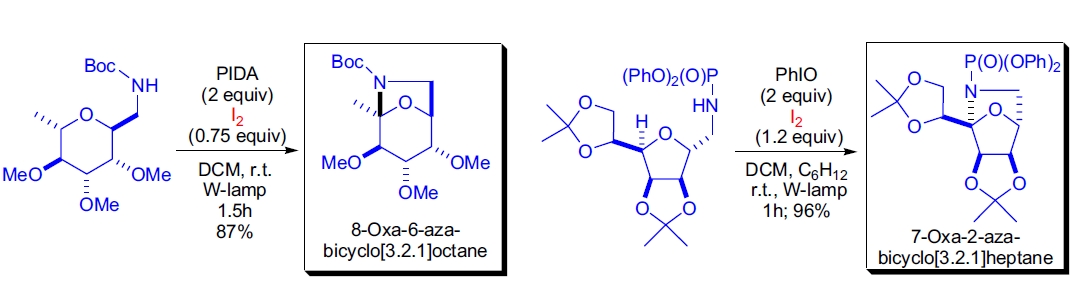
2. 氧杂-氮杂双环环系的合成: E. Suárez 等人通过 Suárez 改进,从氨基糖醇的苯基和苄基酰胺磷酸酯及其碳酸酯衍生物制备了 7-氧杂-2-氮杂双环[3.2.1]辛烷和 8-氧杂-6-氮杂双环[3.2.1]辛烷环系。用 PIDA/I₂ 或 PhIO/I₂ 处理生成的氮中心自由基发生分子内 1,5-氢原子抽取,生成烷基自由基,在反应条件下氧化为稳定的羰氧鎓离子,最终实现分子内 N-糖苷化22。
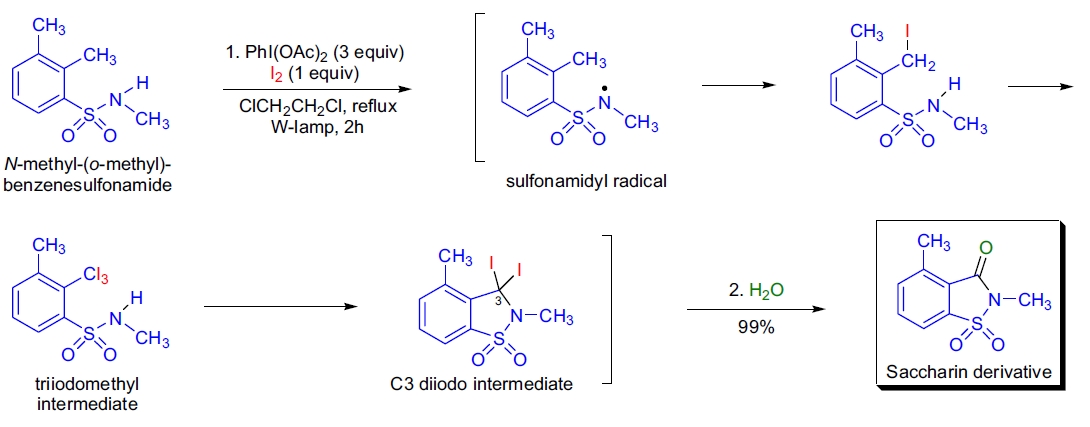
3. N-烷基苯并异噻唑啉酮-1,1-二氧化物的合成: H. Togo 等人以 Suárez 改进为基础,利用二乙酰氧基碘芳烃与碘反应,通过磺酰胺自由基制备了 N-烷基苯并异噻唑啉酮-1,1-二氧化物。反应在黑暗中不进行,表明其为自由基反应。产率从中等到优异不等,底物和二乙酰氧基碘芳烃的芳基取代基对反应有重要影响33。