Hofmann 重排反应
重要性
[开创性文献1-5;综述6-15;改进与优化16-30]
1881年,A.W. Hofmann 发现用一当量的溴(Br₂)和氢氧化钠或钾处理乙酰胺可以生成 N-溴乙酰胺。进一步去质子化并加热后,N-溴乙酰胺生成一种不稳定的盐,该盐在无水条件下容易重排为甲基异氰酸酯1。然而,在水和过量碱的存在下,产物为甲胺。将伯酰胺转化为相应的少一个碳的胺的过程被称为 Hofmann 重排反应(也称为 Hofmann 反应)。
Hofmann 重排反应的主要特点包括:
- 次卤酸盐试剂通过将氯气或溴加入氢氧化钾或钠的水溶液中现制而成;
- 传统碱性反应条件下,酰胺不能含有对碱敏感的官能团,但对酸敏感的基团(如缩醛)保持不变;
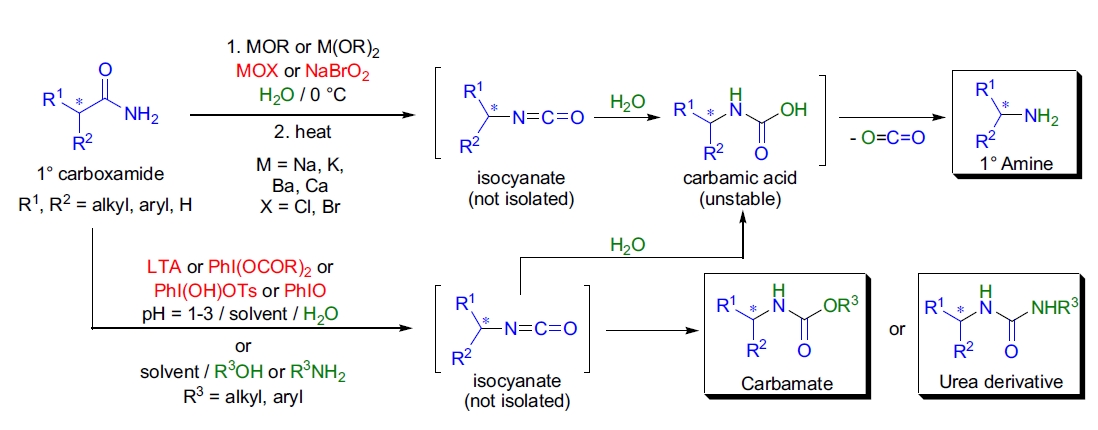
- 异氰酸酯中间体未被分离,因为在反应条件下它会迅速水解(或醇解)为通过不稳定氨基甲酸生成的相应少一个碳的胺;
- 在相转移催化条件下,可以分离出异氰酸酯31,25;
- 如果起始酰胺为光学纯(羰基直接连接到手性中心),产物胺的构型完全保留;
- Hofmann 重排反应对各种脂肪族和芳香族酰胺的产率都很高,且脂肪族酰胺的最佳产率出现在碳数不超过 8 的底物中(亲水性酰胺);
- α,β-不饱和酰胺和 α-羟基酸酰胺重排生成醛或酮32,33。
自发现以来,Hofmann 重排反应已被改进如下:
- 对于疏水性酰胺,使用甲醇钠次溴酸盐(通过将溴加入甲醇中的甲醇钠制得)可以高产率生成相应的甲基氨基甲酸酯6;
- 对于酸碱敏感底物,开发了中性电化学诱导的 Hofmann 重排反应18,26,28;
- 对于碱敏感底物,可使用 LTA 或高价碘试剂(如 PIDA、PIFA、PhI(OH)OTs 等)在温和酸性条件下进行氧化性 Hofmann 重排16,23,14,29;
- 在高价碘试剂或 LTA 存在下,当存在胺或醇时,生成的异氰酸酯原位转化为相应的氨基甲酸酯或脲衍生物17。
机理
[参考文献34-40,19,41]
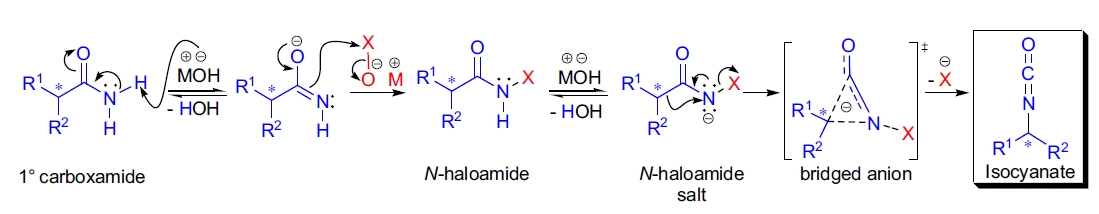
Hofmann 重排反应的机理与 Curtius、Lossen 和 Schmidt 重排密切相关。第一步是生成 N-卤代酰胺。接着,N-卤代酰胺被碱去质子化,形成一种相应的不稳定碱盐,该盐通过桥式阴离子发生协同重排生成异氰酸酯。这一机理得到了动力学证据的强有力支持36-39。因此,Hofmann 重排反应具有完全的构型保留。
合成应用
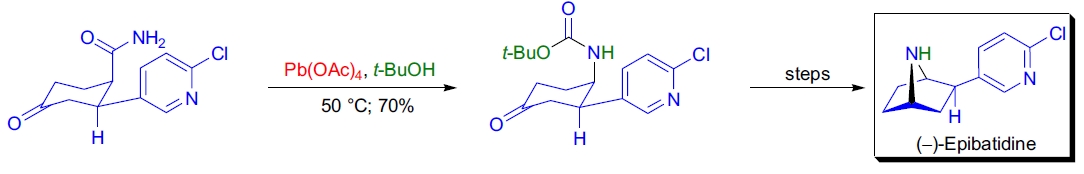
1. (–)-Epibatidine 的全合成: D.A. Evans 实验室通过异 Diels-Alder 反应和改进的 Hofmann 重排反应实现了 (–)-Epibatidine 的对映选择性全合成。在 t-丁醇中用四乙酸铅处理伯酰胺进行重排,生成 N-Boc 保护的伯胺,产率良好42。
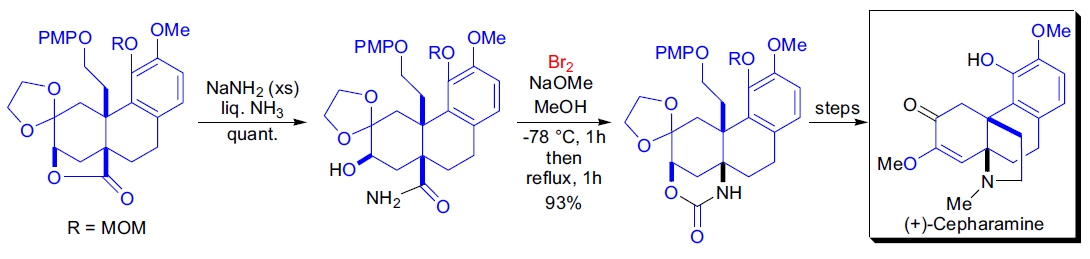
2. (+)-Cepharamine 的首次不对称全合成: A.G. Schultz 等通过 Hofmann 重排反应构建了 cis-融合 N-甲基吡咯烷环。高级四环内酯用液氨中的钠胺处理生成伯酰胺,再用甲醇中的次溴酸钠重排,初步生成异氰酸酯,随后与自由的仲醇分子内反应,生成环状氨基甲酸酯,产率极高43。
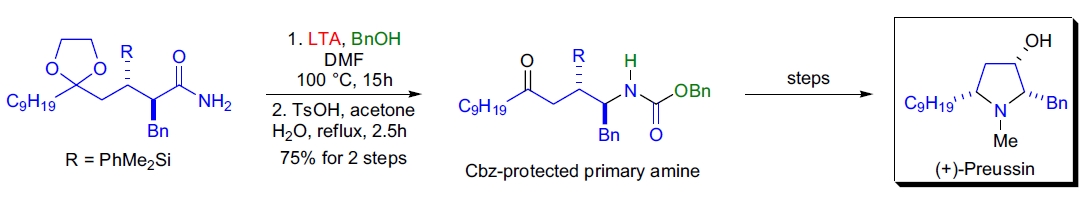
3. (+)-Preussin 的全合成: R. Verma 等人开发了一种硅控全合成方法,利用改进的 Hofmann 重排反应合成抗真菌剂 (+)-Preussin。伯酰胺在苯甲醇存在下用 LTA 处理进行重排,生成 Cbz 保护的伯胺,且未丧失光学活性44。
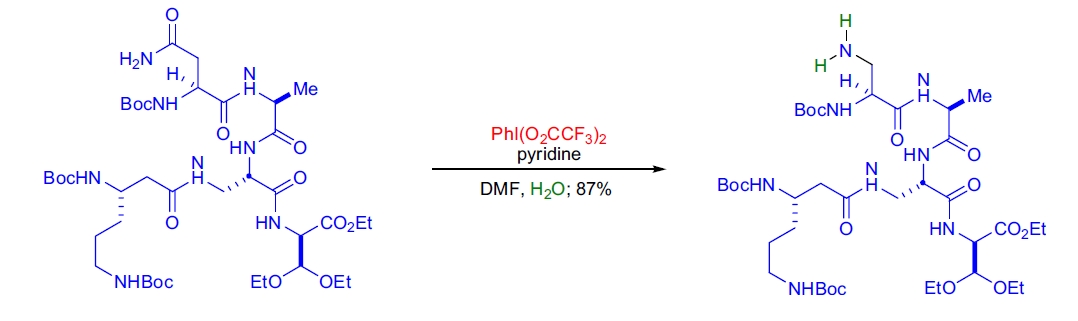
4. Capreomycidine IB 的全合成: R.M. Williams 等人在五肽合成的晚期阶段通过选择性 Hofmann 重排将天冬酰胺转化为二氨基丙酸。用 PIFA 和吡啶在水存在下处理,生成伯胺,产率高45。