Hunsdiecker 反应
重要性
[开创性文献1-3;综述4-7;改进与优化8-30]
1939年,H. Hunsdiecker 报道,当脂肪族羧酸的干燥银盐与溴反应时,可以生成相应的少一个碳的烷基溴2,3。脂肪族、α,β-不饱和及某些芳香族羧酸的卤代脱羧反应被称为 Hunsdiecker 反应。
该反应的主要特点包括:
- 银盐由相应的羧酸与氧化银反应制得;
- 银盐在四氯化碳中的悬浮液与等摩尔的卤素反应,反应过程中会释放二氧化碳;
- 银盐必须纯净且完全干燥才能获得高产率,这一过程较难实现,因为银盐通常对热敏感;
- 脂肪族羧酸是最好的底物,但带有吸电子基团的芳香族羧酸也适用;
- 电子丰富的芳香族羧酸在反应条件下会发生亲电芳香取代;
- 可用更稳定的铊(I)或汞(I)盐代替银盐;
- 对卤素反应敏感的基团(如烯烃、炔烃)在此条件下不兼容;
- 若使用光学活性银羧酸盐,生成的卤代烷中光学活性显著降低。
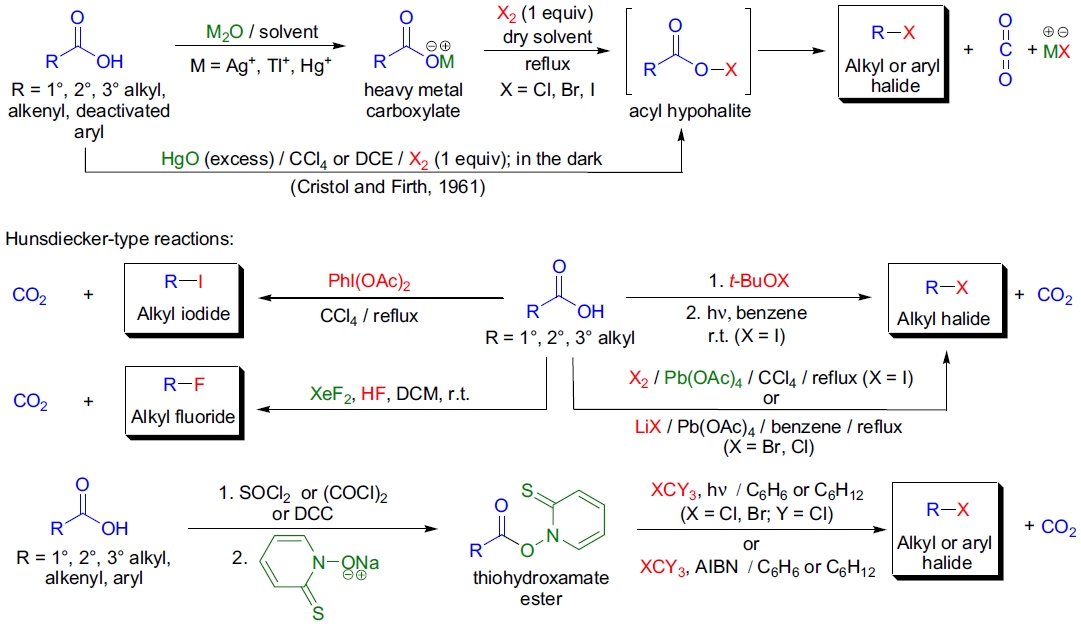
为了简化银羧酸盐的制备,提出了多种改进方法:
- 避免制备银羧酸盐,直接将酰氯溶液加入四氯化碳/溴的银氧化物悬浮液中,收率更高8,9;
- 用结晶性较好的铊(I)羧酸盐替代银盐,提高产率13;
- Cristol-Firth 改进法使用过量红色氧化汞和等摩尔卤素进行一锅法反应10;
- Suárez 改进法利用超价碘试剂处理羧酸,具有良好的官能团耐受性20;
- 通过 LTA 与碘或锂卤化物反应生成相应卤代烷(Kochi 改进法)11,6;
- Barton 改进法利用硫羟氨酸酯在卤素供体溶剂中的热解或光解反应,适用于几乎所有官能团17,19;
- 加入 AIBN 后,Barton 改进法可使任意芳香酸(活化和去活化)高产率脱羧31;
- 该反应可实现无金属催化,但可能遵循非自由基机理24,27,29。
机理
[参考文献4,32-37,29]
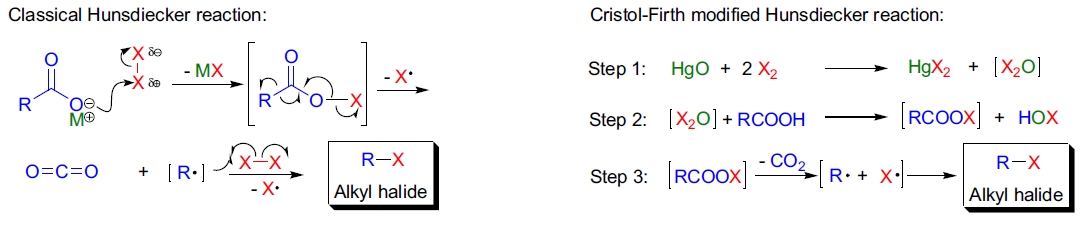
Hunsdiecker 反应的机理涉及羧酸盐的卤化,随后通过自由基途径脱羧生成卤代烷。反应中生成的自由基中间体由卤素与羧酸盐反应产生。
合成应用
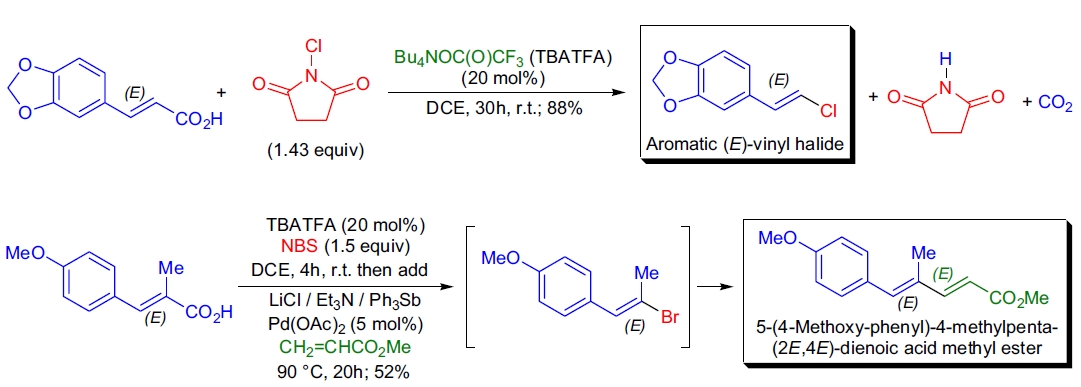
1. (E)-卤代烯烃的合成: S. Roy 研究表明,Hunsdiecker 反应可实现无金属催化,用于从芳香 α,β-不饱和羧酸制备 (E)-卤代烯烃。该策略使用 TBATFA 催化剂和 N-卤代琥珀酰亚胺,室温下分次加入反应物,产率良好到优异27。
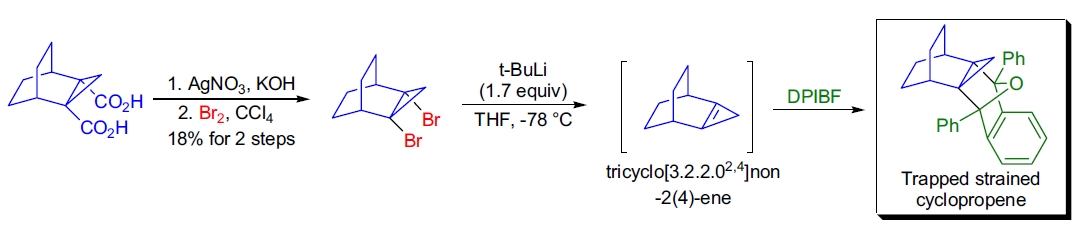
2. 高应力环丙烯的合成: P.J. Chenier 实验室利用经典的 Hunsdiecker 反应制备了三环[3.2.2.0²,⁴]壬-2(4)-烯。二酸通过 Diels-Alder 反应制备,但 Cristol-Firth 改进法未能反应,最终经典条件下生成了 1,2-二溴化物,进一步用 t-BuLi 处理后生成目标环丙烯38。
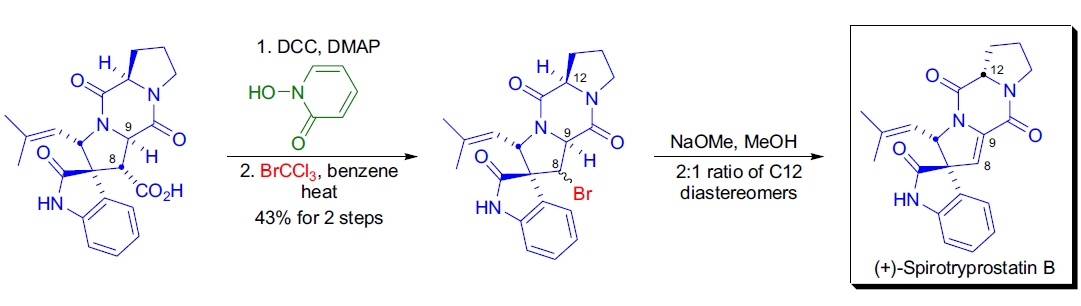
3. Spirotryprostatin B 的全合成: 在抗有丝分裂剂 (+)- 和 (-)-spirotryprostatin B 的全合成中,R.M. Williams 团队采用 Barton 改进法实现 C8-C9 双键的引入和羧基的去除。使用 LTA 或 PIDA 的其他方法均未成功,而 Barton 改进法通过在 C8 位引入溴基后,用甲醇钠处理生成目标化合物39。