Jones 氧化反应
重要性
[开创性文献1,2;综述3-7]
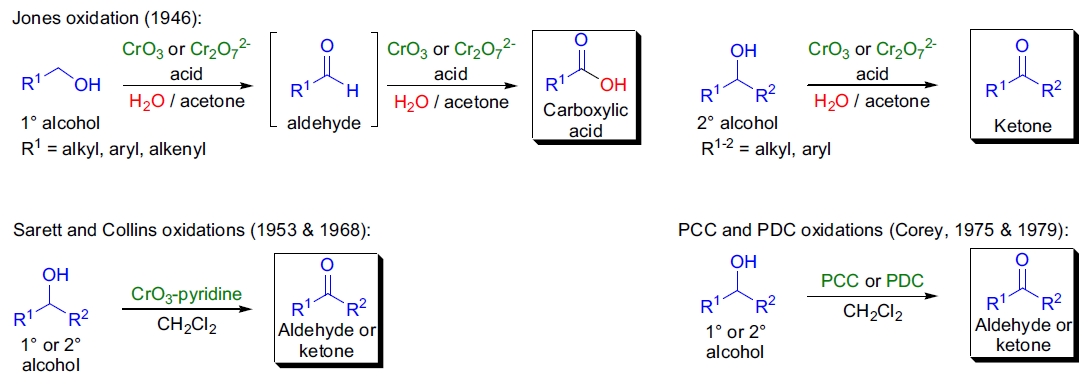
1946年,E.R.H. Jones 和其同事成功将炔基甲醇通过铬酸(CrO₃ 和稀硫酸混合物)氧化为相应的炔基酮,而未氧化敏感的三键1。该反应在丙酮中进行,通过将水相铬酸缓慢加入底物实现,在室温下高产率获得目标产物。利用铬酸氧化伯醇和仲醇被称为 Jones 氧化。
该反应具有以下特点:
- 铬酸 (H₂CrO₄) 可通过将铬酸酐 (CrO₃) 或重铬酸盐溶解于醋酸或稀硫酸中制备;
- 氧化通常在丙酮中进行,丙酮不仅溶解有机底物,还可与过量氧化剂反应保护产物免受过氧化;
- 通常通过滴定将氧化剂的水溶液加入醇类底物中;
- 应避免使用过量试剂,因为底物的其他官能团可能被氧化;
- 适用于大规模氧化;
- 伯醇氧化生成羧酸,中间生成的醛有时可通过蒸馏分离;
- 仲醇氧化生成相应的酮;
- 烯丙基和苄基醇高效氧化为相应的醛,几乎无过氧化;
- 二醇和羟基酮在反应条件下经常发生C-C键断裂,但添加Mn²⁺或Ce³⁺可抑制该副反应;
- 孤立的双键和三键保持不变,但α,β-不饱和醛可能发生双键异构化;
- 刚性环系中,轴向醇反应速率高于赤道向醇;
- 酸敏感保护基容易被去除;
- 游离胺通常与 Jones 氧化不兼容,需要保护为对应的高氯酸盐。
机理
[参考文献21,9,22-24]
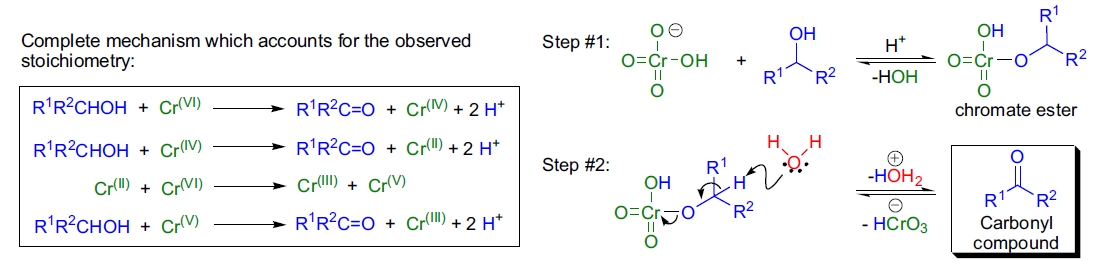
在水溶液中,铬酸的形式受浓度和 pH 影响:稀溶液中为单体形式 HCrO₄⁻,浓溶液中为二聚体 HCr₂O₇⁻。底物醇首先形成铬酸酯,然后经历限速基脱质子化生成 Cr(IV) 物种。该机理由 α-氘代醇氧化中的较大同位素效应支持。
合成应用
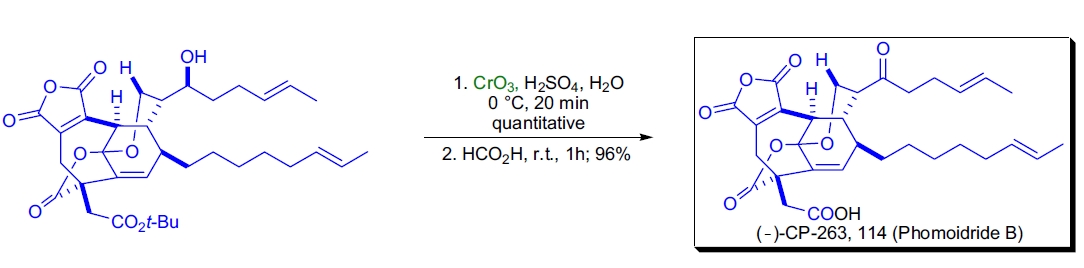
1. Phomoidride B 的全合成: T. Fukuyama 等人在天然产物 Phomoidride B 合成中,使用 Jones 氧化将碳骨架上的仲醇氧化为酮。氧化后脱去叔丁基酯,最终以96% 收率获得目标产物25。
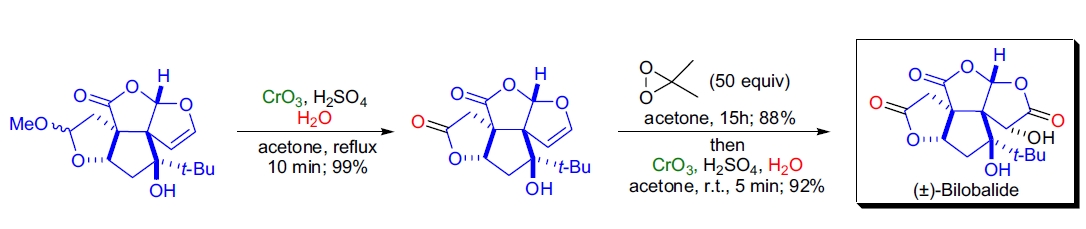
2. Bilobalide 的全合成: M.T. Crimmins 使用 Jones 氧化两次成功将五元内酯氧化为相应的内酯,随后通过多步反应完成了 Bilobalide 的全合成26。
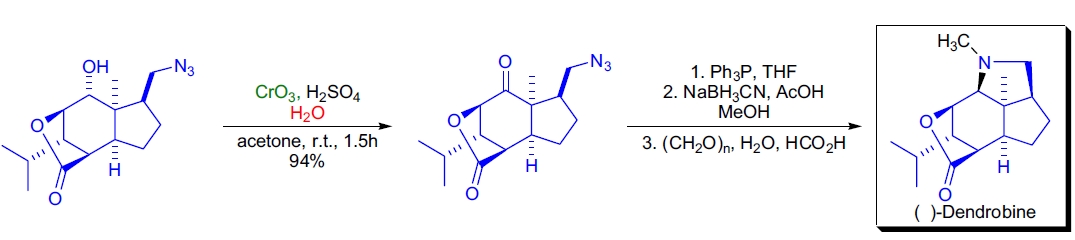
3. Dendrobine 的全合成: C.-K. Sha 通过 Jones 氧化将含叠氮基的仲醇中间体氧化为酮,并在后续步骤中完成天然产物 Dendrobine 的全合成27。
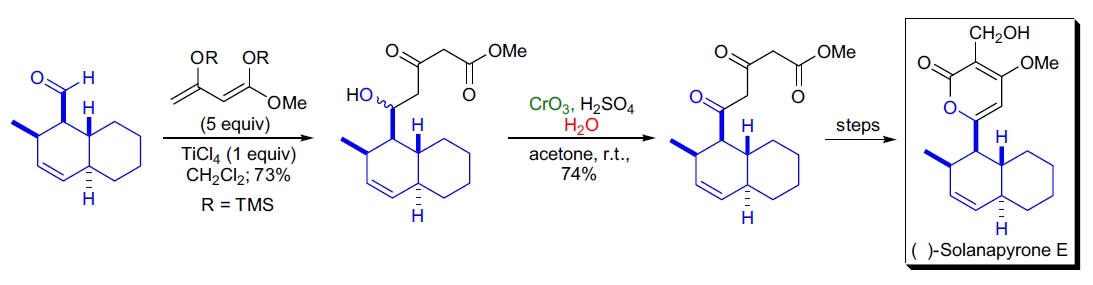
4. Solanapyrone E 的全合成: H. Hagiwara 使用 Jones 氧化在合成过程中氧化 α-羟基-β-酮酯为 α-二酮酯,高效生成关键中间体28。