Julia-Lythgoe 烯烃化反应
重要性
[开创性文献1;综述2-9;改进与优化10-22]
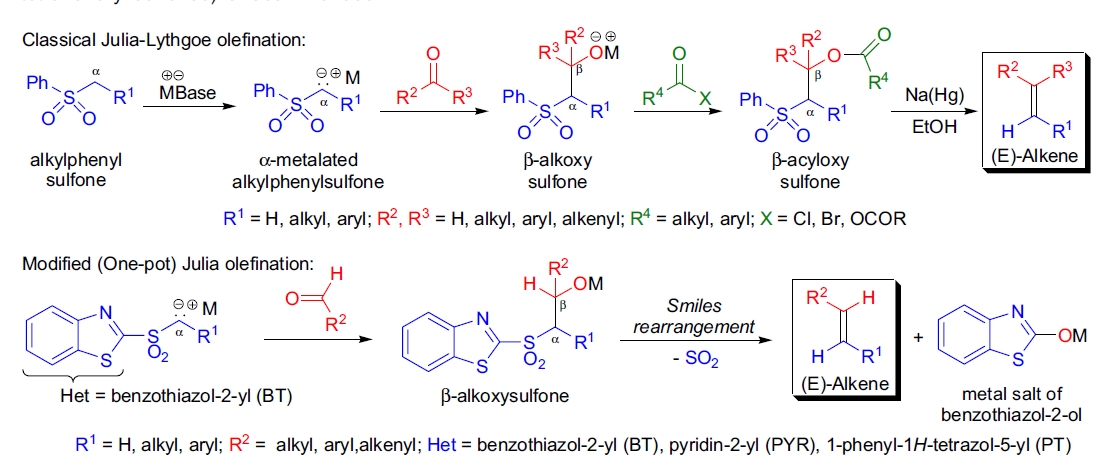
1973年,M. Julia 和 J.-M. Paris 报道了一种新型烯烃合成方法,其中 β-酰氧基磺酮通过单电子供体还原消除生成二、三或四取代烯烃1。该烯烃合成方法包括以下步骤:
- α-金属化芳基磺酮与醛或酮的加成;
- 生成的 β-烷氧基磺酮的酰化;
- β-酰氧基磺酮通过单电子供体还原消除生成目标烯烃。
这种方法后来被 B. Lythgoe 和 P.J. Kocienski 深入研究,并扩展了其适用范围。如今,该方法被称为 Julia-Lythgoe 烯烃化反应10-13。
- 高 (E)-选择性;
- (E)-选择性随双键周围支链的增加而提高;
- 中间体 β-酰氧基磺酮的相对构型不影响烯烃产物的几何选择性。
机理
[参考文献11,13,3,16]
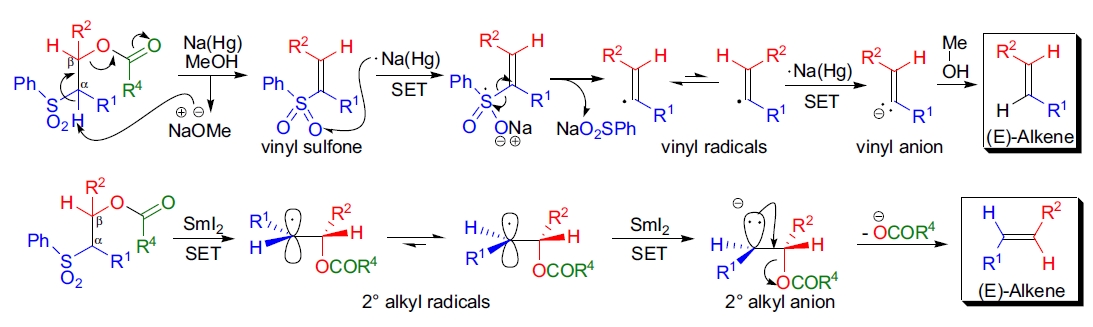
Julia-Lythgoe 反应的具体机理尚不完全清楚。通过氘标记研究表明,还原剂的种类(例如汞齐或 SmI₂)决定了中间体的类型(乙烯基自由基或仲烷基自由基)。这些中间体能够在生成产物前平衡为更稳定的异构体,导致高 (E)-选择性。
合成应用
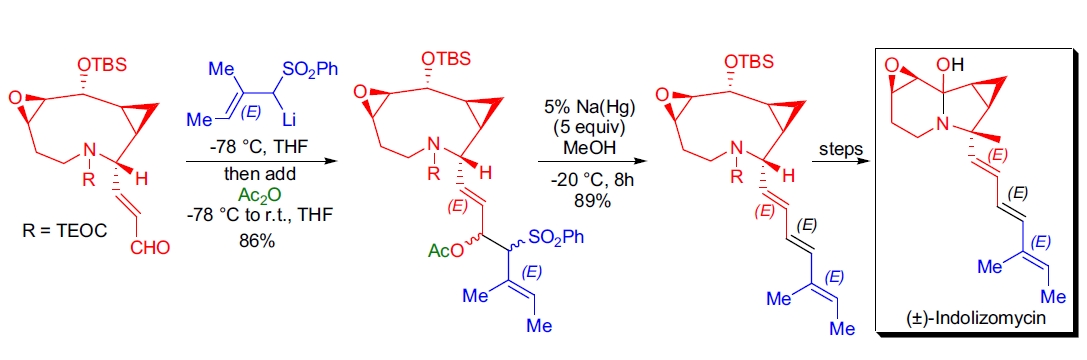
1. Indolizomycin 的全合成: S.J. Danishefsky 等人在其全合成中,通过经典 Julia-Lythgoe 反应构建三烯侧链。暴露于过量汞齐的条件下,高选择性地得到 (E,E,E) 三烯23。
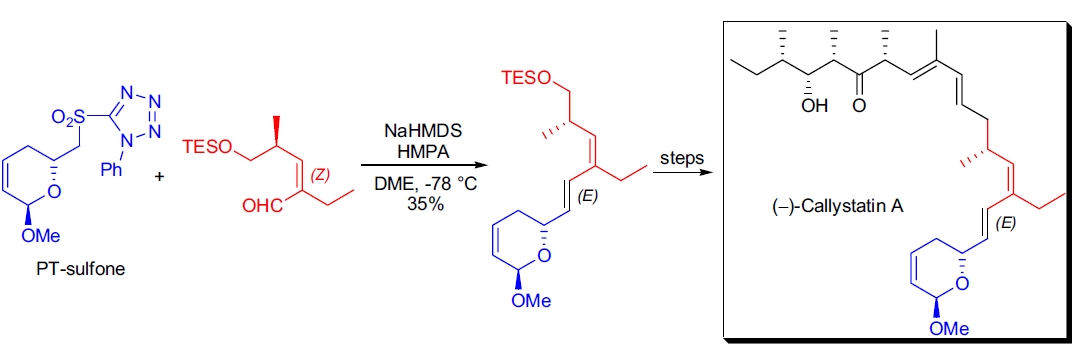
2. (–)-Callystatin A 的全合成: A.B. Smith 等人使用 Kocienski 改进的 Julia 反应引入两个 (E)-烯烃。由于 PT-磺酮的相对不稳定性,产率仅为中等24。
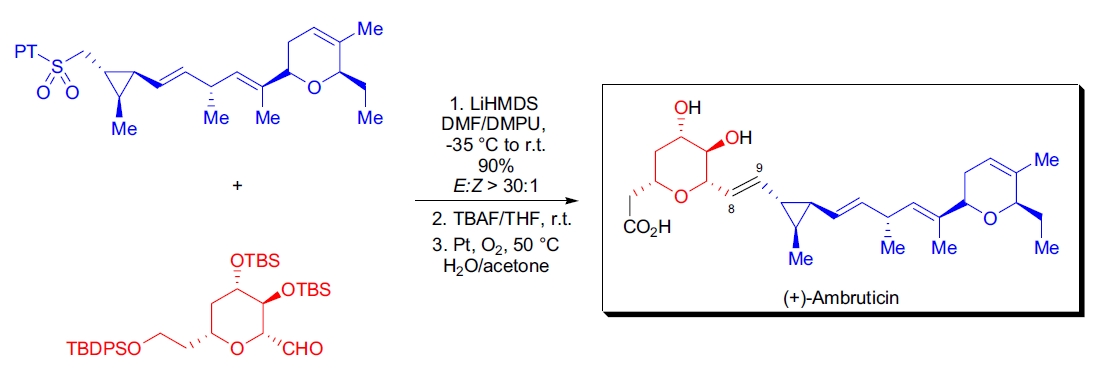
3. (+)-Ambruticin 的合成: E.N. Jacobsen 等人在合成过程中利用 Kocienski 改进 Julia 反应构建 C8-C9 (E)-烯烃。不同碱和溶剂条件下,产物立体选择性显著变化25。