Knoevenagel 缩合反应
重要性
[开创性文献1,2;综述3-10;改进与优化11-41]
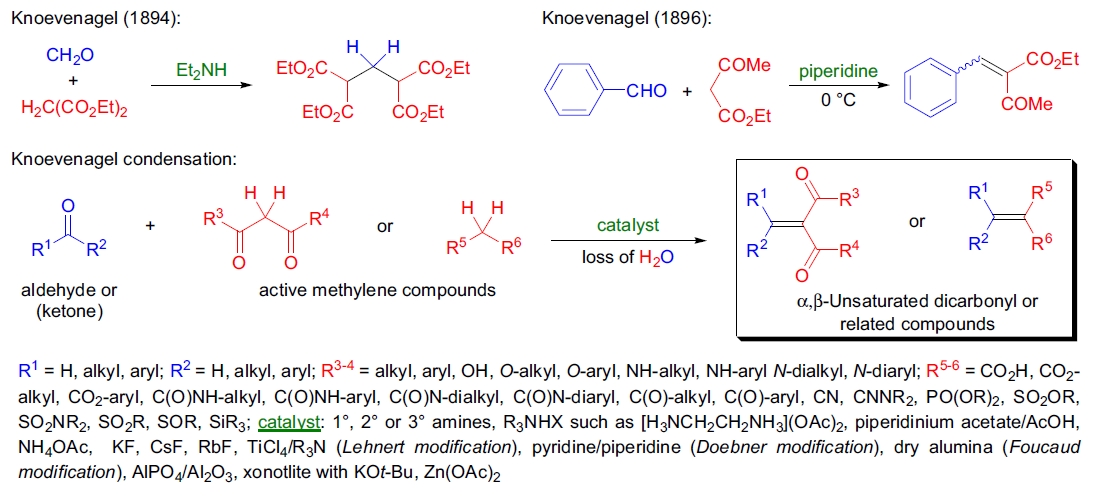
1894年,E. Knoevenagel 报道了二乙胺催化的二乙基丙二酸与甲醛的缩合反应,分离出双加成产物1。1896年,他用哌啶作为催化剂,在 0 °C 下使苯甲醛与乙酰乙酸乙酯反应,得到了乙酰乙酸苯亚甲酯作为唯一产物2。含活性亚甲基化合物与醛酮在弱碱条件下反应生成 α,β-不饱和二羰基化合物或类似化合物的反应被称为 Knoevenagel 缩合。该反应的特点包括:
- 醛比酮反应速率快;
- 活性亚甲基化合物需具有两个吸电子基团,如丙二酸酯、乙酰乙酸酯等;
- 催化剂通常为伯、仲、叔胺或其对应的铵盐,以及某些路易斯酸和胺的组合;
- 通过共沸蒸馏、分子筛或其他脱水剂可移除反应生成的水,推动反应平衡向产物方向移动;
- 溶剂选择很重要,极性非质子溶剂有助于提高反应效率;
- 生成的二羰基化合物可水解和脱羧生成 α,β-不饱和羰基化合物;
- 几何异构体选择性受位阻影响,热力学上更稳定的化合物通常为主要产物。
机理
[参考文献42,4,43-49,7,50-55]
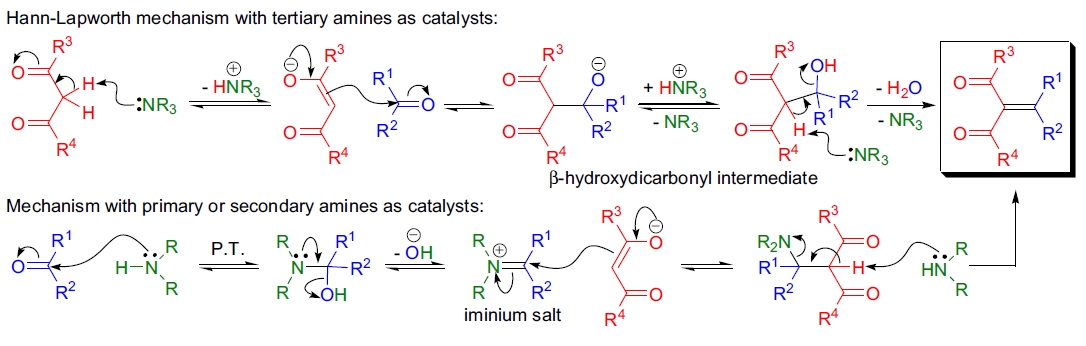
Knoevenagel 缩合是碱催化的 Aldol 型反应,其机理因底物和催化剂的类型而异。使用叔胺作为催化剂时,会生成 β-羟基二羰基中间体,脱水生成产物。而使用伯或仲胺催化时,醛和胺缩合生成亚胺盐,再与烯醇负离子反应,经过 1,2-消除步骤形成 α,β-不饱和二羰基化合物或类似物。最终产物可能与多余的烯醇负离子发生 Michael 加成,生成双加成产物。
合成应用
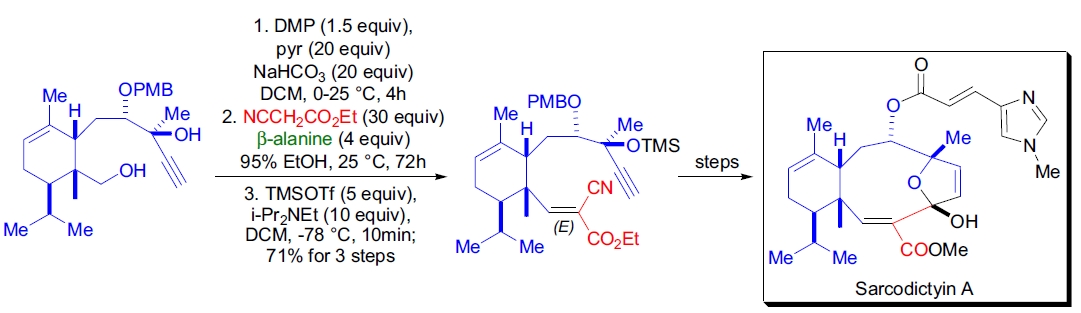
1. Sarcodictyin A 的全合成: K.C. Nicolaou 等利用 β-丙氨酸催化 Knoevenagel 缩合反应引入 α,β-不饱和醛基团,生成专一的 (E)-腈酯产物56。
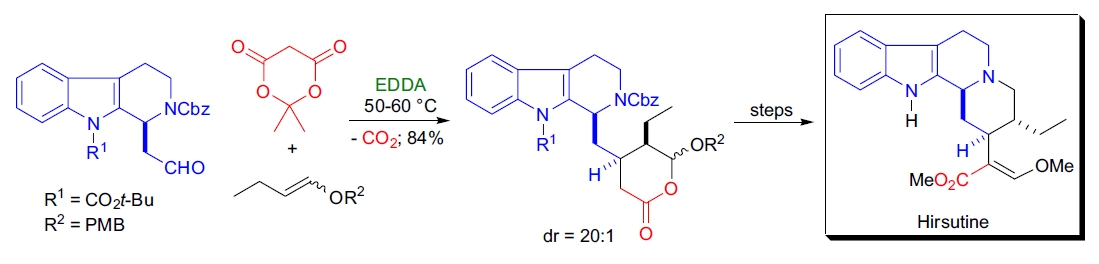
2. Hirsutine 的全合成: L.F. Tietze 等通过 Knoevenagel 缩合与杂-Diels-Alder 反应的串联反应合成了抗流感病毒活性生物碱 hirsutine。此缩合在乙二胺乙酸酯催化下进行,生成高度反应性的 1-氧代-1,3-丁二烯,随后与 4-甲氧基苯基丁烯醚发生 [4+2] 环加成57。
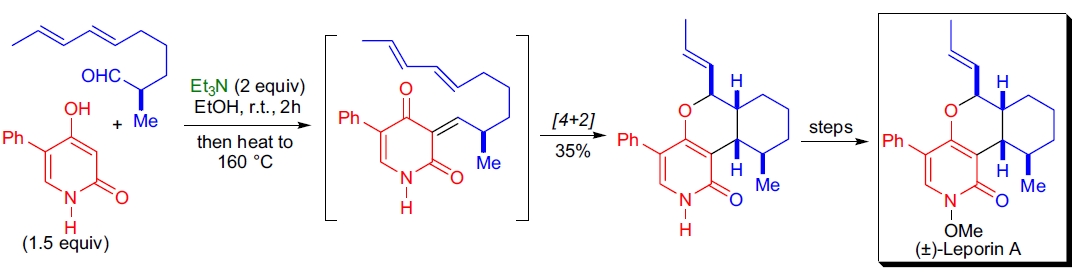
3. (±)-Leporin A 的全合成: B.B. Snider 等通过 Knoevenagel 缩合与逆电子需求的杂-Diels-Alder 反应构建了目标化合物的三环中间体58。
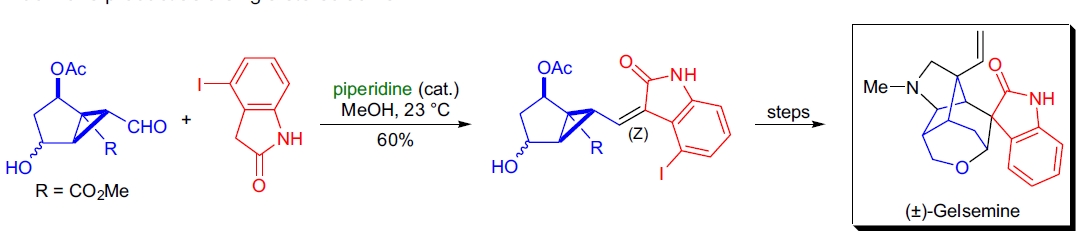
4. (±)-Gelsemine 的全合成: T. Fukuyama 等使用 Knoevenagel 缩合制备了关键的二烯基环丙烷-环庚二烯重排前体。4-碘氧杂吲哚作为活性亚甲基组分,生成了唯一立体异构的 (Z)-烯亚甲基吲哚酮59。