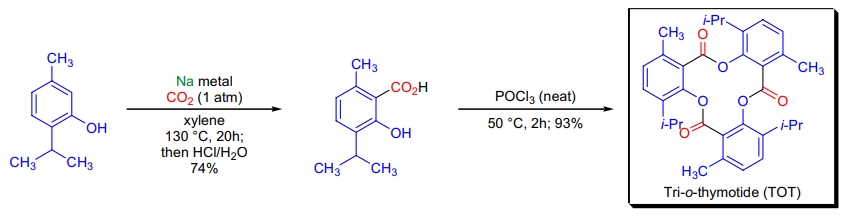
Kolbe-Schmitt 反应
重要性
[开创性文献1-4;综述5,6;改进与优化7-15;理论研究16,17]
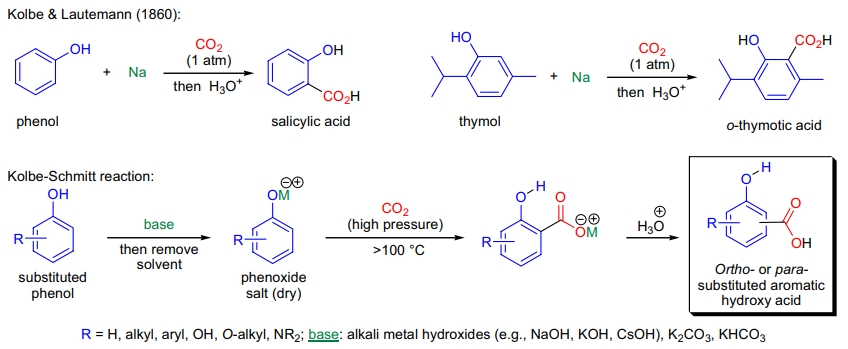
1860年,J. Kolbe 和 E. Lautemann 成功报道了通过在二氧化碳气氛下加热苯酚和金属钠,合成水杨酸(2-羟基苯甲酸)的方法1-3。同年,他们还发表了对对甲酚和麝香草酚的类似转化,分别得到对应的对甲基水杨酸和邻麝香草酸4。这种初始方法具有不稳定性,产率变化较大。1884年,R. Schmitt 发现将干燥的苯酚钠盐在密封管中暴露于高压二氧化碳气体,并加热至100 °C以上,可定量得到相应的水杨酸衍生物7,8。
- 该反应适用于苯酚、取代苯酚、萘酚和电子丰富的杂环化合物(如羟基吡啶、咔唑等);
- 单羟基苯酚需先转化为相应的碱金属或碱土金属酚盐(如Na、K、Mg、Ca、Ba),干燥后在高压二氧化碳气体下加热;
- 多羟基苯酚可在常压下用二氧化碳羧化;
- 反应混合物简单酸化即可得到目标产物芳香羟基酸;
- 碱金属离子的大小显著影响取代位置:使用较大的碱金属离子(如 Rb⁺ 或 Cs⁺)生成对羟基苯甲酸衍生物,而较小的离子(如 Na⁺ 或 K⁺)则生成水杨酸衍生物14;
- 微量水分的存在会显著降低产率,因此反应物、试剂和溶剂需彻底干燥后使用。
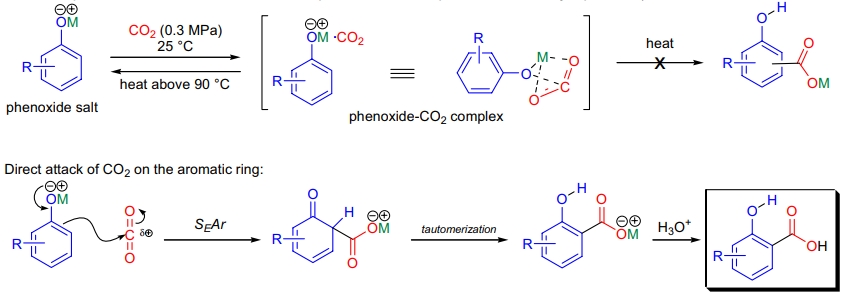
机理
[参考文献8,18,5,19-24,15]
Kolbe-Schmitt 反应的机理自19世纪末起受到研究,但直到100多年后才被阐明。长期以来的观点认为,二氧化碳首先与碱金属酚盐形成复合物,然后在高温下转化为芳香羧酸盐8,18。然而,Y. Kosugi 等的研究显示,此复合物并非反应的中间体,因为复合物在90 °C以上开始分解为酚盐17。研究还表明,羧化产物在200 °C左右仍具有热稳定性17。二氧化碳电亲试剂直接进攻芳环,生成邻位或对位产物(较大的对位产物由较大的阳离子如 Cs⁺ 优先生成)。
合成应用
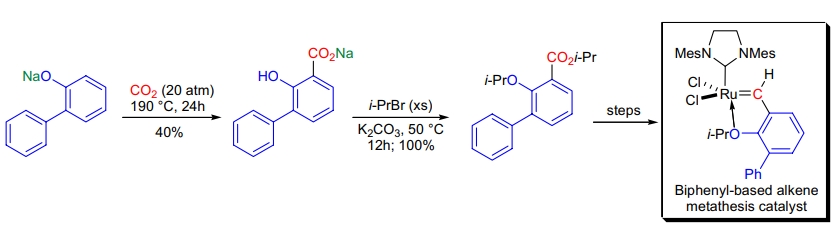
1. 烯烃复分解催化剂的合成: S. Blechert 等在大规模合成高效烯烃复分解催化剂时,使用 Kolbe-Schmitt 反应从 2-羟基联苯制备羧化衍生物。该催化剂对含非保护螯合原子的底物的开环交叉复分解表现出优异的效果25。
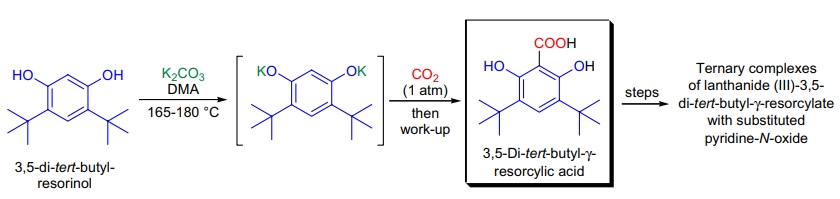
2. 3,5-二叔丁基-γ-间苯二酚酸的合成: Y.-C. Gao 等利用 Kolbe-Schmitt 反应,在常压条件下用二氧化碳羧化 4,6-二叔丁基间苯二酚,制备了 3,5-二叔丁基-γ-间苯二酚酸,用于构建镧系金属配合物26。
3. (+)-Pulvilloric 酸的对映选择性全合成: H. Gerlach 等在合成的最后阶段,使用 Kolbe-Schmitt 反应在常压二氧化碳气氛下引入羧基官能团,最终完成了此真菌代谢物的合成28。